Clear Sky Science · de
Entwicklung eines innovativen Nanopolymer-lncRNA-SRHC-Komplexes als therapeutische Modalität für eine gezielte Therapie des hepatozellulären Karzinoms
Warum diese Forschung für Leberkrebs wichtig ist
Primärer Leberkrebs, insbesondere das hepatozelluläre Karzinom, gehört zu den tödlichsten Krebsarten weltweit und bleibt oft unentdeckt, bis die Behandlungsmöglichkeiten begrenzt sind. Diese Studie untersucht einen neuen Ansatz, um Lebertumoren aufzuhalten, indem ein schützender „Nano“-Träger mit einem natürlich vorkommenden RNA-Molekül kombiniert wird, das in gesunden Lebern das Zellwachstum reguliert. Die Arbeit, durchgeführt an Mäusen, stützt sich auf humanes Datenmaterial und deutet auf eine schonendere, präzisere Therapie hin als die traditionelle Chemotherapie.
Ein fehlender Sicherheitsschalter in Leberzellen
Gesunde Leberzellen produzieren ein langes RNA-Molekül namens SRHC, das keine Proteine kodiert, aber hilft, Wachstumssignale im Gleichgewicht zu halten. Beim Leberkrebs sinken die SRHC-Spiegel stark, wodurch eine wichtige Bremse der Zellteilung entfällt. Frühere Studien deuteten darauf hin, dass die Wiederherstellung von SRHC das Wachstum von Leberkrebszellen im Labor verlangsamen oder stoppen kann, doch das Molekül ist fragil und im Körper leicht zu zerstören. Die Autoren nutzten große Datenbanken zu menschlichen Tumoren, um zunächst zu bestätigen, dass SRHC im normalen Lebergewebe reichlich vorhanden, im hepatozellulären Karzinom jedoch durchgängig verringert ist — ein Befund, der die Annahme untermauert, dass es als Tumorsuppressor wirkt und therapeutisch nutzbar sein könnte.
Aufbau eines winzigen Transportvehikels
Um SRHC in geschädigte Lebern zurückzubringen, griff das Team zur Nanotechnologie. Sie bauten mikroskopische Kügelchen aus einem bekannten biologisch abbaubaren Material namens PLGA, das bereits in Medizinprodukten verwendet wird. SRHC-Stränge wurden beim Entstehen der Partikel eingemischt, sodass die RNA fest in die Polymerhülle eingebettet wurde. Messungen zeigten, dass die resultierenden Nanopartikel etwa 200 Nanometer groß waren — klein genug, um durch undichte Tumorblutgefäße zu gelangen, aber groß genug, um einen schnellen Verlust über die Nieren zu vermeiden — und eine starke Oberflächenladung aufwiesen, die ein Zusammenklumpen verhindert und die Interaktion mit Zellmembranen fördert. In Zellkulturtests mit menschlichen Leberkrebszellen reduzierten sowohl freies SRHC als auch SRHC-beladene Nanopartikel das Überleben der Krebszellen, wobei die Nanoformulierung eine etwas stärkere Wirkung zeigte.
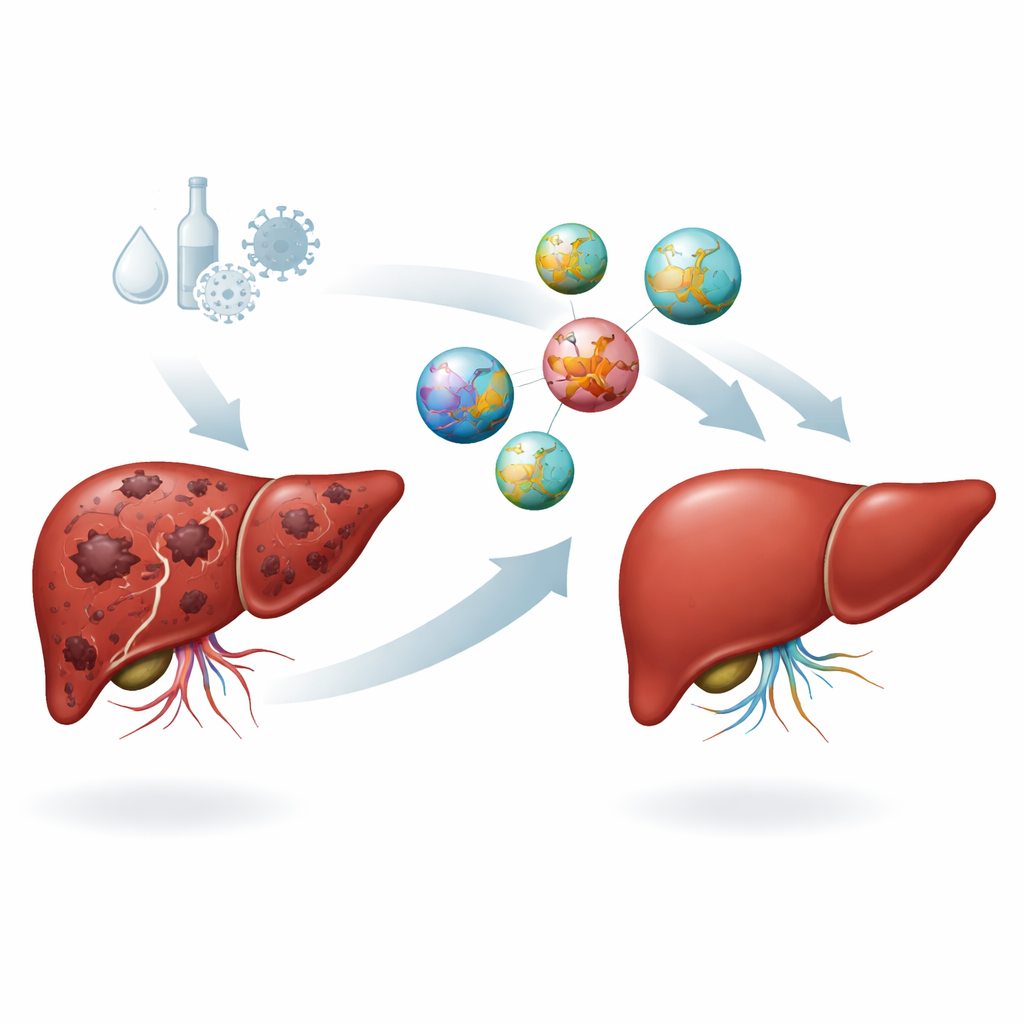
Test der Therapie in einem lebenden Organismus
Der eigentliche Test fand in einem Mausmodell für Leberkrebs statt, das durch Langzeitexposition gegenüber einem chemischen Karzinogen erzeugt wurde. Eine Gruppe von Mäusen blieb gesunde Kontrolle, während andere Lebertumoren entwickelten und dann entweder keine Behandlung, leere Nanopartikel, freies SRHC oder SRHC-beladene Nanopartikel direkt in die Leber injiziert bekamen. Über sechzehn Wochen verfolgten die Forschenden Blutmarker, die mit Tumorwachstum assoziiert sind, darunter Alpha-Fetoprotein und mehrere Signale, die Neubildung von Blutgefäßen und Entzündungen antreiben. Mäuse, die nur dem Karzinogen oder leeren Nanopartikeln ausgesetzt waren, zeigten sehr hohe Werte all dieser Marker und bestätigten so eine aggressive Erkrankung. Im Gegensatz dazu senkten sowohl SRHC als auch SRHC–Nanopartikel die Tumorsignale deutlich, wobei der kombinierte Nano-SRHC-Ansatz den größten Rückgang bewirkte.
Ein Blick in Gene und Gewebestruktur
Um zu verstehen, was in der Leber vor sich ging, untersuchte das Team Schlüsselgene und Gewebeschnitte. Bei unbehandelten tumortragenden Mäusen waren Gene, die Wachstum und Ausbreitung fördern (SENP1 und β‑Catenin), stark aktiv, während ein Gen, das die normale Leberidentität aufrechterhält (HNF‑4α), stark unterdrückt war. Freies SRHC kehrte dieses Muster teilweise um, doch die SRHC–Nanopartikel-Behandlung tat dies noch kraftvoller, indem sie die krebsfördernden Signale reduzierte und das schützende Gen wiederherstellte. Die mikroskopische Untersuchung bestätigte das Bild: Lebern aus unbehandelten oder leeren‑Nanopartikel‑Gruppen waren desorganisiert, voller abnormaler Zellen und neuer Gefäße, während SRHC‑behandelte Lebern weniger maligne Veränderungen zeigten. Die Nano‑SRHC‑Gruppe kam dem Normalzustand am nächsten, mit klarerer Läppchenstruktur und Anzeichen einer aktiven Immun‑Beseitigung restlicher Tumorzellen. Wichtig ist, dass keine Behandlungsgruppe offensichtliche Anzeichen von Toxizität oder Unwohlsein zeigte.
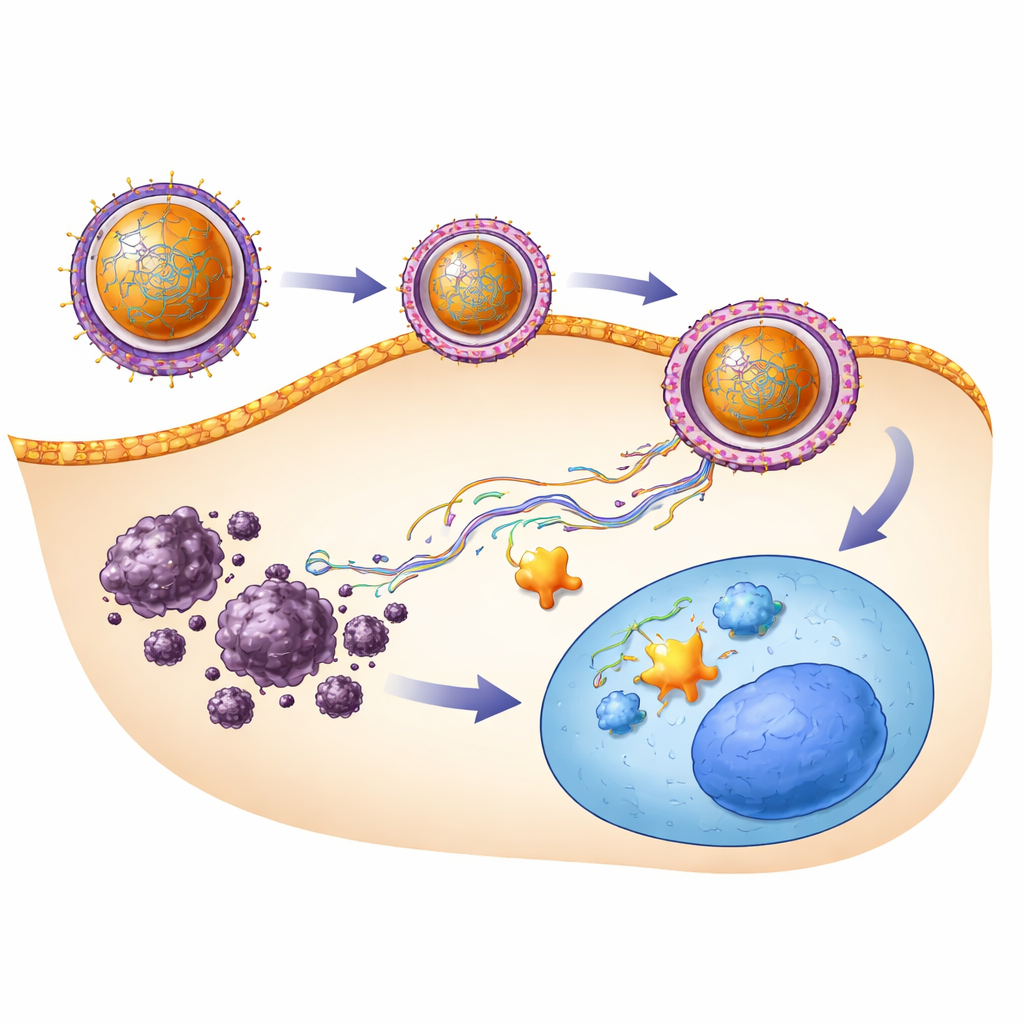
Was das für künftige Behandlungen bedeuten könnte
Kurz gesagt zeigt diese Studie, dass das Ersetzen eines fehlenden „Bremse“-Moleküls in Leberzellen und dessen Schutz durch einen intelligenten Nano‑Träger Leberkrebs bei Mäusen verlangsamen oder rückgängig machen kann, ohne offensichtlichen Schaden zu verursachen. Der SRHC–Nanopartikel‑Komplex reduzierte nicht nur Tumormarker und gefährliche Wachstumssignale, sondern trug auch zur Wiederherstellung der normalen Leberarchitektur bei. Obwohl noch viel Arbeit nötig ist, bevor ein solcher Ansatz für Patientinnen und Patienten verfügbar ist — einschließlich der Verfeinerung der Verabreichungswege, der Sicherstellung der Langzeitsicherheit und der Kombination mit bestehenden Medikamenten — heben diese Ergebnisse eine vielversprechende Strategie hervor: ingenieurtechnisch hergestellte Partikel zu nutzen, um fragile genetische Regulatoren dorthin zurückzubringen, wo sie hingehören, und Krebs von innen heraus zu dämpfen.
Zitation: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
Schlüsselwörter: hepatozelluläres Karzinom, Nanopartikeltherapie, lange nichtkodierende RNA, Leberkrebsbehandlung, gezielte Wirkstofffreisetzung