Clear Sky Science · pl
Opracowanie innowacyjnego kompleksu nanopolimer‑lncRNA‑SRHC jako terapii celowanej dla raka wątrobowokomórkowego
Dlaczego te badania są ważne dla raka wątroby
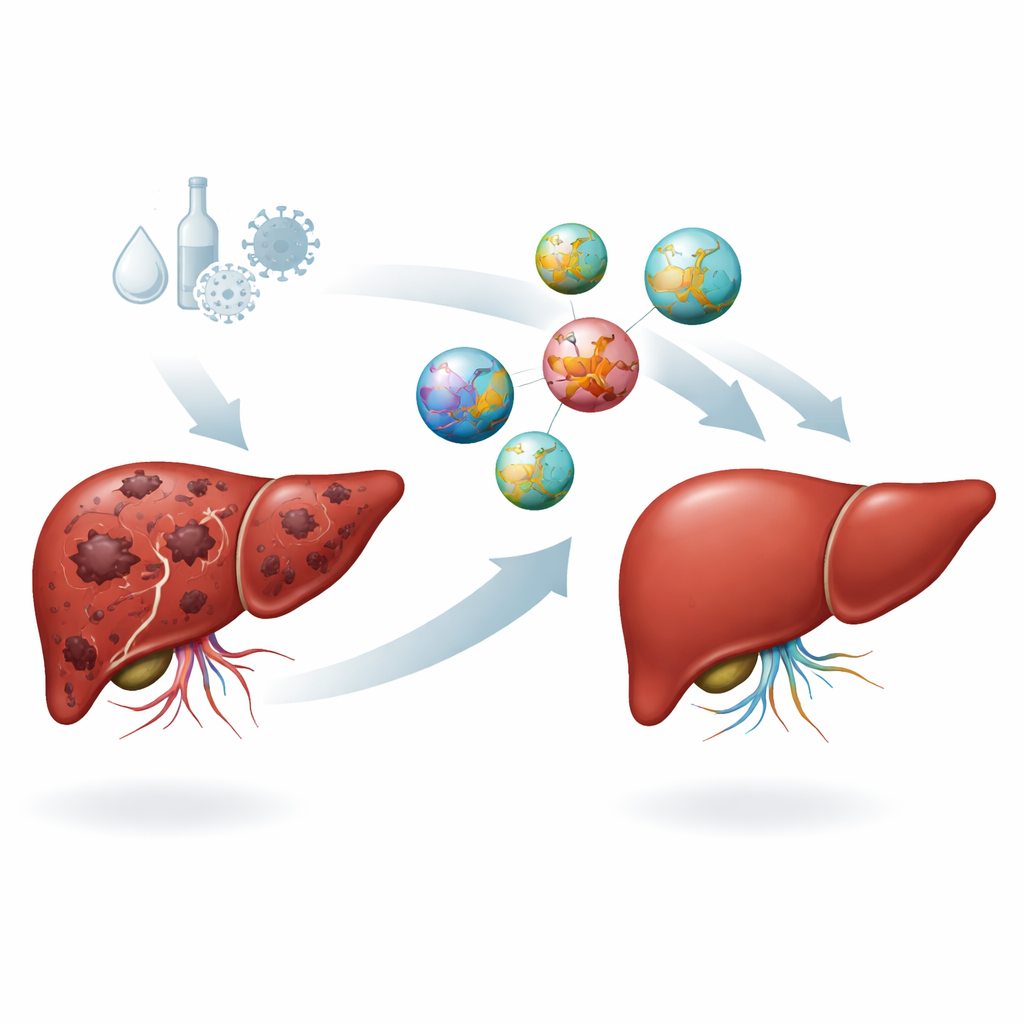
Pierwotny rak wątroby, w szczególności rak wątrobowokomórkowy, należy do najbardziej śmiertelnych nowotworów na świecie i często pozostaje niezauważony, aż możliwości leczenia są ograniczone. W tej pracy badano nowy sposób zatrzymania wzrostu guzów wątroby poprzez połączenie ochronnego nośnika „nano” z naturalnie występującą cząsteczką RNA, której zdrowa wątroba używa do kontroli podziałów komórkowych. Prace przeprowadzono na myszach, opierając się na danych ludzkich, i wskazują na łagodniejszą, bardziej precyzyjną terapię niż tradycyjna chemioterapia.
Brakujący przełącznik bezpieczeństwa w komórkach wątroby
Zdrowe komórki wątroby wytwarzają długą cząsteczkę RNA nazwaną SRHC, która nie koduje białka, ale pomaga utrzymać równowagę sygnałów wzrostu. W raku wątroby poziom SRHC gwałtownie spada, co usuwa ważny hamulec podziałów komórkowych. Wcześniejsze badania sugerowały, że przywrócenie SRHC może spowolnić lub zatrzymać komórki raka w warunkach laboratoryjnych, jednak cząsteczka ta jest krucha i łatwo ulega degradacji w organizmie. Autorzy najpierw wykorzystali obszerne bazy danych ludzkich guzów, aby potwierdzić, że SRHC jest obfity w prawidłowej tkance wątroby, ale konsekwentnie zmniejszony w raku wątrobowokomórkowym, co wzmacnia przekonanie, że działa jako supresor guza i może być celem terapeutycznym.
Budowa mikroskopijnego nośnika
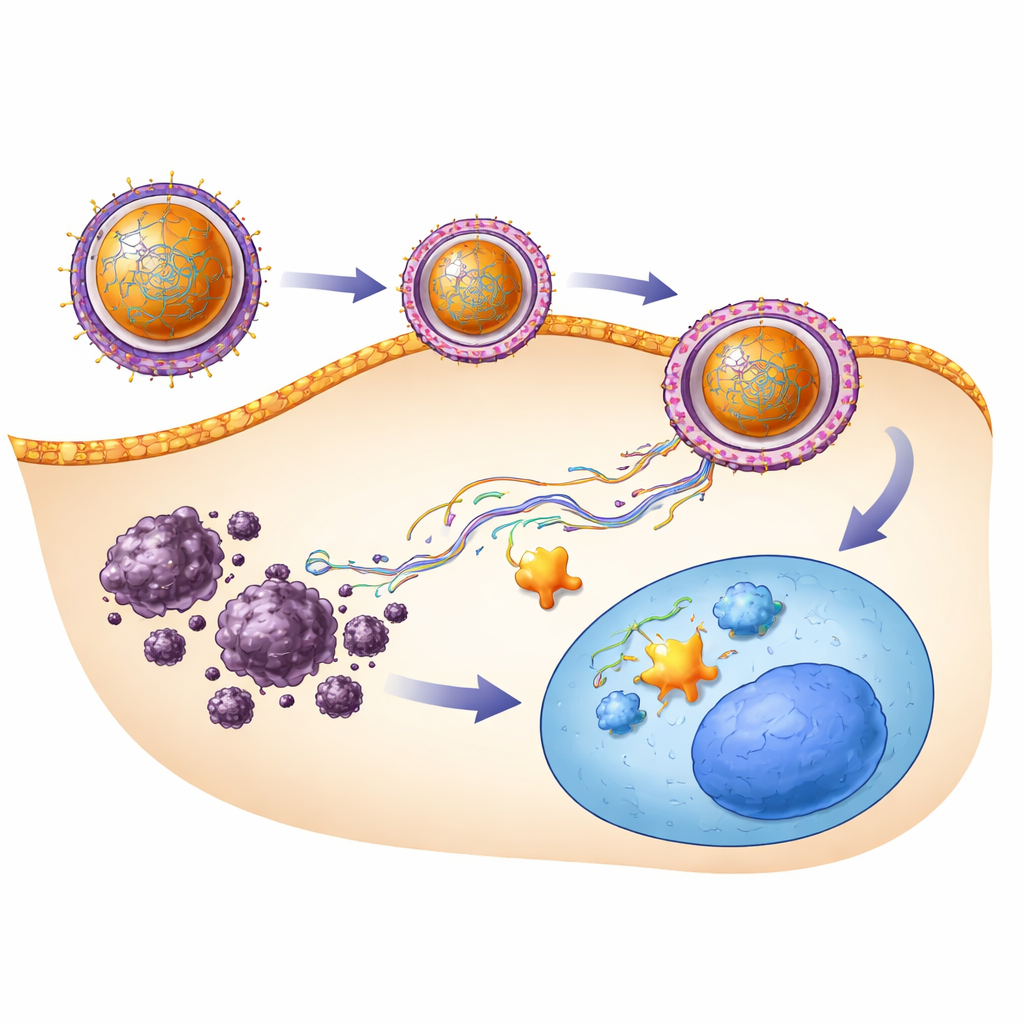
Aby dostarczyć SRHC do uszkodzonych wątrób, zespół sięgnął po nanotechnologię. Zbudowano mikroskopijne kulki z dobrze znanego biodegradowalnego materiału o nazwie PLGA, już stosowanego w produktach medycznych. Struny SRHC zostały wmieszane w tworzące się cząstki, tak że RNA zostało mocno osadzone w polimerowej powłoce. Pomiary wykazały, że powstałe nanocząstki miały około 200 nanometrów średnicy — na tyle małe, by przechodzić przez nieszczelne naczynia krwionośne guza, lecz na tyle duże, by uniknąć szybkiej utraty przez nerki — i miały silny ładunek powierzchniowy zapobiegający aglomeracji oraz wspomagający interakcję z błonami komórkowymi. W testach in vitro na ludzkich komórkach raka wątroby zarówno wolne SRHC, jak i nanocząstki z SRHC zmniejszały przeżywalność komórek nowotworowych, przy czym forma nano wykazywała nieco silniejsze działanie.
Testowanie terapii in vivo
Rzeczywisty test przeprowadzono na modelu myszy z rakiem wątroby wywołanym długotrwałą ekspozycją na chemiczny kancerogen. Jedna grupa myszy pozostała zdrową kontrolą, podczas gdy inne rozwinęły guzy wątroby, a następnie nie otrzymały leczenia, otrzymały puste nanocząstki, wolne SRHC lub nanocząstki z SRHC wstrzyknięte bezpośrednio do wątroby. Przez szesnaście tygodni badacze śledzili markery krwi związane ze wzrostem guza, w tym alfa‑fetoproteinę oraz kilka sygnałów napędzających tworzenie naczyń i zapalenie. Myszom leczonym tylko chemicznie lub pustymi nanocząstkami towarzyszyły bardzo wysokie poziomy wszystkich tych markerów, potwierdzając agresywny przebieg choroby. W przeciwieństwie do tego zarówno SRHC, jak i terapia SRHC–nanocząstki wyraźnie obniżyły sygnały nowotworowe, a podejście nano‑SRHC dało największy spadek.
Zaglądanie w geny i strukturę tkanki
Aby zrozumieć, co działo się wewnątrz wątroby, zespół zbadał kluczowe geny i preparaty tkankowe. U nieleczonych myszy z guzami geny promujące wzrost i rozprzestrzenianie się (SENP1 i β‑katenina) były wysoce aktywne, podczas gdy gen utrzymujący normalną tożsamość wątroby (HNF‑4α) był silnie tłumiony. Wolne SRHC częściowo odwróciło ten wzorzec, ale leczenie SRHC–nanocząstkami zrobiło to silniej, redukując sygnały sprzyjające nowotworowi i przywracając sygnał ochronny. Mikroskopowa ocena potwierdziła te obserwacje: wątroby z grup nieleczonych lub otrzymujących puste nanocząstki były zdezorganizowane, wypełnione nieprawidłowymi komórkami i nowymi naczyniami, podczas gdy wątroby po leczeniu SRHC wykazywały mniej zmian złośliwych. Grupa nano‑SRHC była najbliższa normalnej, z czytelniejszą strukturą zrazikową i oznakami aktywnego oczyszczania pozostałych komórek nowotworowych przez układ odpornościowy. Co ważne, żadna grupa leczona nie wykazała wyraźnych objawów toksyczności ani złego samopoczucia.
Co to może znaczyć dla przyszłych terapii
Krótko mówiąc, badanie pokazuje, że zastąpienie brakującej cząsteczki „hamulca” w komórkach wątroby i jej ochrona przez inteligentny nośnik nano może spowolnić lub odwrócić raka wątrobowokomórkowego u myszy bez widocznych szkód. Kompleks SRHC–nanocząstki nie tylko zmniejszał markery guza i niebezpieczne sygnały wzrostowe, lecz także pomagał odbudować normalną architekturę wątroby. Choć przed zastosowaniem u pacjentów pozostało jeszcze wiele pracy — w tym dopracowanie dróg dostarczania, zapewnienie długoterminowego bezpieczeństwa oraz łączenie z istniejącymi lekami — wyniki te wskazują obiecującą strategię: użycie zaprojektowanych cząstek do transportu delikatnych regulatorów genetycznych z powrotem tam, gdzie są potrzebne, aby od wewnątrz osłabić nowotwór.
Cytowanie: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
Słowa kluczowe: rak wątrobowokomórkowy, terapia nanopartikelami, długa niekodująca RNA, leczenie raka wątroby, celowane dostarczanie leków