Clear Sky Science · he
פיתוח קומפלקס חדשני של ננופולימר-lncRNA-SRHC כמודלים טיפוליים לטיפול ממוקד בסרטן הכבד ההפטוצלולי
מדוע המחקר הזה חשוב לסרטן הכבד
סרטן הכבד הראשוני, ובפרט הסרטן ההפטוצלולי, הוא מאחד הסרטנים הקטלניים ביותר בעולם ובמקרים רבים לא מאובחן עד שהאפשרויות הטיפוליות מוגבלות. מחקר זה בוחן גישה חדשה לעצור גידולים כבדיים על ידי שילוב של נשא ננו־ממגן יחד עם מולקולת RNA טבעית שהכבד הבריא משתמש בה כדי לווסת את גדילת התאים. העבודה נעשתה בעכברים אך נשענת על נתונים אנושיים, ומהווה כיוון לעבר טיפול עדין ומדויק יותר מאשר כימותרפיה מסורתית.
ממסך בטיחות חסר בתאי הכבד
תאי כבד בריאים מייצרים מולקולת RNA ארוכה בשם SRHC, שאינה מקודדת לחלבון אך מסייעת לשמור על איזון אותות הגדילה. בסרטן הכבד, רמות ה‑SRHC יורדות בחדות, ובכך מוסרת מעצור חשוב על חלוקות התא. מחקרים קודמים הציעו ששיחזור SRHC יכול להאט או לעצור תאי סרטן כבד במעבדה, אך המולקולה רגישה בקלות וניזוקה בגוף. החוקרים השתמשו תחילה במאגרי מידע רחבים של גידולים אנושיים כדי לאשר כי SRHC שגשג ברקמת כבד נורמלית אך יורד בעקביות בסרטן הכבד ההפטוצלולי, מחזק את הרעיון שהיא פועלת כמדכא גידול ויכולה לשמש כיעד טיפולי.
בניית כלי נשיאה זעיר
כדי להחזיר את ה‑SRHC לכבד הפגוע, הצוות פנה לננוטכנולוגיה. הם בנו כדורים מיקרוסקופיים מחומר ביודגרדבילי ידוע בשם PLGA, שכבר נמצא בשימוש במוצרים רפואיים. גדילי ה‑SRHC נמסרו לתוך החלקיקים המתהווים כך שה‑RNA נלכד בתוך מעטפת הפולימר. מדידות הראו שהננו־חלקיקים שהתקבלו היו כ‑200 ננומטר בקוטר—קטנים מספיק לעבור דרך כלי דם מנוקבים של הגידול אך גדולים דיים כדי למנוע אובדן מהיר דרך הכליות—ונשאו מטען פני שטח חזק שמונע שקיעה ומסייע באינטראקציה עם ממברנות התא. בניסויים בתרביות תאים עם תאי סרטן כבד אנושיים, גם SRHC חופשי וגם SRHC באריזת ננו הורידו את הישרדות תאי הסרטן, כאשר הננספירה הראתה פעילות מעט חזקה יותר.
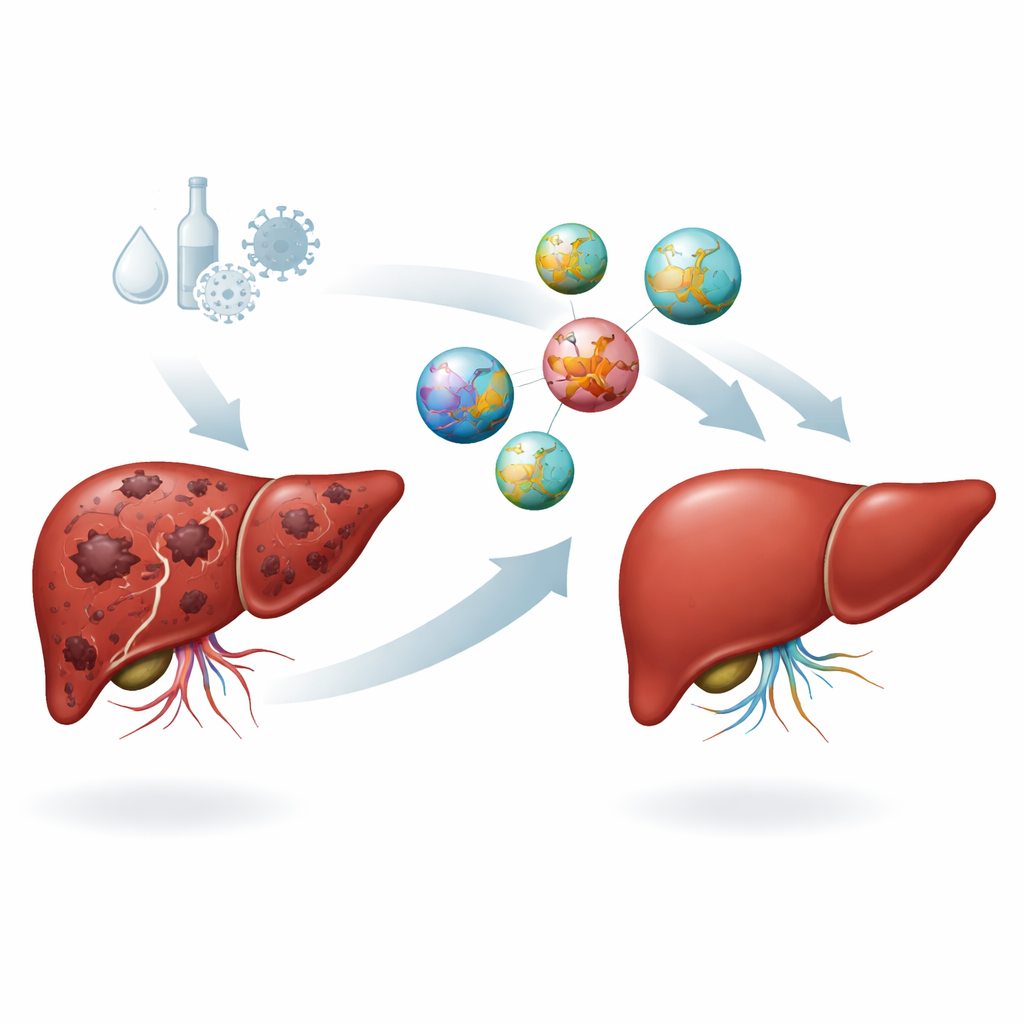
בדיקת הטיפול בעאזור חי
המבחן האמיתי נעשה במודל עכבר של סרטן הכבד שנוצר על ידי חשיפה ממושכת לקרצינוגן כימי. קבוצה אחת של עכברים נשמרה כבקרה בריאה, בעוד שאחרות פיתחו גידולים בכבד ואז קיבלו טיפול: ללא טיפול, ננו־חלקיקים ריקים, SRHC חופשי או ננו־חלקיקים טעונים ב‑SRHC שהוזרקו ישירות לכבד. במשך שישה עשר שבועות עקבו החוקרים אחרי סמני דם הקשורים לצמיחת הגידול, כולל אלפא‑פטופרוטאין וכמה אותות שמניעים יצירת כלי דם חדשים ודלקת. עכברים שטופלו רק בחומר הכימי או בננו־חלקיקים הריקים הראו רמות גבוהות מאוד של כל סמנים אלה, ואשררו מחלה אגרסיבית. לעומת זאת, גם טיפול ב‑SRHC וגם ב‑SRHC–ננו הורידו בחדות את סמני הגידול, כאשר הגישה המשולבת של ננו‑SRHC הניבה את הירידה הגדולה ביותר.
מבט לגנים ולמבנה הרקמה
כדי להבין מה מתרחש בתוך הכבד, הצוות בדק גנים מפתח ופרוסות רקמה. בעכברים נושאי גידול שלא טופלו, גנים המעודדים גדילה והתפשטות (SENP1 ובטא‑קטנין) היו פעילים מאוד, בעוד גן המשמר זהות כבדית נורמלית (HNF‑4α) היה מדוכא בחוזקה. SRHC חופשי הפך באופן חלקי דפוס זה, אך טיפול ב‑SRHC–ננו עשה זאת בעוצמה רבה יותר, הקטין את האותות המקודמים סרטן והשיב את הביטוי של הגן המגן. בדיקה מיקרוסקופית סיפקה תמונה דומה: כבדות מקבוצות שלא טופלו או מקבוצת הננו‑חלקיקים הריקים היו בלתי מסודרות, רוויות תאים לא תקינים וכלי דם חדשים, בעוד כבדות שטופלו ב‑SRHC הראו פחות שינויים ממאירים. קבוצת ננו‑SRHC התקרבה למצב הנורמלי ביותר, עם מבנה לובולרי ברור יותר וסימנים לפעילות חיסונית המנקת תאי גידול שאריתיים. חשוב לציין שלא נמצאו עדויות ברורות להרעלה או מצוקה בקבוצות המטופלות.
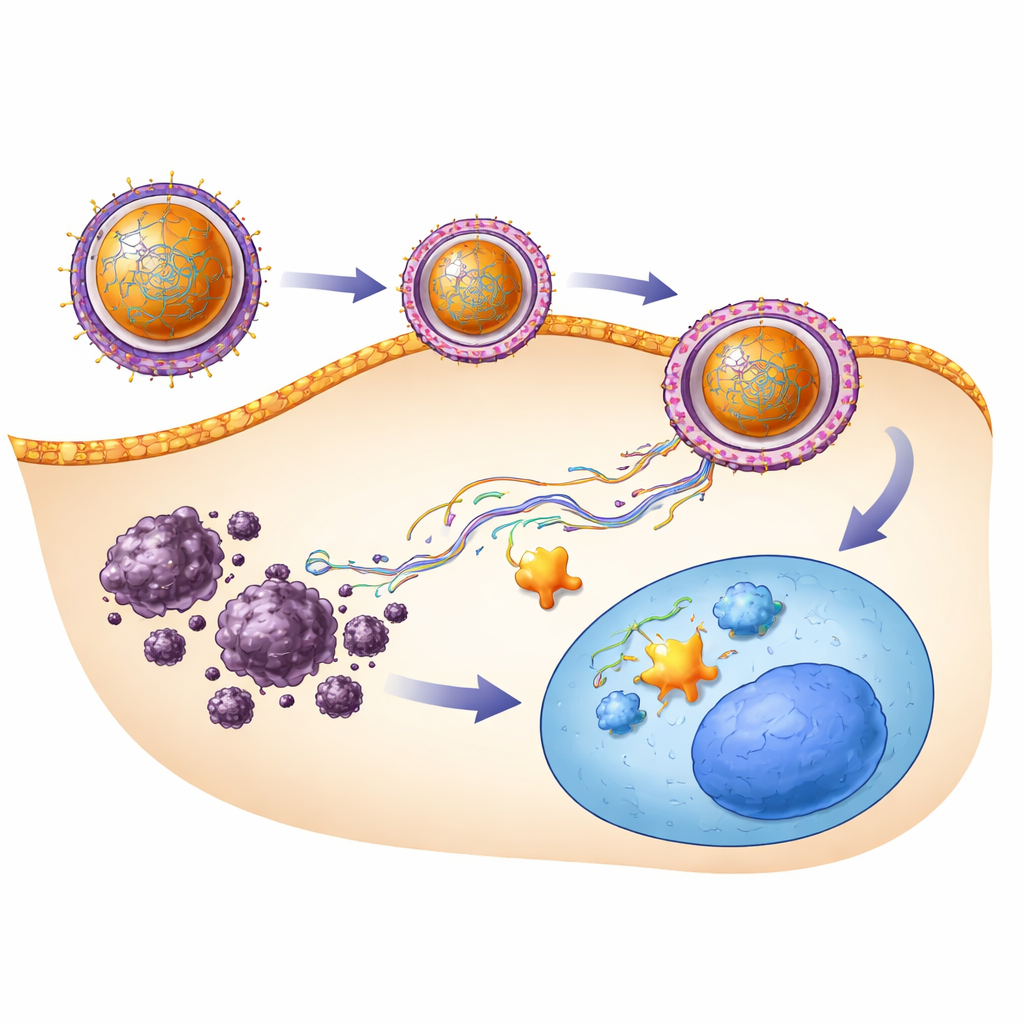
מה משמעות הדבר לטיפולים עתידיים
באופן פשוט, מחקר זה מראה ששחזור מולקולת "המעצור" החסרה בתאי הכבד, והגנה עליה באמצעות נשא ננו חכם, יכול להאט או להפוך את סרטן הכבד בעכברים ללא נזק ברור. קומפלקס ה‑SRHC–ננו לא רק הוריד סמני גידול ואותות גדילה מסוכנים אלא גם סייע לשקם את ארכיטקטורת הכבד הנורמלית. עדיין נדרש עבודה רבה לפני שגישה כזו תגיע לחולים—כולל שיפור נתיבי ההעברה, הבטחת בטיחות ארוכת טווח ושילוב עם תרופות קיימות—אך התוצאות מדגישות אסטרטגיה מבטיחה: שימוש בחלקיקים מהונדסים כדי לשנע רגולטורים גנטיים שבירים חזרה למקום שאליו הם שייכים, ולדכא את הסרטן מבפנים.
ציטוט: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
מילות מפתח: סרטן הכבד הראשוני, טיפול בננו-חלקיקים, RNA לא מקודד ארוך, טיפולי סרטן כבד, העברה ממוקדת של תרופות