Clear Sky Science · zh
TLR7/8 信号在新生儿单核细胞中平衡细胞因子反应
为什么新生儿免疫很重要
新生儿面临一种完美风暴:他们与病原体的首次接触恰逢免疫系统仍在学习规则之时。本研究提出了一个对父母和临床医生都至关重要的问题——为什么新生儿对医院获得性感染如此脆弱,病毒引发的早期免疫信号是否会改变婴儿应对大肠杆菌等危险细菌的方式?通过聚焦一种名为单核细胞的白细胞类型,研究者揭示了这些细胞内微小感应装置如何在有效防御与有害、持久性炎症之间倾斜平衡。
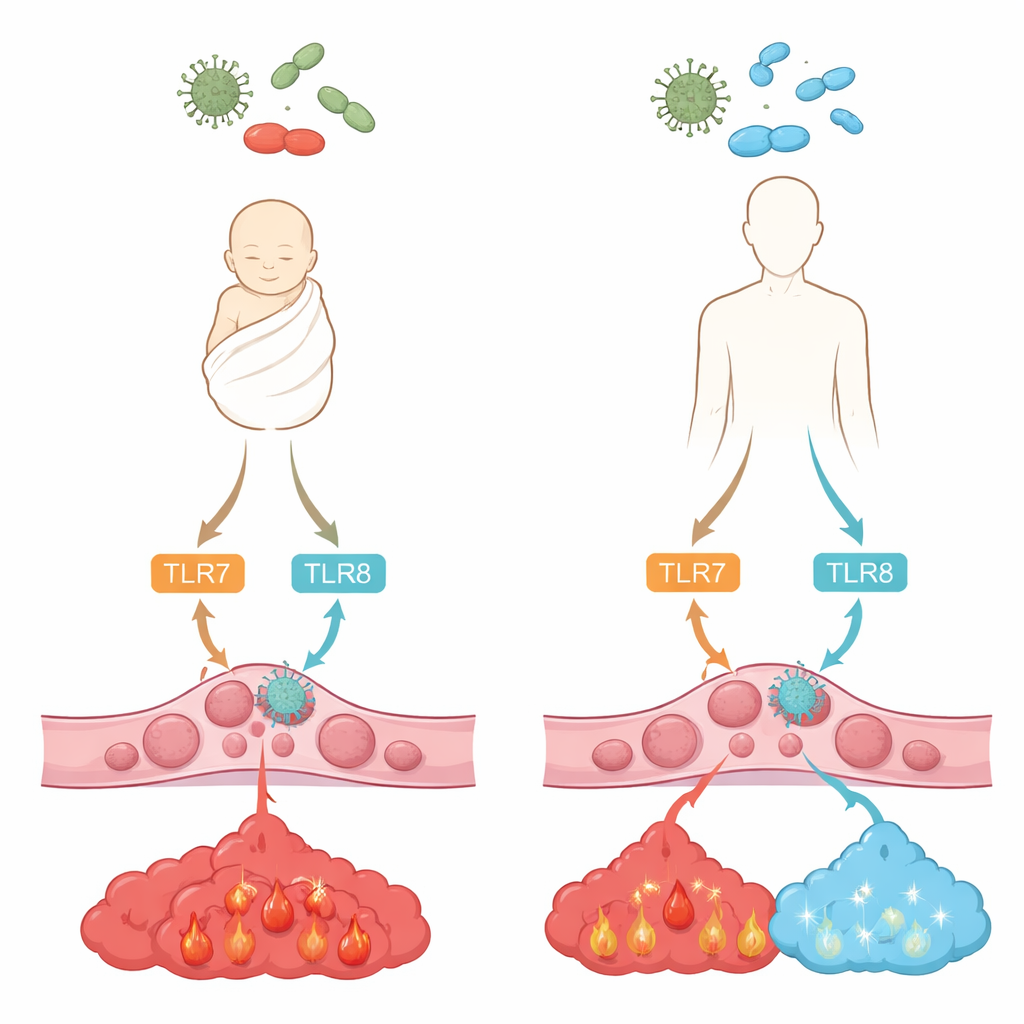
细胞如何感知入侵者
我们的免疫细胞使用被称为 Toll 样受体的分子“警钟”来检测病毒和细菌的片段。其中两种,TLR7 和 TLR8,位于细胞内并识别单链 RNA——这是一种在许多病毒及某些细菌中常见的遗传物质。被激活时,它们会启动内部信号链,导致化学信使(或称细胞因子)的释放,这些因子塑造炎症和抗病毒防御。研究团队比较了来自成人血液和健康新生儿脐带血的单核细胞,考察 TLR7 与 TLR8 的表达水平以及当用两种模拟病毒 RNA 的药物样化合物激活时它们的反应强度。
新生儿与成人细胞的不同接线方式
研究发现,新生儿单核细胞携带的 TLR7 与成人相当,但 TLR8 明显减少。尽管如此,当用测试化合物激活这些受体时,成人与新生儿细胞释放的强炎性信使 TNF-α 与多功能细胞因子 IL-6 水平相当。显著差异出现在 IL-10——一种抑制性信号,有助于在炎症变得有害前将其关闭。成人细胞在 TLR7/8 刺激后产生大量 IL-10,但新生儿细胞几乎不产生,尽管当通过另一条通路激活时它们可以产生 IL-10。这一模式表明新生儿单核细胞倾向于产生强烈炎症反应,但缺乏重要的“刹车踏板”。
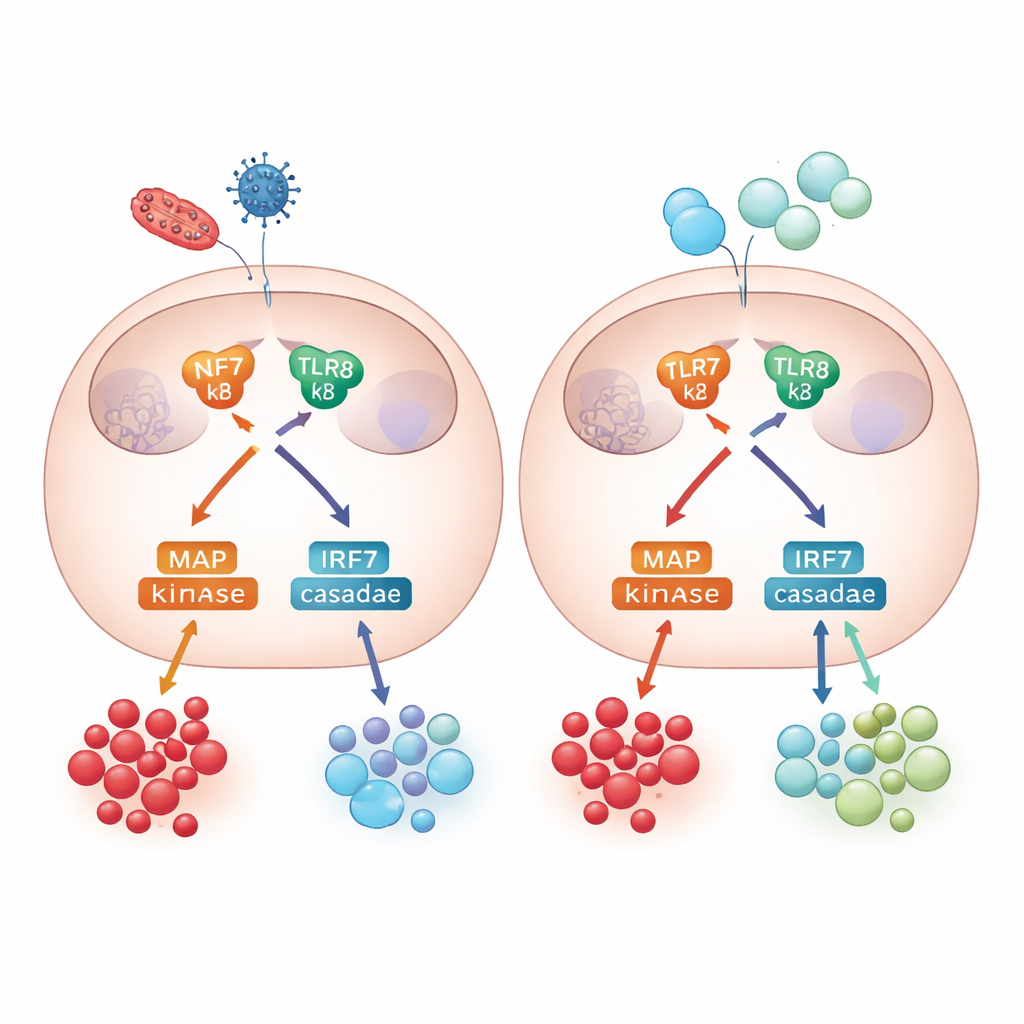
信号控制室内部
为理解这些差异如何产生,团队探查了将 TLR7/8 激活与细胞因子释放连接起来的内部信号机械。成人与新生儿单核细胞都启动了主要信号通路,包括 NF-κB 及一类称为 MAP 激酶的酶群。阻断其中一种激酶 p38 对 TNF-α 和 IL-6 等炎性信号的影响仅为温和,但在成人细胞中显著降低了 IL-10 的产生,凸显了抗炎控制对该通路的依赖性。研究还检查了抗病毒反应:成人与新生儿单核细胞均激活转录因子 IRF7 并产生 I 型干扰素——关键的抗病毒细胞因子,表明尽管新生儿的调控反馈较弱,其抗病毒防御在很大程度上仍然完整。
当病毒预警遇到细菌威胁
由于现实世界中的感染常常按顺序发生——例如先有病毒继而被细菌侵袭——研究者在体外模拟了这一情形。他们先刺激单核细胞的 TLR7/8,然后将细胞暴露于荧光标记的大肠杆菌,以追踪细胞吞噬和杀灭细菌的能力。事先激活 TLR7/8 改变了参与细菌摄取的表面分子水平,并总体上降低了细胞吞噬大肠杆菌的能力,尤其在新生儿单核细胞中更为明显。然而有趣的是,以 TLR7 为主的化合物伊马唑莫德(imiquimod)预处理使新生儿细胞内的大肠杆菌存活率下降,这暗示出尽管它们摄入的细菌更少,但一旦入内可能更有效地将其杀死。在这些共同挑战中细胞因子的释放未显示出强烈的协同效应,但与新生儿相比,成人再次表现出更平衡的炎性与抗炎信号混合。
这对脆弱新生儿意味着什么
综合来看,这项工作描绘了这样一幅图景:新生儿单核细胞能够识别病毒与细菌并发动稳健的炎性与抗病毒反应,但缺乏帮助成人避免过度、持久炎症的 IL-10 “关闭开关”。这种偏斜的平衡可能助长新生儿对严重感染及败血症等并发症的易感性。与此同时,发现针对 TLR7 的化合物可降低新生儿细胞内细菌存活率,提示经过细致调整的药物或许有朝一日能够增强对机会性感染的保护。任何此类方法都需经充分测试,但本研究为理解及潜在改善早期生命免疫防御提供了机制性路线图。
引用: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
关键词: 新生儿免疫, Toll 样受体, 单核细胞, 新生儿败血症, 炎症