Clear Sky Science · pt
Sinalização TLR7/8 equilibra respostas de citocinas em monócitos neonatais
Por que a imunidade dos recém-nascidos importa
Bebês recém-nascidos enfrentam uma tempestade perfeita: seus primeiros encontros com microrganismos ocorrem justamente quando seus sistemas imunológicos ainda estão aprendendo as regras. Este estudo investiga uma questão crucial para pais e médicos — por que os recém-nascidos são tão vulneráveis a infecções hospitalares, e sinais imunes precoces de vírus podem alterar a forma como os bebês lidam com bactérias perigosas como E. coli? Ao focalizar um tipo específico de célula branca do sangue chamada monócito, os pesquisadores revelam como pequenos sensores dentro dessas células podem inclinar o equilíbrio entre uma defesa útil e uma inflamação persistente e prejudicial.
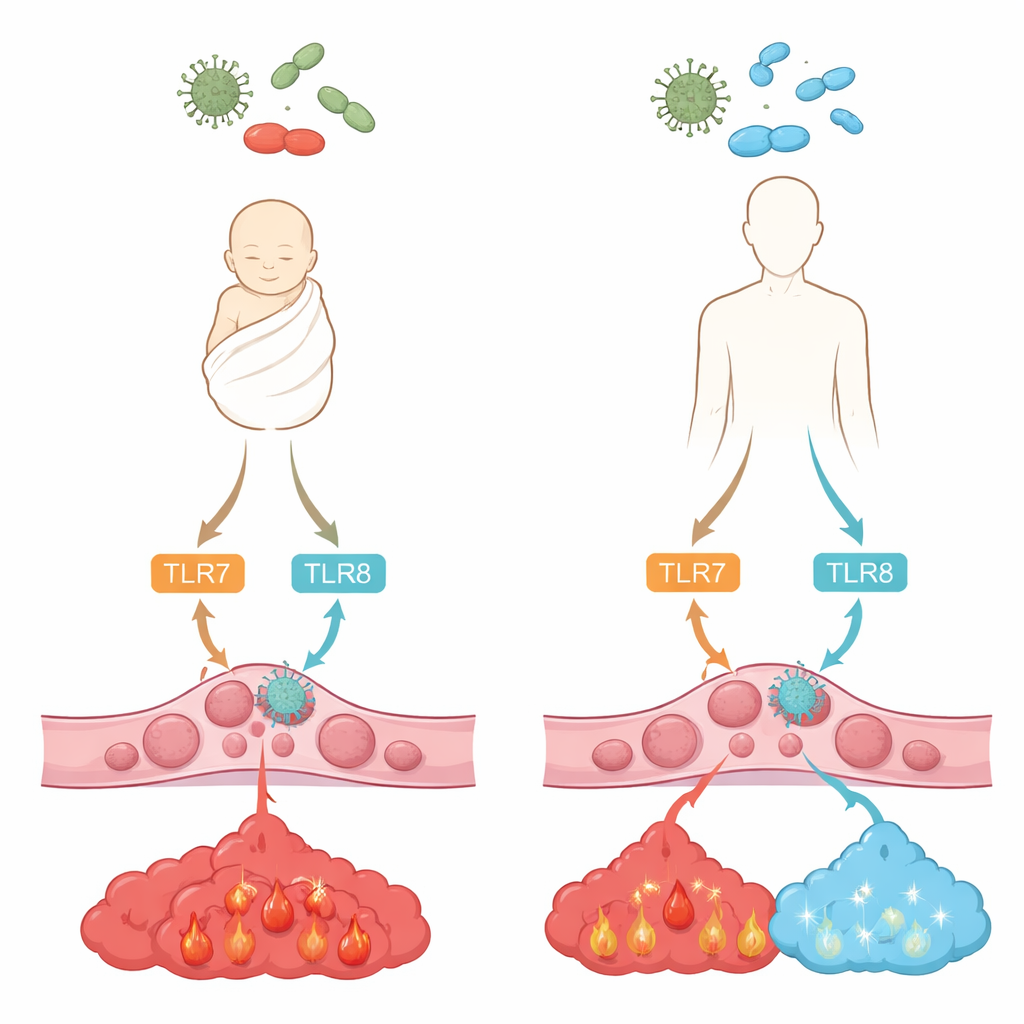
Como as células detectam invasores
Nossas células imunes usam “sinos de alarme” moleculares conhecidos como receptores Toll-like para detectar fragmentos de vírus e bactérias. Dois deles, chamados TLR7 e TLR8, ficam dentro das células e reconhecem RNA de fita simples, um material genético comum em muitos vírus e em algumas bactérias. Quando ativados, desencadeiam cadeias de sinal internas que levam à liberação de mensageiros químicos, ou citocinas, que moldam a inflamação e a defesa antiviral. A equipe comparou monócitos de sangue adulto com aqueles do sangue do cordão umbilical de recém-nascidos saudáveis, investigando quão presentes estão TLR7 e TLR8 e como respondem quando ativados por dois compostos semelhantes a drogas que mimetizam RNA viral.
Diferenças na fiação entre células neonatais e adultas
Os pesquisadores descobriram que monócitos neonatais têm quantidades semelhantes de TLR7 em comparação com adultos, mas notavelmente menos TLR8. Apesar disso, quando esses receptores foram ativados com os compostos de teste, tanto células adultas quanto neonatais liberaram níveis comparáveis da potente citocina inflamatória TNF-alfa e da versátil IL-6. A grande diferença apareceu na IL-10, um sinal calmante que ajuda a encerrar a inflamação antes que ela se torne danosa. Células adultas produziram bastante IL-10 após estimulação de TLR7/8, mas células neonatais produziram quase nada, embora fossem capazes de gerar IL-10 quando outra via era acionada. Esse padrão sugere que os monócitos neonatais estão programados para montar uma inflamação robusta, mas carecem de um importante “freio”.
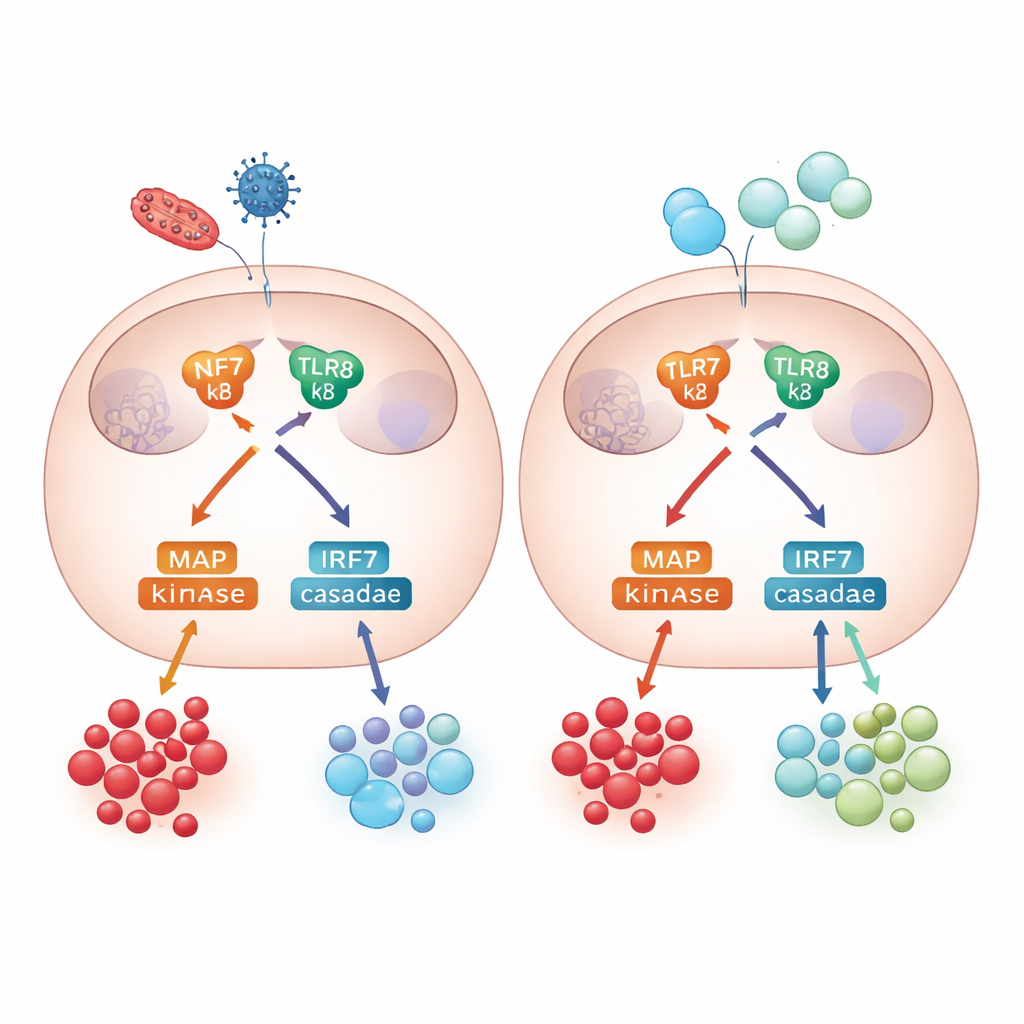
Dentro da sala de controle da sinalização
Para entender como surgem essas diferenças, a equipe investigou a maquinaria de sinalização interna que liga a ativação de TLR7/8 à liberação de citocinas. Tanto monócitos adultos quanto neonatais engajaram rotas de sinal importantes, incluindo NF-κB e um grupo de enzimas chamadas MAP quinases. Bloquear uma dessas enzimas, p38, teve apenas efeitos modestos em sinais inflamatórios como TNF-alfa e IL-6, mas reduziu fortemente a produção de IL-10 em células adultas, ressaltando que o controle anti-inflamatório depende dessa via. O estudo também examinou respostas antivirais: tanto monócitos adultos quanto neonatais ativaram o fator de transcrição IRF7 e produziram interferons do tipo I, citocinas antivirais-chave, mostrando que as defesas antivirais estavam amplamente preservadas nos recém-nascidos, apesar de seu feedback regulatório ser mais fraco.
Quando um alerta viral encontra uma ameaça bacteriana
Como infecções no mundo real frequentemente ocorrem em sequência — por exemplo, um vírus seguido por um invasor bacteriano — os pesquisadores imitaram esse cenário no laboratório. Primeiro estimularam TLR7/8 em monócitos e depois expuseram as células a E. coli fluorescente para rastrear quão bem englobavam e matavam as bactérias. A ativação prévia de TLR7/8 alterou os níveis de moléculas de superfície envolvidas na captura bacteriana e, em geral, reduziu a capacidade das células de engolir E. coli, especialmente em monócitos neonatais. Ainda assim, intrigantemente, o pré-tratamento com o composto focado em TLR7, imiquimode, levou à redução da sobrevivência de E. coli em células neonatais, sugerindo que, embora elas internalizem menos bactérias, podem matá-las mais eficazmente uma vez dentro. A liberação de citocinas durante esses desafios combinados não mostrou forte sinergia, mas os adultos novamente exibiram uma mistura mais equilibrada de sinais inflamatórios e anti-inflamatórios em comparação com os recém-nascidos.
O que isso significa para recém-nascidos frágeis
Em conjunto, o trabalho desenha o retrato de monócitos neonatais capazes de reconhecer vírus e bactérias e montar respostas inflamatórias e antivirais sólidas, mas que carecem do “interruptor de desligar” IL-10 que ajuda adultos a evitar inflamação excessiva e persistente. Esse desequilíbrio pode contribuir para a suscetibilidade dos recém-nascidos a infecções graves e complicações como sepse. Ao mesmo tempo, a descoberta de que um composto direcionado a TLR7 pode diminuir a sobrevivência bacteriana em células neonatais sugere que drogas cuidadosamente ajustadas podem, no futuro, aumentar a proteção contra infecções oportunistas. Qualquer abordagem desse tipo exigiria testes rigorosos, mas este estudo oferece um roteiro mecanístico para entender — e potencialmente melhorar — as defesas imunológicas nos primeiros dias de vida.
Citação: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
Palavras-chave: imunidade neonatal, receptores Toll-like, monócitos, sepse neonatal, inflamação