Clear Sky Science · fr
La signalisation TLR7/8 équilibre les réponses en cytokines dans les monocytes néonatals
Pourquoi l’immunité du nouveau-né importe
Les nouveau-nés affrontent une tempête parfaite : leurs premières rencontres avec des agents infectieux surviennent alors que leur système immunitaire est encore en pleine maturation. Cette étude pose une question cruciale pour les parents et les cliniciens : pourquoi les nouveau-nés sont-ils si vulnérables aux infections nosocomiales, et les signaux immunitaires précoces d’origine virale peuvent-ils modifier la manière dont les nourrissons gèrent des bactéries dangereuses comme E. coli ? En se concentrant sur un type précis de globule blanc, le monocyte, les chercheurs montrent comment de petits détecteurs intracellulaires peuvent faire pencher la balance entre une défense utile et une inflammation prolongée et nuisible.
Comment les cellules détectent les agents envahisseurs
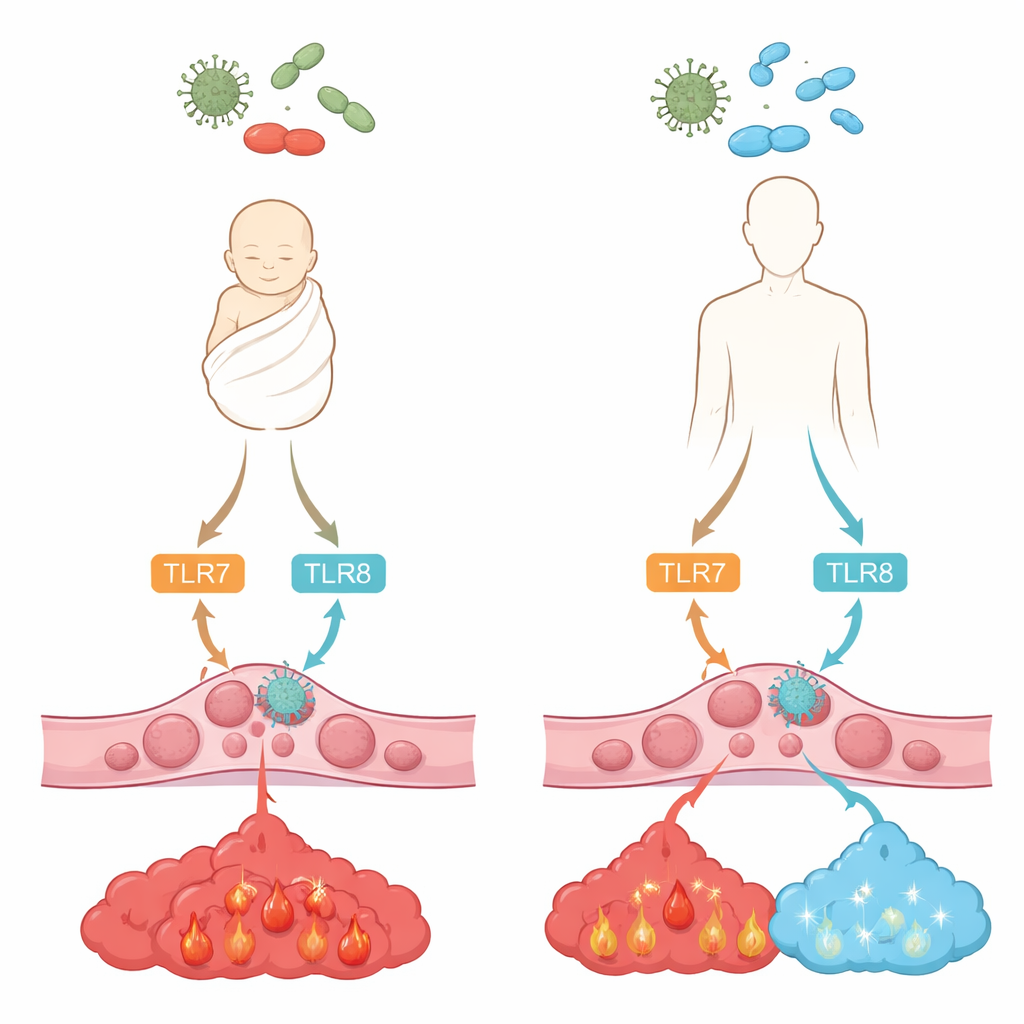
Nos cellules immunitaires utilisent des « sonnettes d’alarme » moléculaires connues sous le nom de récepteurs Toll-like pour repérer des fragments de virus et de bactéries. Deux d’entre eux, TLR7 et TLR8, se trouvent à l’intérieur des cellules et reconnaissent l’ARN simple brin, un matériel génétique courant chez de nombreux virus et présent chez certaines bactéries. Lorsqu’ils sont activés, ils déclenchent des cascades de signalisation internes qui conduisent à la libération de messagers chimiques, ou cytokines, qui façonnent l’inflammation et la défense antivirale. L’équipe a comparé des monocytes prélevés dans du sang adulte et du sang de cordon sain de nouveau-nés, cherchant à savoir dans quelle mesure TLR7 et TLR8 sont exprimés et comment ils répondent lorsqu’on les active par deux composés de type médicament imitant l’ARN viral.
Une architecture différente dans les cellules néonatales et adultes
Les chercheurs ont observé que les monocytes néonatals contiennent des quantités de TLR7 similaires à celles des adultes mais nettement moins de TLR8. Malgré cela, lorsque ces récepteurs ont été activés par les composés testés, les cellules adultes et néonatales ont libéré des niveaux comparables du puissant médiateur inflammatoire TNF-alpha et de la cytokine polyvalente IL-6. La grande différence concernait l’IL-10, un signal apaisant qui aide à arrêter l’inflammation avant qu’elle ne devienne dommageable. Les cellules adultes produisaient abondamment de l’IL-10 après stimulation TLR7/8, alors que les cellules néonatales en produisaient presque pas, bien qu’elles puissent fabriquer de l’IL-10 lorsqu’une autre voie était engagée. Ce schéma suggère que les monocytes néonatals sont câblés pour déclencher une inflammation robuste mais leur manque une importante « pédale de frein ».
À l’intérieur de la salle de contrôle de la signalisation
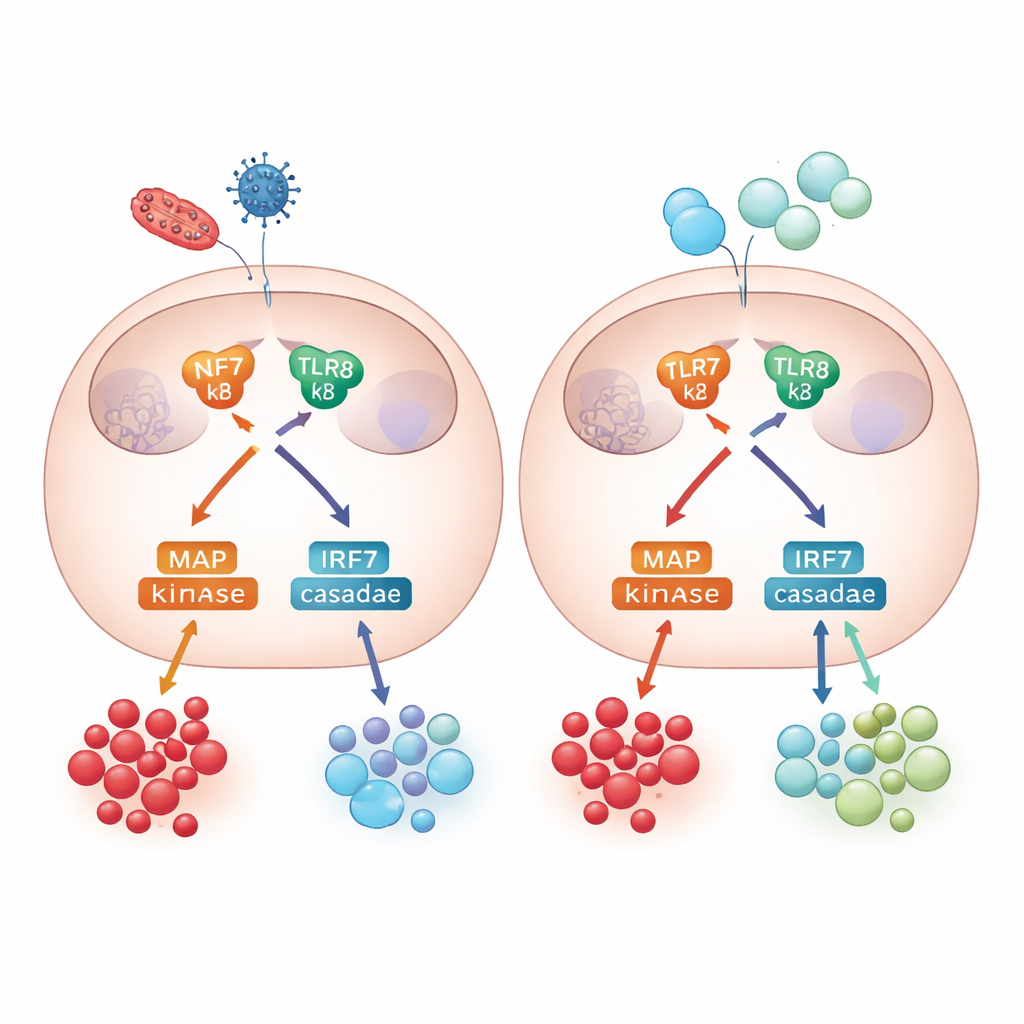
Pour comprendre comment ces différences apparaissent, l’équipe a exploré la machinerie de signalisation interne qui relie l’activation de TLR7/8 à la libération de cytokines. Les monocytes adultes et néonatals mobilisaient des voies signalétiques majeures, y compris NF-κB et un groupe d’enzymes appelées MAP kinases. Le blocage d’une de ces enzymes, p38, n’a eu que des effets modestes sur des signaux inflammatoires comme le TNF-alpha et l’IL-6 mais a fortement réduit la production d’IL-10 dans les cellules adultes, soulignant que le contrôle anti-inflammatoire dépend de cette voie. L’étude a aussi examiné les réponses antivirales : les monocytes adultes et néonatals activaient le facteur de transcription IRF7 et produisaient des interférons de type I, cytokines antivirales clés, montrant que les défenses antivirales étaient en grande partie préservées chez les nouveau-nés malgré un retour régulateur affaibli.
Quand un avertissement viral rencontre une menace bactérienne
Parce que les infections dans le monde réel surviennent souvent en séquence — par exemple un virus suivi d’un envahisseur bactérien — les chercheurs ont reproduit ce scénario en laboratoire. Ils ont d’abord stimulé TLR7/8 des monocytes, puis exposé les cellules à des E. coli fluorescents pour suivre leur capacité à engloutir et tuer les bactéries. L’activation préalable de TLR7/8 a modifié les niveaux de molécules de surface impliquées dans la capture bactérienne et a généralement réduit la capacité des cellules à ingérer E. coli, en particulier dans les monocytes néonatals. Pourtant, de manière intrigante, le prétraitement avec le composé centré sur TLR7, l’imquimod, a entraîné une survie réduite d’E. coli dans les cellules néonatales, suggérant que même si elles internalisent moins de bactéries, elles pourraient les tuer plus efficacement une fois à l’intérieur. La libération de cytokines lors de ces co-défis n’a pas montré de forte synergie, mais les adultes présentaient à nouveau un mélange plus équilibré de signaux inflammatoires et anti-inflammatoires comparé aux nouveau-nés.
Ce que cela signifie pour les nouveau-nés fragiles
Pris ensemble, les résultats dressent le portrait de monocytes néonatals capables de reconnaître virus et bactéries et de monter des réponses inflammatoires et antivirales solides, mais qui sont dépourvus de l’interrupteur IL-10 qui aide les adultes à éviter une inflammation excessive et persistante. Ce déséquilibre pourrait contribuer à la vulnérabilité des nouveau-nés aux infections sévères et aux complications telles que la septicémie. Dans le même temps, la découverte qu’un composé ciblant TLR7 peut diminuer la survie bactérienne dans les cellules néonatales suggère que des médicaments finement ajustés pourraient un jour renforcer la protection contre les infections opportunistes. Toute approche de ce type exigerait des tests approfondis, mais cette étude fournit une feuille de route mécanistique pour comprendre — et potentiellement améliorer — les défenses immunitaires en début de vie.
Citation: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
Mots-clés: immunité du nouveau-né, récepteurs Toll-like, monocytes, septicémie néonatale, inflammation