Clear Sky Science · es
La señalización TLR7/8 equilibra las respuestas de citoquinas en monocitos neonatales
Por qué importa la inmunidad del recién nacido
Los recién nacidos enfrentan una tormenta perfecta: sus primeros encuentros con microbios se producen justo cuando sus sistemas inmunitarios aún están aprendiendo las reglas. Este estudio plantea una pregunta crucial para padres y médicos: ¿por qué los recién nacidos son tan vulnerables a las infecciones nosocomiales, y pueden las señales inmunitarias tempranas de virus cambiar la forma en que los bebés manejan bacterias peligrosas como E. coli? Al centrarse en un tipo específico de glóbulo blanco llamado monocito, los investigadores revelan cómo pequeños sensores dentro de estas células pueden inclinar la balanza entre una defensa útil y una inflamación dañina y persistente.
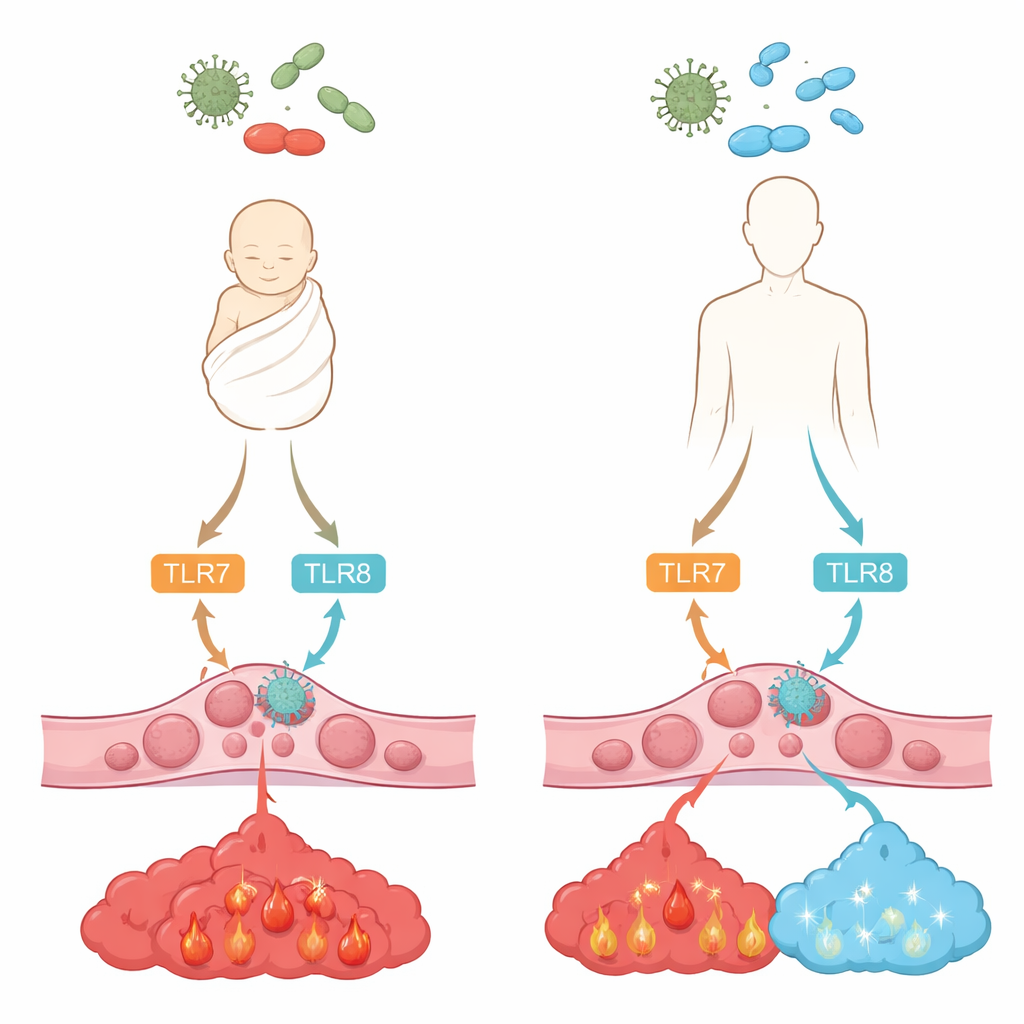
Cómo las células detectan microbios invasores
Nuestras células inmunitarias usan “campanas de alarma” moleculares conocidas como receptores tipo Toll para detectar fragmentos de virus y bacterias. Dos de estos, llamados TLR7 y TLR8, se sitúan dentro de las células y reconocen ARN monocatenario, un material genético común en muchos virus y en algunas bacterias. Cuando se activan, desencadenan cadenas de señales internas que conducen a la liberación de mensajeros químicos, o citoquinas, que moldean la inflamación y la defensa antiviral. El equipo comparó monocitos de sangre de adultos con los de sangre del cordón umbilical de recién nacidos sanos, preguntando cuán abundantes son TLR7 y TLR8 y cómo responden cuando se activan con dos compuestos tipo fármaco que imitan el ARN viral.
Conexión diferente en células de recién nacidos y adultos
Los investigadores hallaron que los monocitos neonatales poseen cantidades similares de TLR7 que los adultos, pero notablemente menos TLR8. A pesar de ello, al activar estos receptores con los compuestos de prueba, tanto las células adultas como las neonatales liberaron niveles comparables de la potente citoquina inflamatoria TNF-alfa y de la citoquina versátil IL-6. La gran diferencia apareció en IL-10, una señal calmante que ayuda a apagar la inflamación antes de que cause daño. Las células adultas produjeron abundante IL-10 tras la estimulación TLR7/8, pero las células neonatales prácticamente no la produjeron, aun cuando podían fabricar IL-10 al activarse por otra vía. Este patrón sugiere que los monocitos neonatales están programados para montar una inflamación robusta pero carecen de un importante “pedal de freno”.
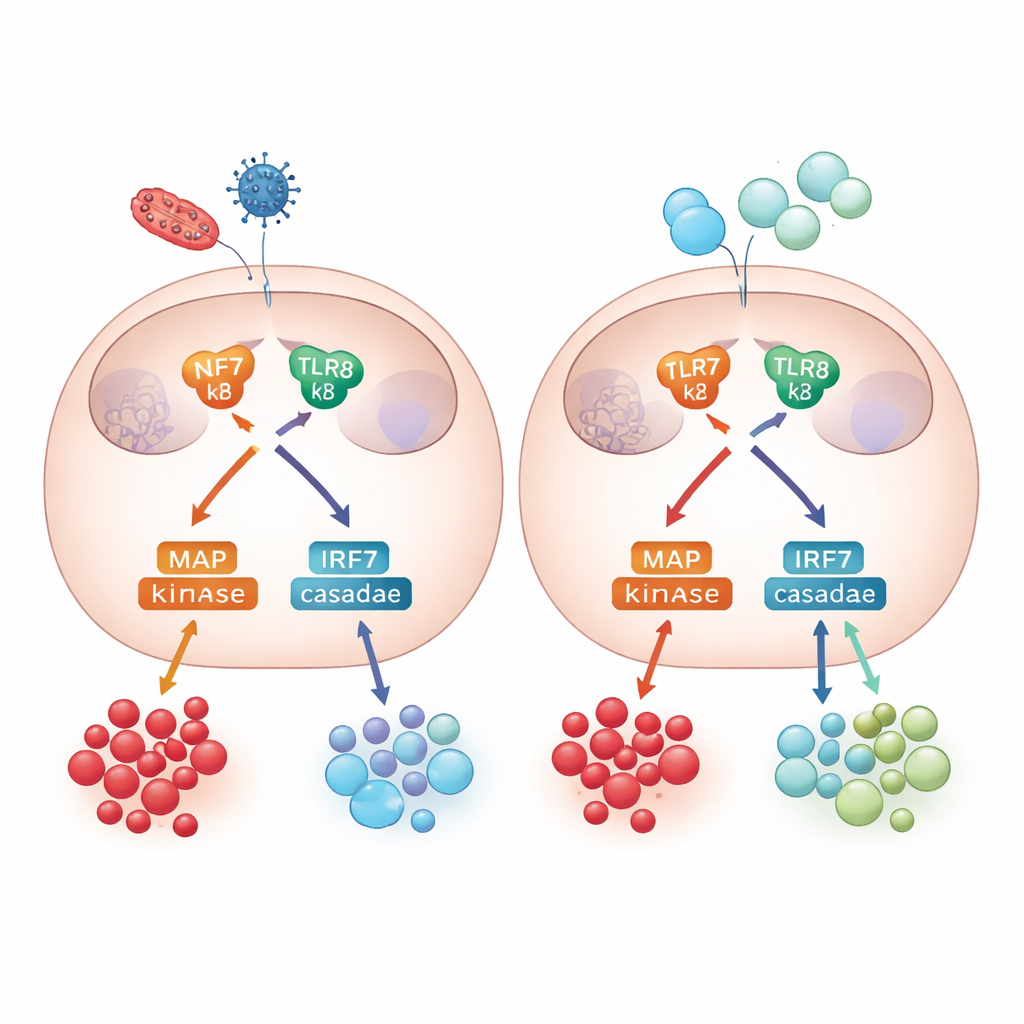
Dentro de la sala de control de la señalización
Para entender cómo surgen estas diferencias, el equipo examinó la maquinaria interna de señalización que enlaza la activación de TLR7/8 con la liberación de citoquinas. Tanto los monocitos adultos como los neonatales activaron vías de señalización principales, incluida NF-κB y un grupo de enzimas llamadas quinasas MAP. Bloquear una de estas enzimas, p38, tuvo solo efectos modestos sobre señales inflamatorias como TNF-alfa e IL-6, pero redujo con fuerza la producción de IL-10 en células adultas, subrayando que el control antiinflamatorio depende de esta vía. El estudio también examinó las respuestas antivirales: tanto monocitos adultos como neonatales activaron el factor de transcripción IRF7 y produjeron interferones tipo I, citoquinas antivirales clave, lo que muestra que las defensas antivirales estaban en gran medida intactas en los recién nacidos a pesar de que su retroalimentación reguladora era más débil.
Cuando una advertencia viral se encuentra con una amenaza bacteriana
Puesto que las infecciones reales suelen ocurrir en secuencia —por ejemplo, un virus seguido de un invasor bacteriano— los investigadores imitaron este escenario en el laboratorio. Primero estimularon TLR7/8 en monocitos y luego expusieron las células a E. coli fluorescente para seguir cómo absorbían y mataban las bacterias. La activación previa de TLR7/8 cambió los niveles de moléculas de superficie implicadas en la captación bacteriana y, en general, redujo la capacidad de las células para engullir E. coli, especialmente en los monocitos neonatales. Sin embargo, de manera intrigante, el pretratamiento con el compuesto centrado en TLR7 imiquimod condujo a una menor supervivencia de E. coli en células neonatales, lo que sugiere que, aunque internalizan menos bacterias, pueden matarlas más eficazmente una vez dentro. La liberación de citoquinas durante estos co-desafíos no mostró una fuerte sinergia, pero los adultos volvieron a mostrar una mezcla más equilibrada de señales proinflamatorias y antiinflamatorias en comparación con los neonatos.
Qué significa esto para los frágiles recién nacidos
En conjunto, el trabajo dibuja la imagen de monocitos neonatales capaces de reconocer virus y bacterias y de montar respuestas inflamatorias y antivirales sólidas, pero que carecen del “interruptor de apagado” IL-10 que ayuda a los adultos a evitar una inflamación excesiva y persistente. Este desequilibrio podría contribuir a la vulnerabilidad de los recién nacidos a infecciones severas y complicaciones como la sepsis. Al mismo tiempo, el hallazgo de que un compuesto que apunta a TLR7 puede disminuir la supervivencia bacteriana en células neonatales sugiere que fármacos afinados con cuidado podrían algún día mejorar la protección frente a infecciones oportunistas. Cualquier enfoque de este tipo requeriría pruebas exhaustivas, pero este estudio ofrece una hoja de ruta mecanística para comprender y, potencialmente, mejorar las defensas inmunitarias en la primera etapa de la vida.
Cita: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
Palabras clave: inmunidad neonatal, receptores tipo Toll, monocitos, sepsis neonatal, inflamación