Clear Sky Science · pl
Sygnalizacja TLR7/8 równoważy odpowiedzi cytokinowe w monocytach noworodków
Dlaczego odporność noworodków ma znaczenie
Noworodki stoją przed idealną burzą: ich pierwsze zetknięcia z drobnoustrojami przypadają na czas, gdy układ odpornościowy dopiero uczy się zasad. To badanie stawia kluczowe pytanie dla rodziców i lekarzy — dlaczego noworodki są tak podatne na zakażenia szpitalne i czy wczesne sygnały immunologiczne wywołane przez wirusy mogą zmienić sposób, w jaki niemowlęta radzą sobie z groźnymi bakteriami, takimi jak E. coli? Skupiając się na specyficznym typie białych krwinek zwanych monocytami, badacze pokazują, jak drobne czujniki w tych komórkach mogą przechylić równowagę między pożyteczną obroną a szkodliwym, utrzymującym się zapaleniem.
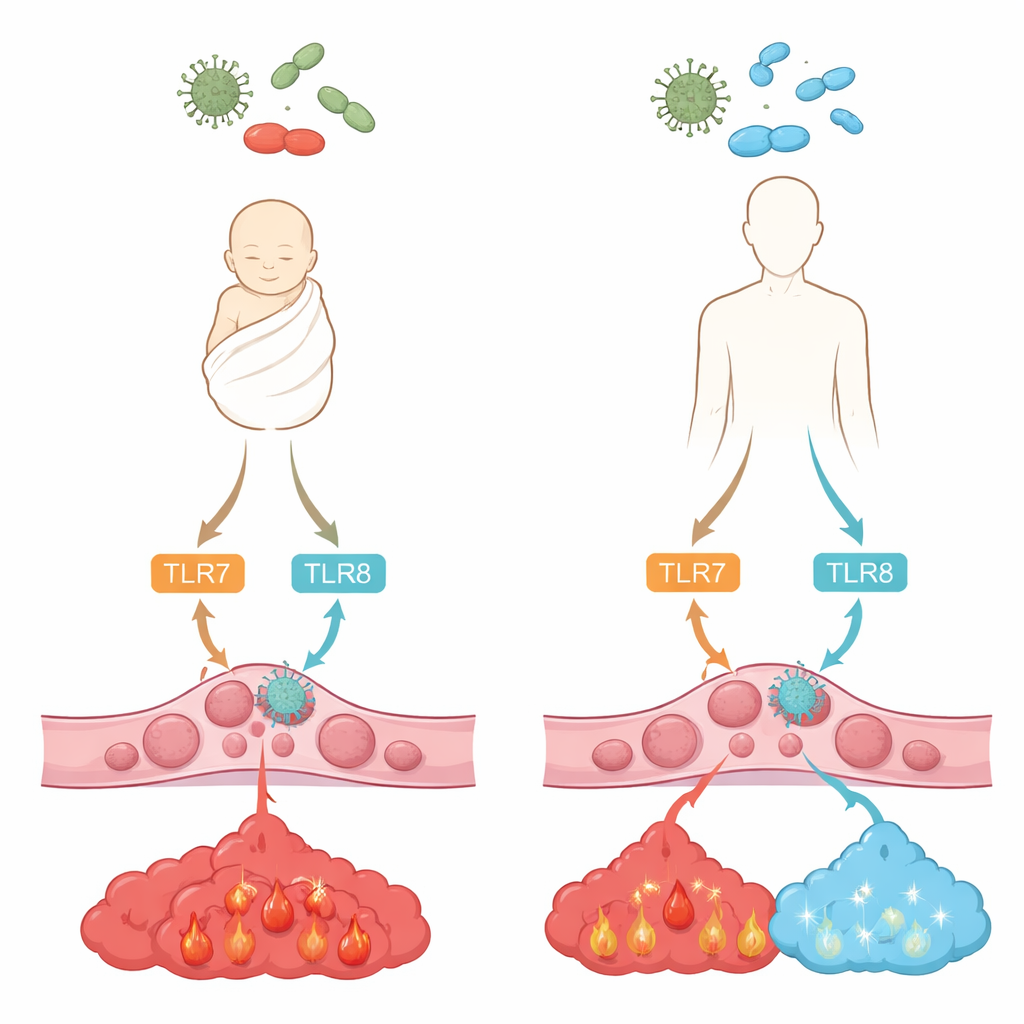
Jak komórki wyczuwają najeźdźców
Nasze komórki odpornościowe korzystają z molekularnych „dzwonków alarmowych” znanych jako receptory Toll-podobne, aby wykrywać fragmenty wirusów i bakterii. Dwa z nich, TLR7 i TLR8, znajdują się wewnątrz komórek i rozpoznają jednoniciowe RNA — materiał genetyczny występujący w wielu wirusach i niektórych bakteriach. Po uruchomieniu uruchamiają wewnętrzne kaskady sygnałowe prowadzące do wydzielania przekaźników chemicznych, czyli cytokin, które kształtują zapalenie i obronę przeciwwirusową. Zespół porównał monocyty z krwi dorosłych i z krwi pępowinowej zdrowych noworodków, badając, jak obficie występują TLR7 i TLR8 i jak reagują po aktywacji dwoma związkami przypominającymi wirusowe RNA.
Inne okablowanie w komórkach noworodków i dorosłych
Badacze stwierdzili, że monocyty noworodków zawierają podobne ilości TLR7 jak u dorosłych, ale zauważalnie mniej TLR8. Mimo to, po uaktywnieniu tych receptorów testowanymi związkami zarówno komórki dorosłych, jak i noworodków wydzielały porównywalne poziomy silnego mediatora zapalenia TNF-alfa oraz wszechstronnej cytokiny IL-6. Duża różnica pojawiła się w przypadku IL-10, sygnału kojącego, który pomaga wygasić zapalenie zanim stanie się szkodliwe. Komórki dorosłych produkowały dużo IL-10 po stymulacji TLR7/8, podczas gdy komórki noworodków wytwarzały niemal żadnego, mimo że mogły produkować IL-10 po aktywacji innej drogi. Ten wzorzec sugeruje, że monocyty noworodków są zaprogramowane do silnej odpowiedzi zapalnej, ale brakuje im ważnego „hamulca”.
W środku sterowni sygnałowej
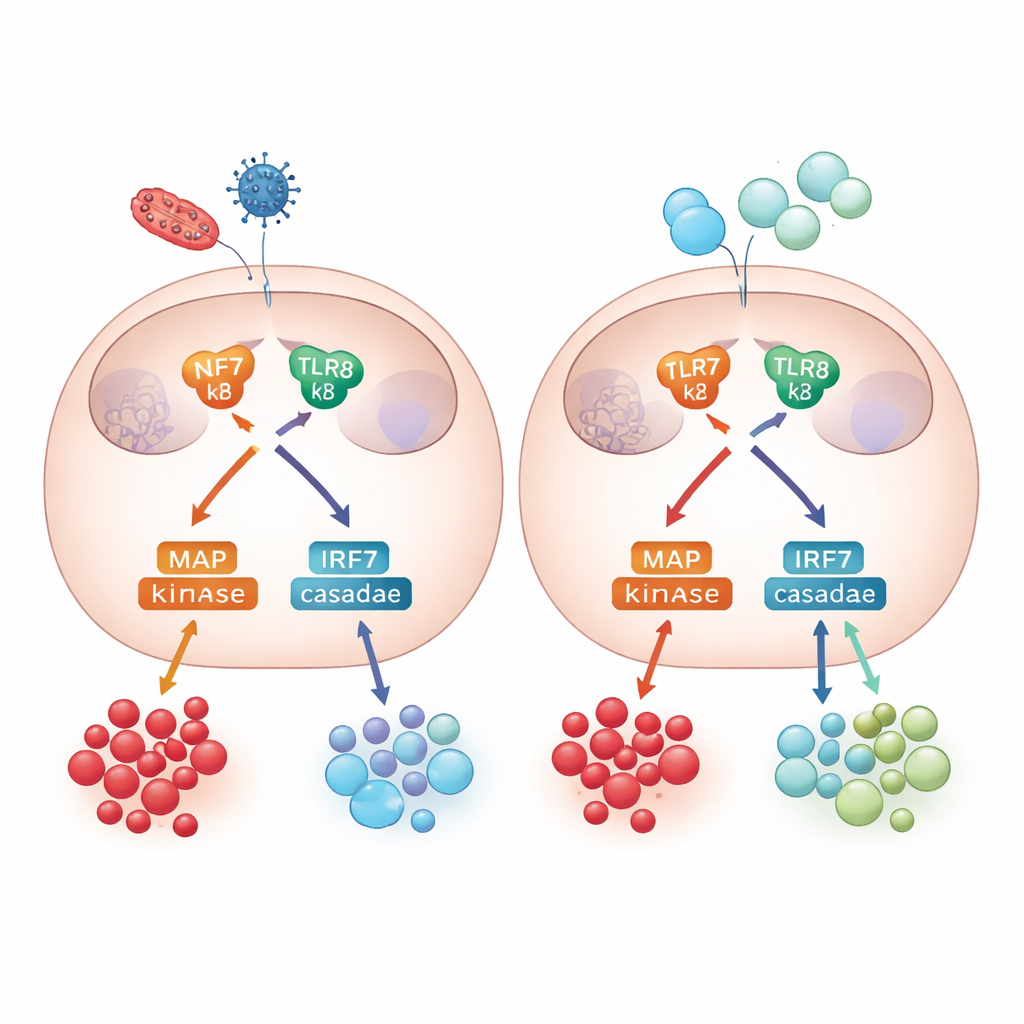
Aby zrozumieć, skąd biorą się te różnice, zespół zbadał wewnętrzne mechanizmy sygnalizacyjne łączące aktywację TLR7/8 z wydzielaniem cytokin. Zarówno monocyty dorosłych, jak i noworodków uruchamiały główne szlaki sygnałowe, w tym NF-κB oraz grupę enzymów zwanych kinazami MAP. Zablokowanie jednej z tych kinaz, p38, miało jedynie umiarkowany wpływ na sygnały zapalne takie jak TNF-alfa i IL-6, ale silnie zmniejszyło produkcję IL-10 w komórkach dorosłych, podkreślając, że kontrola przeciwzapalna zależy od tego szlaku. Badanie objęło także odpowiedzi przeciwwirusowe: zarówno monocyty dorosłych, jak i noworodków aktywowały czynnik transkrypcyjny IRF7 i produkowały interferony typu I — kluczowe cytokiny przeciwwirusowe — co pokazuje, że obrona przeciwwirusowa u noworodków jest w dużej mierze zachowana, mimo słabszego sprzężenia zwrotnego regulującego.
Gdy wirusowe ostrzeżenie spotyka bakteryjne zagrożenie
Ponieważ rzeczywiste zakażenia często pojawiają się sekwencyjnie — na przykład wirus, a potem bakteria — badacze odtworzyli taki scenariusz w laboratorium. Najpierw stymulowali TLR7/8 w monocytach, potem eksponowali komórki na fluorescencyjne E. coli, by śledzić, jak dobrze komórki pochłaniają i zabijają bakterie. Wcześniejsza aktywacja TLR7/8 zmieniała poziomy cząsteczek powierzchniowych zaangażowanych w pobieranie bakterii i ogólnie zmniejszała zdolność komórek do „jedzenia” E. coli, szczególnie w monocytach noworodków. Jednak intrygująco, wstępne traktowanie związkiem ukierunkowanym na TLR7 — imikwimodem — prowadziło do zmniejszenia przeżywalności E. coli w komórkach noworodków, co sugeruje, że choć pobierają mniej bakterii, mogą je skuteczniej zabijać po wniesieniu. Wydzielanie cytokin podczas takich współzakażeń nie wykazywało silnej synergii, ale po raz kolejny dorośli ujawniali bardziej zrównoważony miks sygnałów zapalnych i przeciwzapalnych w porównaniu z noworodkami.
Co to oznacza dla wrażliwych noworodków
Podsumowując, praca ukazuje obraz monocytów noworodków, które potrafią rozpoznawać wirusy i bakterie oraz wytwarzać solidne odpowiedzi zapalne i przeciwwirusowe, ale którym brakuje „wyłącznika” IL-10, pomagającego dorosłym unikać nadmiernego, utrzymującego się zapalenia. Ta zachwiana równowaga może przyczyniać się do podatności noworodków na ciężkie zakażenia i powikłania, takie jak sepsa. Równocześnie odkrycie, że związek celujący w TLR7 może zmniejszać przeżywalność bakterii w komórkach noworodków, sugeruje, że precyzyjnie dobrane leki mogą kiedyś wzmocnić ochronę przed oportunistycznymi zakażeniami. Każde takie podejście wymagałoby gruntownych badań, ale to badanie dostarcza mechanistycznej mapy do zrozumienia — i potencjalnego poprawienia — wczesnożyciowej odporności.
Cytowanie: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
Słowa kluczowe: odporność noworodków, receptory Toll-podobne, monocyty, sepsa noworodkowa, zapalanie