Clear Sky Science · it
La segnalazione TLR7/8 equilibra le risposte di citochine nei monociti neonatali
Perché conta l’immunità del neonato
I neonati affrontano una tempesta perfetta: i loro primi incontri con i germi avvengono proprio mentre il sistema immunitario sta ancora imparando le regole. Questo studio pone una domanda cruciale per genitori e medici: perché i neonati sono così vulnerabili alle infezioni nosocomiali e i primi segnali immunitari indotti dai virus possono modificare il modo in cui i bambini fronteggiano batteri pericolosi come E. coli? Focalizzandosi su un tipo specifico di globulo bianco chiamato monocita, i ricercatori rivelano come piccoli sensori all’interno di queste cellule possano spostare l’equilibrio tra una difesa utile e un’infiammazione dannosa e persistente.
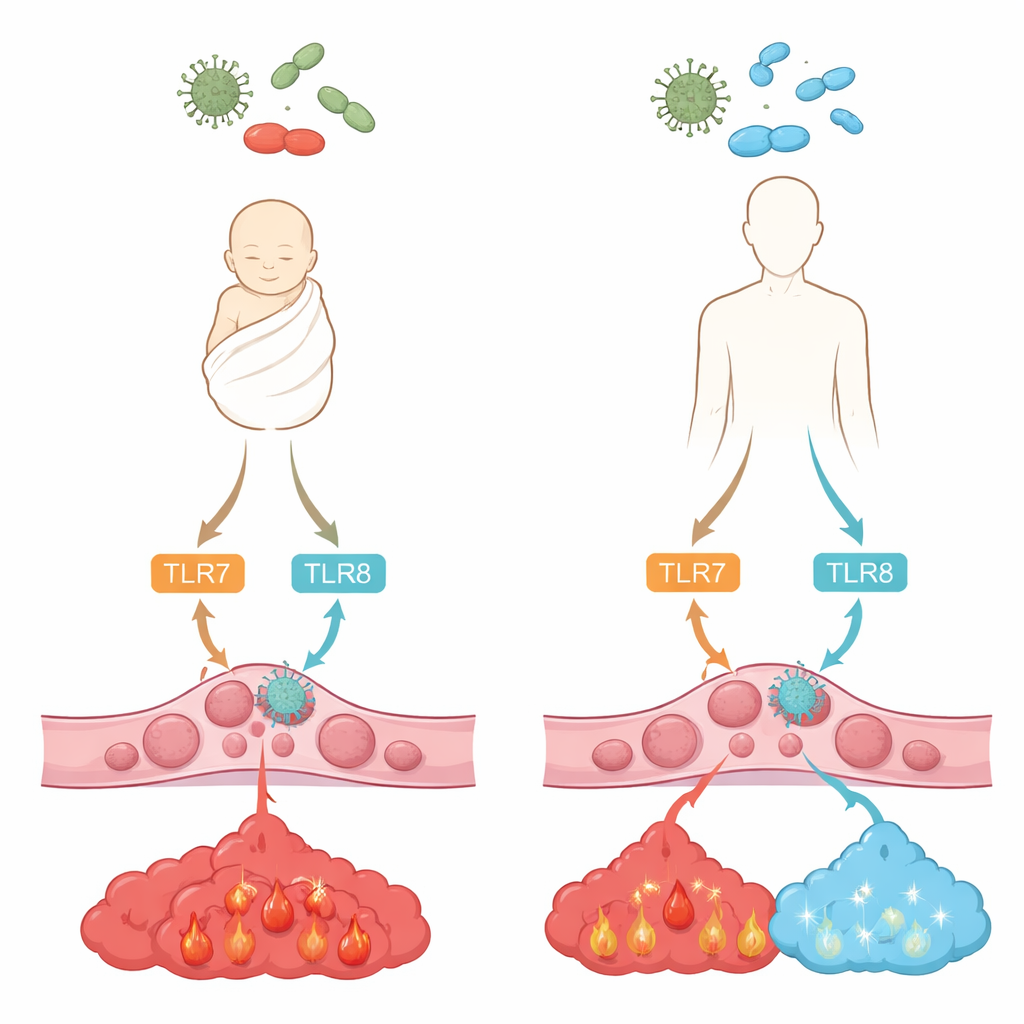
Come le cellule percepiscono i germi invasori
Le nostre cellule immunitarie usano «campanelli di allarme» molecolari noti come recettori Toll-like per rilevare frammenti di virus e batteri. Due di questi, chiamati TLR7 e TLR8, si trovano all’interno delle cellule e riconoscono l’RNA a singolo filamento, un materiale genetico comune in molti virus e in alcuni batteri. Quando vengono attivati, innescano catene di segnalazione interne che portano al rilascio di messaggeri chimici, o citochine, che modellano l’infiammazione e la difesa antivirale. Il gruppo ha confrontato i monociti del sangue adulto con quelli del sangue del cordone ombelicale di neonati sani, chiedendosi quanto fossero espressi TLR7 e TLR8 e come rispondessero quando attivati da due composti simili a farmaci che imitano l’RNA virale.
Un cablaggio diverso nelle cellule neonatali e adulte
I ricercatori hanno riscontrato che i monociti neonatali possiedono quantità di TLR7 simili a quelle degli adulti ma hanno notevolmente meno TLR8. Nonostante ciò, quando questi recettori sono stati attivati con i composti di prova, sia le cellule adulte sia quelle neonatali hanno rilasciato livelli comparabili del forte mediatore infiammatorio TNF-alfa e della citochina versatile IL-6. La grande differenza è emersa con IL-10, un segnale calmante che aiuta a spegnere l’infiammazione prima che diventi dannosa. Le cellule adulte producevano abbondante IL-10 dopo la stimolazione di TLR7/8, mentre le cellule neonatali ne producevano quasi nulla, anche se potevano generare IL-10 quando veniva attivata un’altra via. Questo schema suggerisce che i monociti neonatali sono programmati per montare una forte infiammazione ma sono privi di un importante “pedale del freno”.
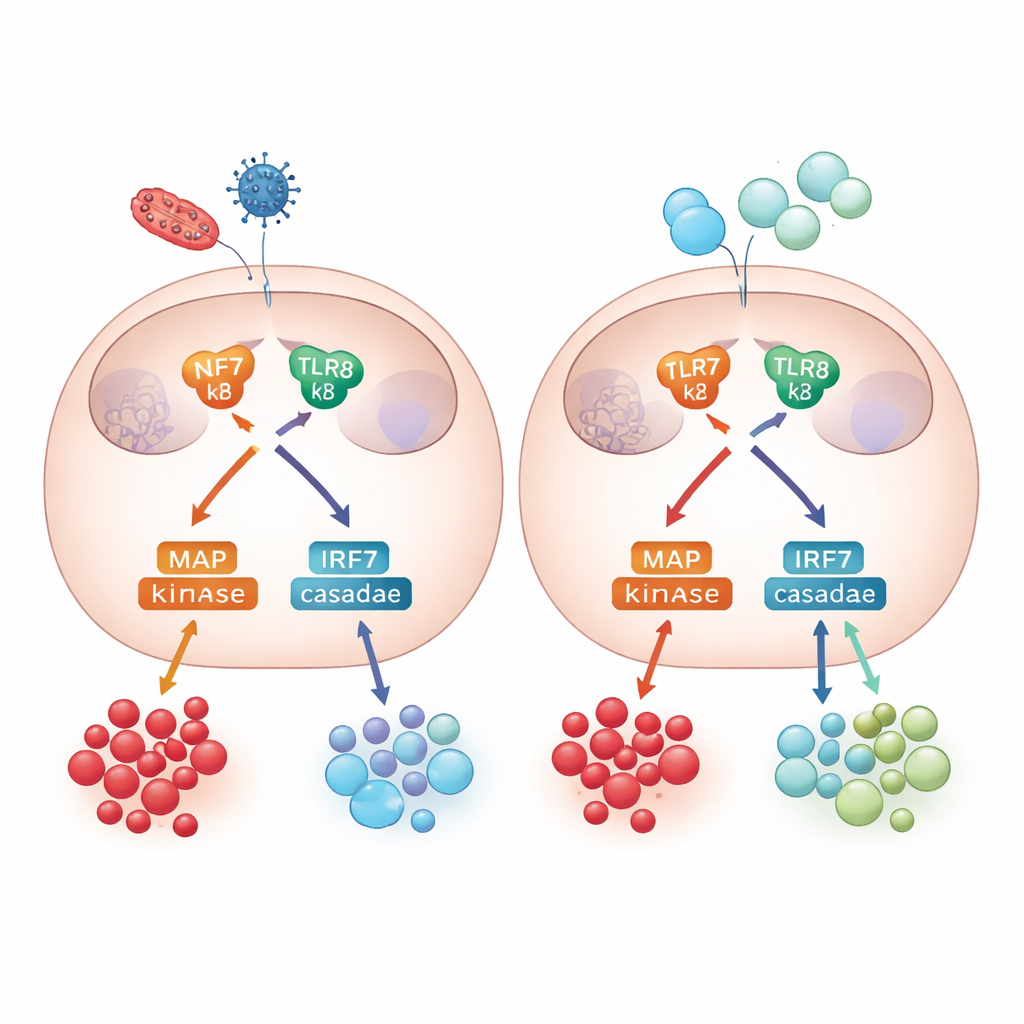
All’interno della sala di controllo della segnalazione
Per capire come emergano queste differenze, il gruppo ha esplorato la macchina interna di segnalazione che collega l’attivazione di TLR7/8 al rilascio di citochine. Sia i monociti adulti sia quelli neonatali attivavano le principali vie di segnale, inclusi NF-κB e un gruppo di enzimi chiamati chinasi MAP. Il blocco di una di queste chinasi, p38, ha avuto effetti soltanto modesti sui segnali infiammatori come TNF-alfa e IL-6 ma ha ridotto fortemente la produzione di IL-10 nelle cellule adulte, sottolineando che il controllo anti-infiammatorio dipende da questa via. Lo studio ha anche esaminato le risposte antivirali: sia i monociti adulti sia quelli neonatali hanno attivato il fattore di trascrizione IRF7 e prodotto interferoni di tipo I, citochine antivirali chiave, mostrando che le difese antivirali erano in gran parte intatte nei neonati nonostante il feedback regolatorio fosse più debole.
Quando un allarme virale incontra una minaccia batterica
Poiché le infezioni nel mondo reale spesso si verificano in sequenza — per esempio un virus seguito da un invasore batterico — i ricercatori hanno imitato questo scenario in laboratorio. Hanno prima stimolato TLR7/8 nei monociti, poi hanno esposto le cellule a E. coli fluorescenti per monitorare quanto bene le inghiottivano e uccidevano. La precedente attivazione di TLR7/8 ha modificato i livelli delle molecole di superficie coinvolte nell’assorbimento batterico e in generale ha ridotto la capacità delle cellule di inglobare E. coli, soprattutto nei monociti neonatali. Tuttavia, in modo intrigante, il pretrattamento con il composto focalizzato su TLR7, imiquimod, ha portato a una ridotta sopravvivenza di E. coli nelle cellule neonatali, suggerendo che, pur captando meno batteri, potrebbero ucciderli più efficacemente una volta all’interno. Il rilascio di citochine durante queste co-sfide non ha mostrato una forte sinergia, ma gli adulti hanno nuovamente mostrato un mix più equilibrato di segnali infiammatori e anti-infiammatori rispetto ai neonati.
Cosa significa per i neonati fragili
Nel complesso, il lavoro dipinge il quadro di monociti neonatali in grado di riconoscere virus e batteri e di montare risposte infiammatorie e antivirali solide, ma privi dell’interruttore di spegnimento IL-10 che aiuta gli adulti a evitare un’infiammazione eccessiva e persistente. Questo squilibrio può contribuire alla suscettibilità dei neonati a infezioni gravi e a complicazioni come la sepsi. Allo stesso tempo, l’osservazione che un composto che mira a TLR7 può diminuire la sopravvivenza batterica nelle cellule neonatali suggerisce che farmaci finemente calibrati potrebbero un giorno aumentare la protezione contro infezioni opportunistiche. Qualsiasi approccio di questo tipo richiederebbe test approfonditi, ma questo studio offre una mappa meccanicistica per comprendere — e potenzialmente migliorare — le difese immunitarie nella prima infanzia.
Citazione: Dreschers, S., Heiler, E., Oppermann, L. et al. TLR7/8 signaling balances cytokine responses in neonatal monocytes. Sci Rep 16, 12202 (2026). https://doi.org/10.1038/s41598-026-46534-6
Parole chiave: immunità del neonato, recettori Toll-like, monociti, sepsi neonatale, infiammazione