Clear Sky Science · zh
富含胆固醇的饮食加剧了STAM小鼠模型中的脂肪性肝炎
这一点对日常健康为何重要
脂肪肝疾病不再只是酗酒者的专属问题;伴随肥胖和2型糖尿病的人群中发病率正在上升。本研究提出了一个出人意料但很实用的问题:我们饮食中的胆固醇只是提高血液中的含量,还是能主动促使肝脏从相对沉默的脂肪堆积转变为更危险的、瘢痕化和炎症性状态?通过微调一个广泛使用的晚期糖尿病小鼠模型,研究者证明额外的膳食胆固醇会显著加重肝脏损伤,有助于科学家为未来药物搭建更合适的测试平台。
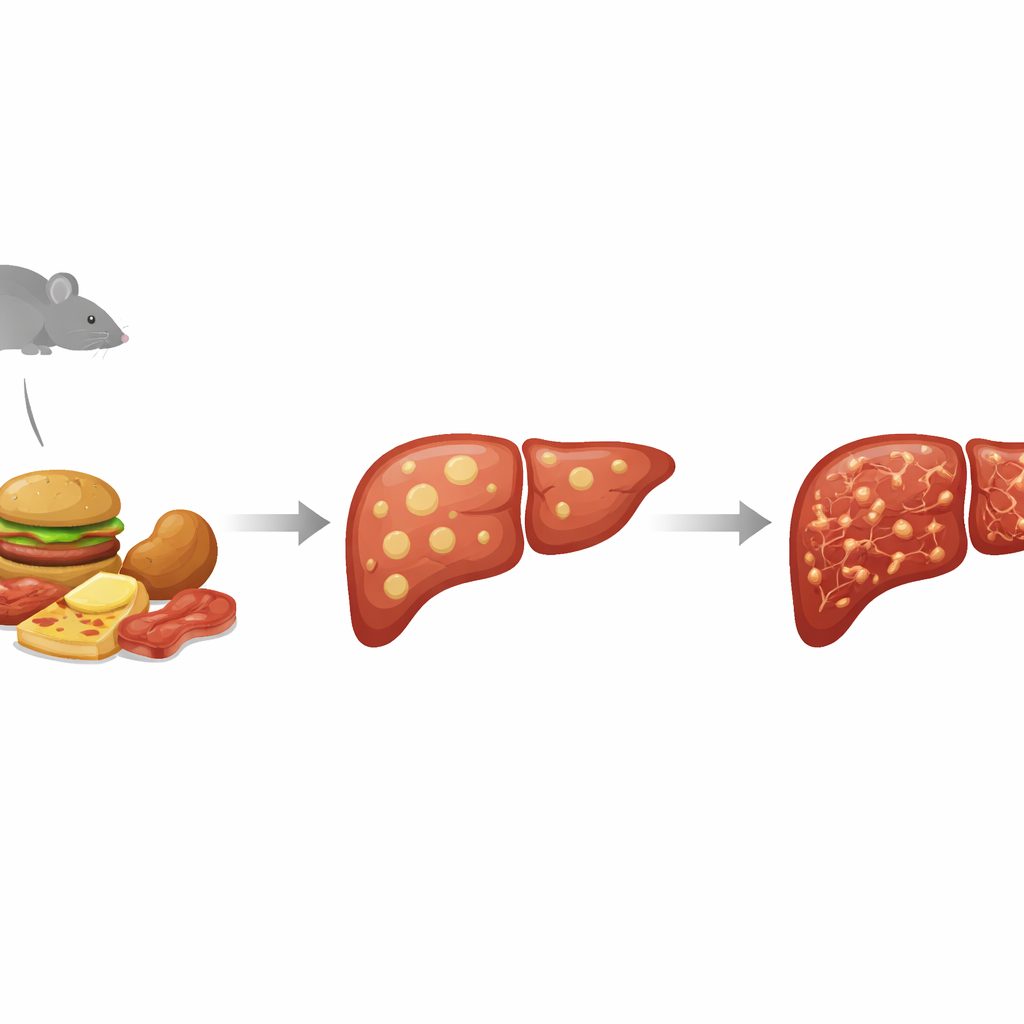
从简单的脂肪堆积到病变、瘢痕化的肝脏
临床上现在把广泛的脂肪肝问题归入“代谢功能障碍相关脂肪性肝病”(MASLD)的范畴。在轻度阶段,肝细胞只是储存过多脂肪;在重度阶段,器官出现炎症和瘢痕化,称为代谢功能障碍相关脂肪性肝炎(MASH),可进展为肝硬化和肝癌。由于在人体中研究这一整个进展过程既困难又有风险,研究者依赖模拟糖代谢异常与肝脏逐步损伤的动物模型。STAM小鼠模型通过化学方法损伤胰腺的胰岛素产生细胞,然后给予高脂饮食,使动物进入类似糖尿病的状态,从而快速出现肝病。
通过额外胆固醇把调节旋钮拧大
研究团队探讨了如果用不仅富含脂肪且富含胆固醇和某些植物油的饮食替代标准高脂饲料,会发生什么。雄性小鼠接受或不接受STAM处理,然后分别喂以经典高脂饮食或高脂高胆固醇饮食,并随访长达16周。如预期,STAM小鼠出现高血糖并丧失体脂,反映严重的糖尿病。胆固醇丰富饮食带来的变化出现在肝脏:这些小鼠在更早期出现更大、更富脂的肝脏,肝细胞内既有大脂滴也有小脂滴混合存在。其总体疾病评分——涵盖脂肪堆积、炎症和受损、肿胀的肝细胞——在高胆固醇的STAM组中最高。
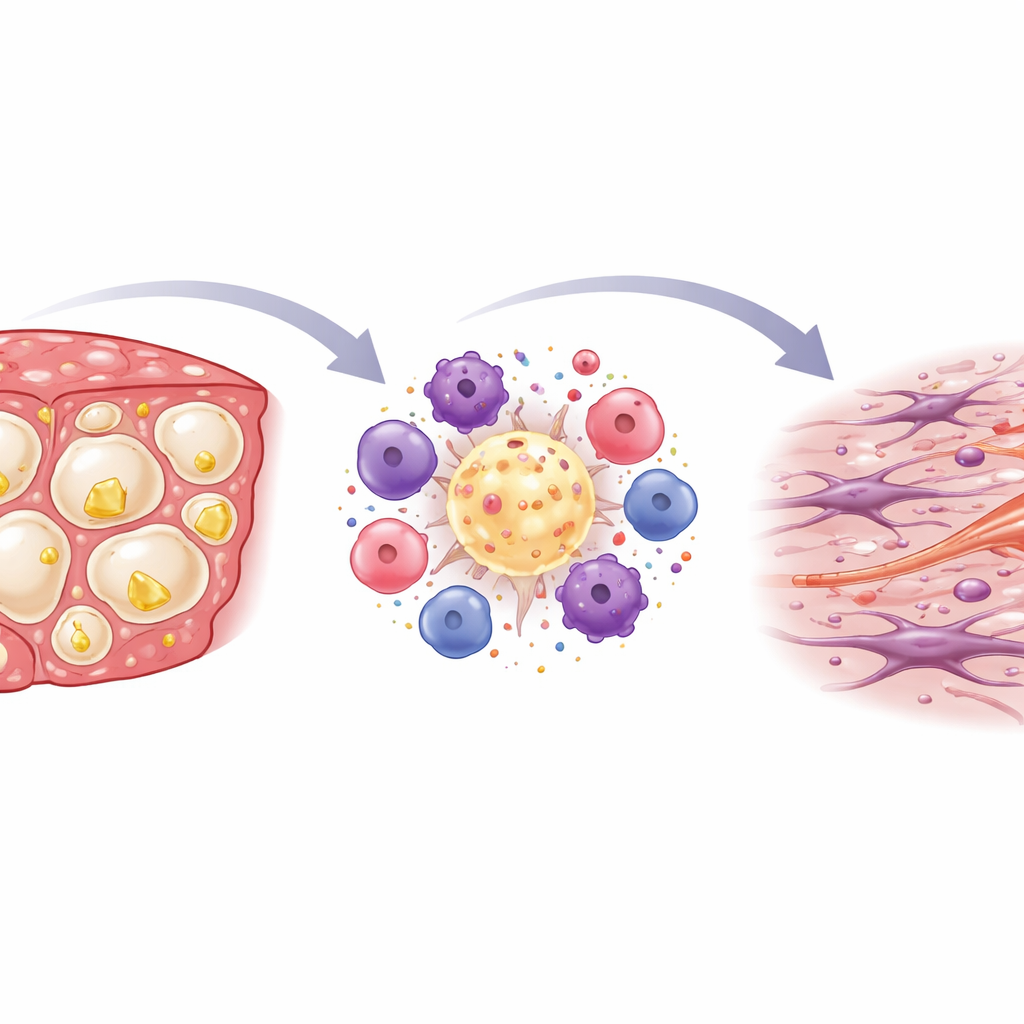
肝脏内部的炎症与瘢痕形成
当研究者对肝切片进行染色并在显微镜下观察时,发现富胆固醇饮食大幅增强了免疫活性。免疫细胞聚集形成皇冠样环绕在濒死且脂肪堆积的肝细胞周围,这一模式此前与进展性的人类MASH有关。来自肝组织的化学指标证实了这一图景:标记免疫细胞和经典炎性介质的基因在高胆固醇STAM小鼠中被强烈激活。随着时间推移,这种炎症伴随着瘢痕组织的积累。特异性染色显示胶原纤维增加,特别是在这些免疫细胞簇周围,与纤维化相关的基因显著上调,表明产生瘢痕的细胞被激活了。
胆固醇在分子水平上的作用
为更深入理解这一过程,团队分析了不同饮食下肝脏中基因活性的变化。在STAM小鼠中,富含胆固醇的饮食改变了肝脏处理脂质与胆固醇的通路平衡,可能促成细胞内形成有毒且无法缓冲的胆固醇库。与此同时,与免疫反应、炎性信号传导和组织基质重塑相关的基因网络被强烈激活,尤以动物从8周龄到12周龄时更明显。综合来看,这些模式支持这样一种叙述:额外的胆固醇加剧了肝细胞的应激,招募免疫细胞,进而驱动支持细胞转化为产生纤维的细胞,沉积持久的瘢痕组织。
该模型如何加速更好疗法的研发
尽管没有任何小鼠模型可以完全复制人类脂肪肝疾病——后者通常伴随肥胖和高胰岛素水平——但改良后的STAM模型捕捉到了一个关键环节:在晚期糖尿病背景下,胆固醇驱动的肝损伤加重。通过在确定的时间过程中稳定地诱导强烈的炎症和纤维化,该模型为旨在阻止或逆转瘢痕形成的实验性药物提供了更现实的测试场景。简单来说,这项研究表明,至少在该模型中,膳食胆固醇并非无辜旁观者;它有助于将脂肪肝推向持久性损伤。这个见解以及基于它改进的模型,应能帮助研究者更快识别出哪些未来疗法最有可能保护人类肝脏免受代谢性疾病长期后果的侵害。
引用: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
关键词: 脂肪肝疾病, 膳食胆固醇, 肝纤维化, 2型糖尿病, 小鼠疾病模型