Clear Sky Science · it
Una dieta ricca di colesterolo aggrava la steatoepatite nel modello murino STAM
Perché è importante per la salute quotidiana
La steatosi epatica non riguarda più solo le persone che bevono molto alcol; colpisce sempre più spesso chi convive con obesità e diabete di tipo 2. Questo studio pone una domanda sorprendentemente pratica: il colesterolo nella nostra dieta si limita ad aumentare i livelli ematici oppure può attivamente trasformare il fegato da un accumulo di grasso relativamente silente in uno stato molto più pericoloso, fibrotico e infiammato? Mettendo a punto un modello murino ampiamente usato per il diabete avanzato, i ricercatori dimostrano che aggiungere colesterolo alla dieta peggiora nettamente il danno epatico, aiutando gli scienziati a costruire piattaforme di test migliori per i futuri farmaci.
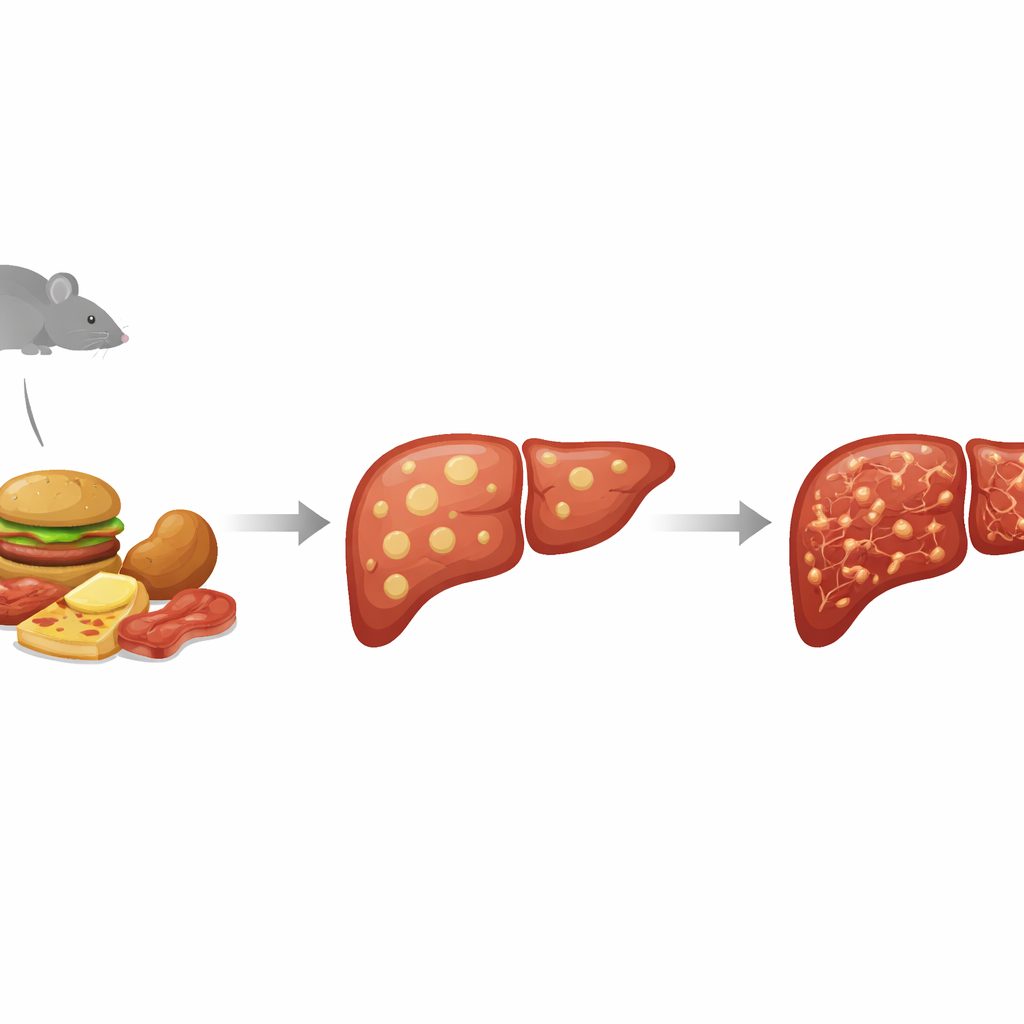
Da semplice accumulo di grasso a fegato malato e cicatrizzato
I medici ora raggruppano una vasta gamma di problemi epatici grassi sotto l’ombrello della malattia epatica steatosica associata a disfunzione metabolica (MASLD). Nella forma lieve, le cellule del fegato accumulano semplicemente troppo grasso. Nella forma grave, l’organo si infiamma e si cicatrizza, una condizione chiamata steatoepatite associata a disfunzione metabolica (MASH), che può progredire verso cirrosi e cancro epatico. Poiché è difficile e rischioso studiare in persone l’intera progressione, i ricercatori si affidano a modelli animali che riproducono sia i problemi metabolici del diabete sia il danno graduale all’interno del fegato. Il modello murino STAM lo ottiene danneggiando chimicamente le cellule produttrici di insulina nel pancreas e poi somministrando una dieta ad alto contenuto di grassi, spingendo gli animali in uno stato simile al diabete in cui la malattia epatica si sviluppa rapidamente.
Aumentare la dose con colesterolo extra
Il gruppo ha chiesto cosa succede se la dieta standard ad alto contenuto di grassi in questo modello viene sostituita da una dieta non solo ricca di grassi ma anche di colesterolo e di alcuni oli vegetali. Ai topi maschi è stato somministrato il trattamento STAM o non è stato effettuato alcun trattamento, quindi sono stati alimentati o con la classica dieta ad alto contenuto di grassi o con la versione ricca di grassi e colesterolo e seguiti fino a 16 settimane. Come previsto, i topi STAM hanno sviluppato iperglicemia e hanno perso tessuto adiposo, riflettendo un diabete severo. Ciò che è cambiato con la dieta ricca di colesterolo è stato il fegato: questi animali mostravano fegati più grandi e più grassi fin dalla giovane età, con una miscela di goccioline lipidiche grandi e piccole nelle cellule epatiche. I loro punteggi complessivi di malattia — che includono accumulo di grasso, infiammazione e cellule epatiche danneggiate e gonfie — erano più alti nel gruppo STAM ad alto contenuto di colesterolo.
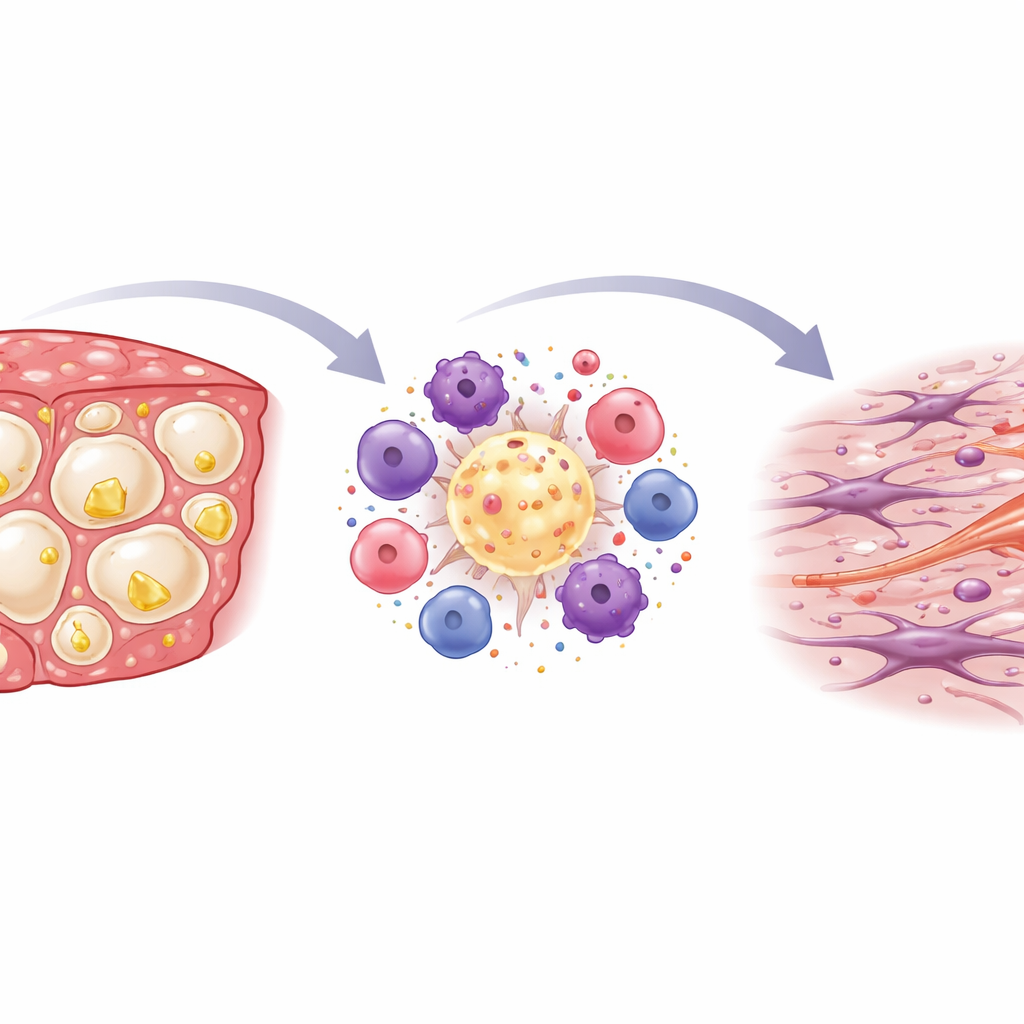
Infiammazione e cicatrizzazione all’interno del fegato
Quando i ricercatori hanno colorato ed esaminato le sezioni di fegato al microscopio, hanno osservato che la dieta ricca di colesterolo aumentava notevolmente l’attività immunitaria. Aggregati di cellule immunitarie formavano anelli a corona attorno a cellule epatiche morenti e ricche di grasso, un pattern associato in precedenza a forme aggressive di MASH nell’uomo. Letture chimiche dai tessuti epatici hanno confermato questo quadro: i geni che marcano le cellule immunitarie e i classici mediatori infiammatori erano più fortemente attivati nei topi STAM ad alto contenuto di colesterolo. Nel tempo, questa infiammazione è andata di pari passo con l’accumulo di tessuto cicatriziale. Colorazioni speciali hanno rivelato un aumento delle fibre di collagene, soprattutto intorno a questi ammassi immunitari, e i geni associati alla fibrosi erano chiaramente elevati, indicando l’attivazione delle cellule che producono cicatrici.
Cosa fa il colesterolo a livello molecolare
Per comprendere più a fondo il processo, il team ha analizzato quali geni nel fegato cambiavano la loro attività nelle diverse diete. Nei topi STAM, la dieta ricca di colesterolo ha spostato l’equilibrio delle vie che controllano il metabolismo dei grassi e del colesterolo, in modi che probabilmente favoriscono l’accumulo di una frazione di colesterolo tossica e non tamponata all’interno delle cellule. Allo stesso tempo, reti di geni legate alle risposte immunitarie, alla segnalazione infiammatoria e al rimodellamento della struttura tissutale sono state fortemente attivate, in particolare man mano che gli animali invecchiavano da 8 a 12 settimane. Nel loro insieme, questi pattern raccontano una storia in cui il colesterolo extra aggrava lo stress delle cellule epatiche, richiama cellule immunitarie e poi spinge la trasformazione delle cellule di supporto in produttori di fibre che depositano tessuto cicatriziale permanente.
Come questo modello può accelerare terapie migliori
Sebbene nessun topo possa riprodurre completamente la steatosi epatica umana — che spesso insorge nell’obesità con livelli elevati di insulina — il modello STAM perfezionato cattura un pezzo critico del puzzle: il peggioramento del danno epatico guidato dal colesterolo nel contesto di un diabete avanzato. Producendo in modo affidabile forte infiammazione e fibrosi in un arco temporale definito, questo modello offre un terreno di prova più realistico per farmaci sperimentali mirati a fermare o invertire la cicatrizzazione. In termini pratici, lo studio mostra che, almeno in questo contesto, il colesterolo alimentare non è un semplice spettatore; contribuisce a spingere un fegato steatosico verso un danno duraturo. Questa intuizione, e il modello migliorato che ne deriva, dovrebbero aiutare i ricercatori a identificare più rapidamente quali terapie future hanno maggiori probabilità di proteggere il fegato umano dalle conseguenze a lungo termine della malattia metabolica.
Citazione: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
Parole chiave: steatosi epatica, colesterolo alimentare, fibrosi epatica, diabete di tipo 2, modelli murini di malattia