Clear Sky Science · de
Cholesterinreiche Ernährung verschlimmert Steatohepatitis im STAM-Mausmodell
Warum das für die Alltagsgesundheit wichtig ist
Fettlebererkrankung ist längst nicht mehr nur ein Problem bei starkem Alkoholkonsum; sie betrifft zunehmend Menschen mit Adipositas und Typ‑2‑Diabetes. Diese Studie stellt eine überraschend praktische Frage: Führt das Cholesterin in unserer Nahrung nur zu höheren Blutwerten, oder kann es aktiv die Leber von einer vergleichsweise ruhigen Fettspeicherung in einen weitaus gefährlicheren, vernarbten und entzündeten Zustand treiben? Durch die Feinabstimmung eines weit verbreiteten Mausmodells für fortgeschrittenen Diabetes zeigen die Forschenden, dass zusätzliches diätetisches Cholesterin die Leberschädigung deutlich verschärft und so bessere Testbedingungen für künftige Arzneimittel schafft.
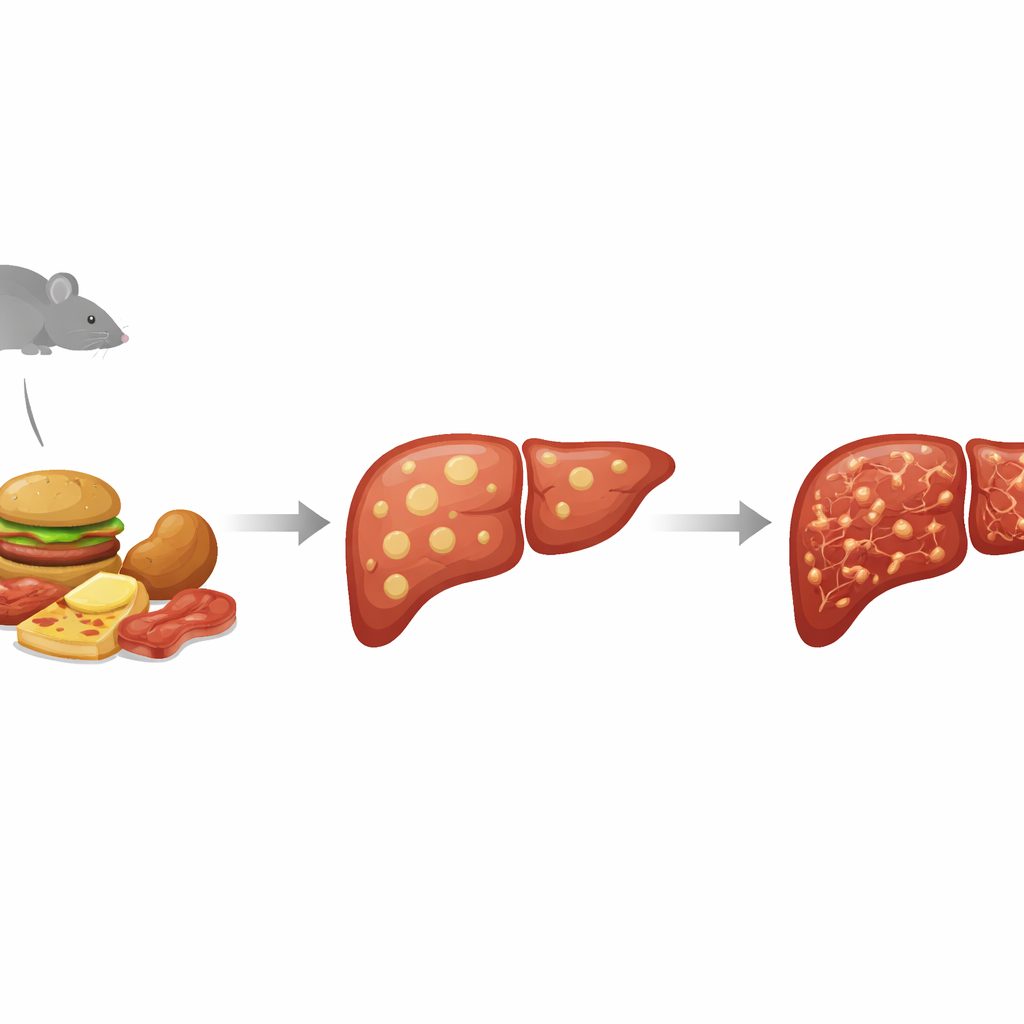
Von einfacher Fettspeicherung zur kranken, vernarbten Leber
Ärztinnen und Ärzte fassen heute ein breites Spektrum an Leberfettproblemen unter dem Begriff „metabolic dysfunction–associated steatotic liver disease“ (MASLD) zusammen. Am milden Ende speichern Leberzellen einfach zu viel Fett. Am schweren Ende entzündet sich das Organ und vernarbt – ein Zustand, der als metabolic dysfunction–associated steatohepatitis (MASH) bezeichnet wird und zu Zirrhose und Leberkrebs fortschreiten kann. Weil es schwierig und riskant ist, diesen gesamten Verlauf beim Menschen zu untersuchen, stützen sich Forschende auf Tiermodelle, die sowohl die metabolischen Probleme des Diabetes als auch die schrittweise Schädigung der Leber nachbilden. Das STAM‑Mausmodell erreicht dies, indem es die insulinproduzierenden Zellen der Bauchspeicheldrüse chemisch schädigt und die Tiere anschließend mit einer fettreichen Diät füttert, wodurch sie in einen diabetesähnlichen Zustand gedrängt werden, in dem sich schnell Lebererkrankungen entwickeln.
Den Pegel aufdrehen mit zusätzlichem Cholesterin
Das Team fragte, was passiert, wenn die standardmäßige fettreiche Diät in diesem Modell durch eine ersetzt wird, die nicht nur reich an Fett, sondern auch an Cholesterin und bestimmten Pflanzenölen ist. Männliche Mäuse erhielten die STAM‑Behandlung oder blieben unbehandelt, wurden dann entweder mit der klassischen fettreichen Diät oder mit der fettreichen, cholesterinreichen Variante gefüttert und bis zu 16 Wochen beobachtet. Wie erwartet entwickelten die STAM‑Mäuse hohen Blutzucker und verloren Körperfett, ein Zeichen für schweren Diabetes. Was sich durch die cholesterinreiche Diät änderte, war die Leber: Diese Mäuse zeigten schon früher größere, fettigere Lebern mit einer Mischung aus großen und kleinen Fetttröpfchen in den Leberzellen. Ihre Gesamtkrankheitsscores – die Fettspeicherung, Entzündung und verletzte, geschwollene Leberzellen erfassen – waren in der cholesterinreichen STAM‑Gruppe am höchsten.
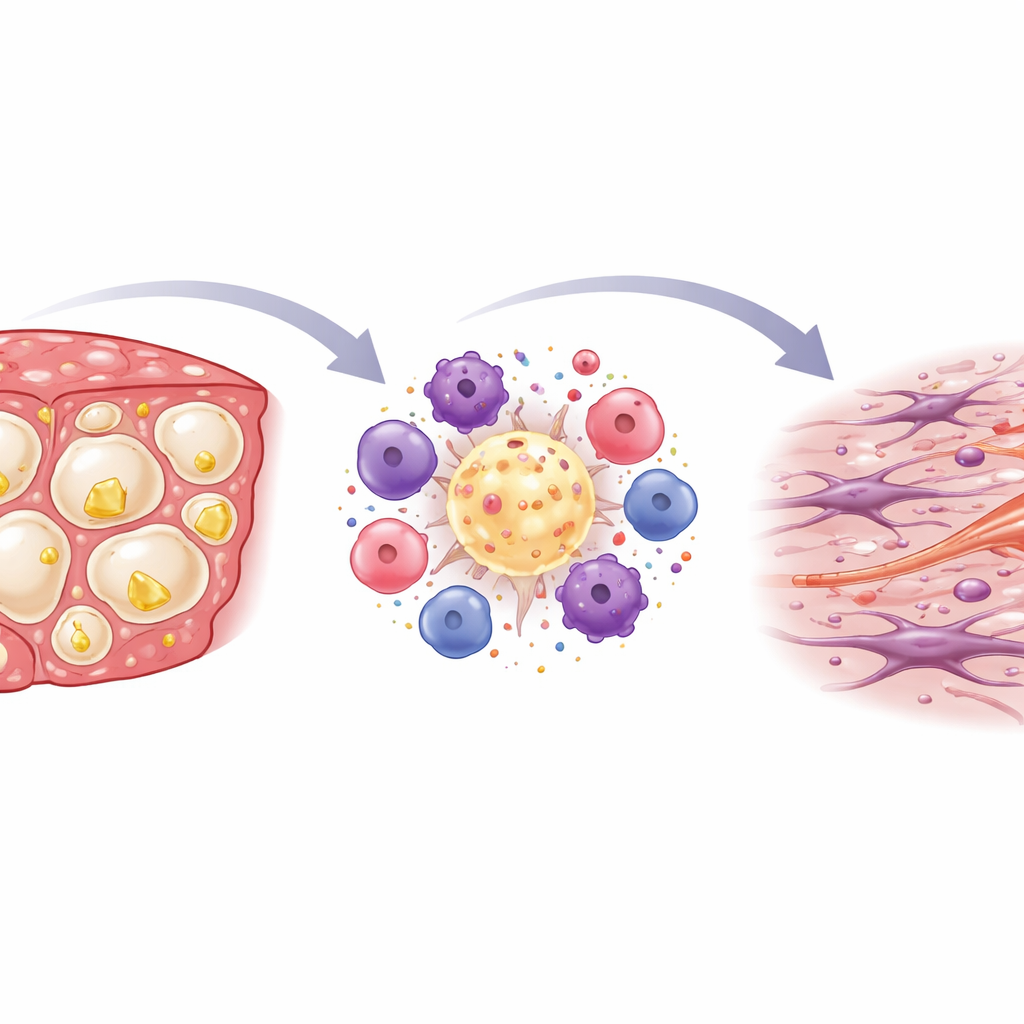
Entzündung und Vernarbung in der Leber
Als die Forschenden Leberscheiben anfärbten und mikroskopisch untersuchten, sahen sie, dass die cholesterinreiche Diät die Immunaktivität stark erhöhte. Ansammlungen von Immunzellen bildeten kronenartige Ringe um sterbende, fetthaltige Leberzellen – ein Muster, das zuvor mit aggressiver menschlicher MASH in Verbindung gebracht wurde. Chemische Messungen aus Lebergewebe bestätigten dieses Bild: Gene, die Immunzellen markieren, und klassische Entzündungsbotenstoffe waren in den cholesterinreichen STAM‑Mäusen am stärksten aktiviert. Mit der Zeit ging diese Entzündung einher mit der Bildung von Narbengewebe. Spezielle Anfärbungen zeigten zunehmend Kollagenfasern, besonders um diese Immun‑Cluster, und Gene, die mit Fibrose assoziiert sind, waren deutlich erhöht, was darauf hindeutet, dass narbenbildende Zellen aktiviert worden waren.
Was Cholesterin auf molekularer Ebene bewirkt
Um den Prozess tiefer zu verstehen, analysierte das Team, welche Gene in der Leber unter den verschiedenen Diäten ihre Aktivität veränderten. Bei STAM‑Mäusen verschob die cholesterinreiche Diät das Gleichgewicht der Signalwege, die steuern, wie die Leber Fette und Cholesterin verarbeitet, in Richtung einer Konstellation, die wahrscheinlich die Ansammlung eines toxischen, ungepufferten Cholesterinpools in den Zellen begünstigt. Gleichzeitig wurden Netzwerke von Genen, die mit Immunantworten, Entzündungs‑Signalen und Umgestaltung des Gewebe‑Gerüsts verknüpft sind, stark aktiviert, insbesondere als die Tiere von 8 auf 12 Wochen alterten. Zusammen passen diese Muster zu einer Geschichte, in der zusätzliches Cholesterin den Stress in Leberzellen verstärkt, Immunzellen anzieht und dann die Umwandlung von Stütz‑Zellen in faserproduzierende Zellen antreibt, die dauerhaftes Narbengewebe ablagern.
Wie dieses Modell bessere Behandlungen beschleunigen kann
Auch wenn keine Maus die menschliche Fettlebererkrankung vollständig abbilden kann – die beim Menschen oft in einer Adipositas mit hohen Insulinwerten entsteht – fängt das verfeinerte STAM‑Modell ein kritisches Puzzleteil ein: die cholesterinbedingte Verschlechterung der Leberschädigung im Kontext fortgeschrittenen Diabetes. Indem es zuverlässig starke Entzündung und Fibrose über einen definierten Zeitverlauf erzeugt, bietet dieses Modell einen realistischeren Prüfstand für experimentelle Wirkstoffe, die darauf abzielen, Vernarbung zu stoppen oder rückgängig zu machen. Einfach gesagt zeigt die Studie, dass diätetisches Cholesterin zumindest in diesem Setting kein unschuldiger Zuschauer ist; es trägt dazu bei, eine fette Leber in Richtung dauerhafter Schädigung zu treiben. Diese Erkenntnis und das darauf basierende verbesserte Modell sollten Forschenden helfen, schneller zu erkennen, welche zukünftigen Therapien am ehesten menschliche Lebern vor den langfristigen Folgen metabolischer Erkrankungen schützen können.
Zitation: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
Schlüsselwörter: Fettlebererkrankung, diätetisches Cholesterin, Leberfibrose, Typ-2-Diabetes, Maus-Krankheitsmodelle