Clear Sky Science · fr
Un régime riche en cholestérol aggrave la stéato‑hépatite dans le modèle murin STAM
Pourquoi c’est important pour la santé quotidienne
La maladie du foie gras ne concerne plus seulement les personnes qui boivent beaucoup d’alcool ; elle touche de plus en plus celles vivant avec l’obésité et le diabète de type 2. Cette étude pose une question étonnamment pratique : le cholestérol de notre alimentation se contente‑t‑il d’élever le taux sanguin, ou peut‑il activement conduire le foie d’un simple stockage de graisse relativement silencieux vers un état beaucoup plus dangereux, inflammatoire et cicatriciel ? En ajustant finement un modèle murin largement utilisé d’un stade avancé du diabète, les chercheurs montrent que l’ajout de cholestérol alimentaire aggrave fortement les lésions hépatiques, fournissant aux scientifiques de meilleurs bancs d’essai pour les médicaments à venir.
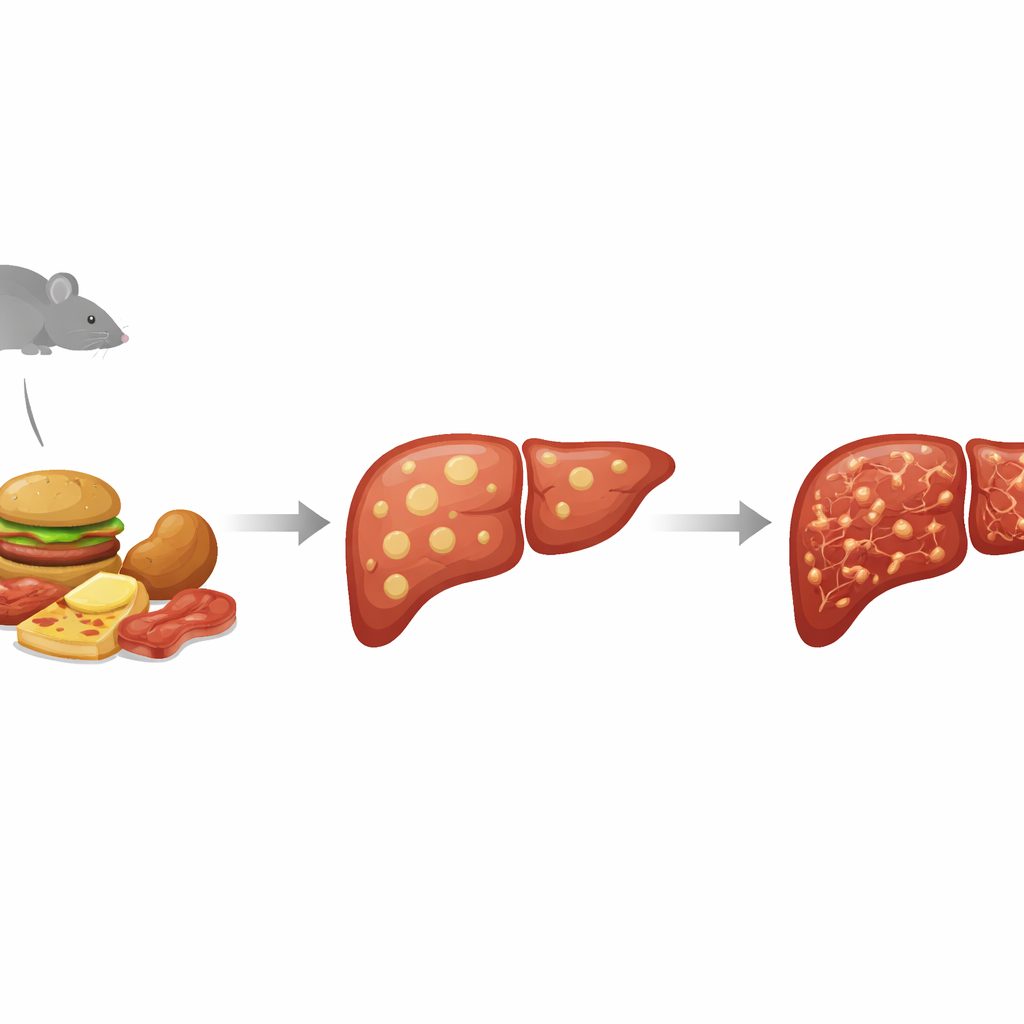
Du simple excès de graisse au foie malade et cicatriciel
Les médecins regroupent aujourd’hui une large gamme de problèmes hépatiques liés aux graisses sous l’appellation maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD). À l’extrémité légère, les cellules hépatiques stockent simplement trop de graisse. À l’extrémité sévère, l’organe s’enflamme et se cicatrise : il s’agit de la stéatohépatite associée à un dysfonctionnement métabolique (MASH), qui peut évoluer vers la cirrhose et le cancer du foie. Parce qu’il est difficile et risqué d’étudier toute cette progression chez l’humain, les chercheurs s’appuient sur des modèles animaux imitant à la fois les troubles métaboliques du diabète et l’endommagement progressif du foie. Le modèle murin STAM reproduit cela en détruisant chimiquement les cellules productrices d’insuline du pancréas puis en nourrissant les animaux avec un régime riche en graisses, les poussant vers un état proche du diabète où la maladie du foie se développe rapidement.
Augmenter la pression avec du cholestérol supplémentaire
L’équipe a examiné ce qui se passe si le régime riche en graisses standard de ce modèle est remplacé par un régime non seulement riche en graisses, mais aussi en cholestérol et en certaines huiles végétales. Des souris mâles ont reçu le traitement STAM ou sont restées non traitées, puis ont été alimentées soit avec le régime riche en graisses classique, soit avec la version riche en graisses et en cholestérol, et suivies jusqu’à 16 semaines. Comme prévu, les souris STAM ont développé une hyperglycémie et perdu de la masse grasse, reflétant un diabète sévère. Ce qui a changé avec le régime riche en cholestérol, c’est le foie : ces souris présentaient des foies plus volumineux et plus graisseux plus tôt dans la vie, avec un mélange de grosses et de petites gouttelettes lipidiques dans leurs hépatocytes. Leurs scores globaux de maladie — intégrant l’accumulation de graisse, l’inflammation et les cellules hépatiques lésées et enflées — étaient les plus élevés dans le groupe STAM à forte teneur en cholestérol.
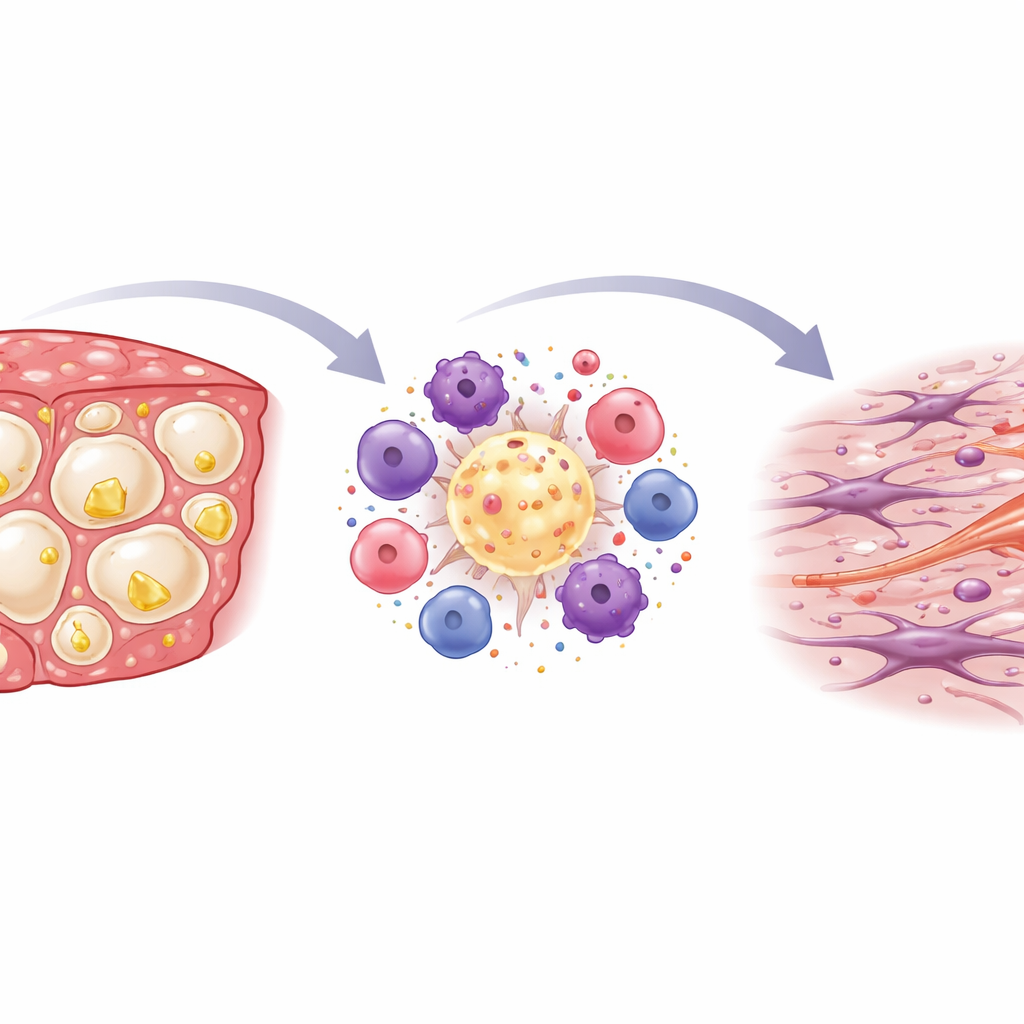
Inflammation et cicatrisation à l’intérieur du foie
Lorsque les chercheurs ont coloré et examiné des coupes de foie au microscope, ils ont observé que le régime riche en cholestérol renforçait fortement l’activité immunitaire. Des amas de cellules immunitaires formaient des anneaux en couronne autour de cellules hépatiques mourantes et chargées de graisses, un schéma déjà associé à une MASH humaine agressive. Les analyses chimiques des tissus hépatiques confirment ce tableau : des gènes marquant les cellules immunitaires et des médiateurs inflammatoires classiques étaient les plus fortement exprimés chez les souris STAM à haute teneur en cholestérol. Avec le temps, cette inflammation s’accompagnait d’un dépôt de tissu cicatriciel. Des colorations spécialisées ont révélé une augmentation des fibres de collagène, en particulier autour de ces amas immunitaires, et les gènes liés à la fibrose étaient nettement élevés, indiquant l’activation de cellules productrices de fibres.
Ce que fait le cholestérol au niveau moléculaire
Pour comprendre le processus plus en profondeur, l’équipe a analysé l’activité des gènes hépatiques selon les différents régimes. Chez les souris STAM, le régime riche en cholestérol a modifié l’équilibre des voies régulant la gestion des lipides et du cholestérol par le foie, de manières susceptibles de favoriser l’accumulation d’un pool de cholestérol toxique et non tamponné à l’intérieur des cellules. Parallèlement, des réseaux de gènes liés aux réponses immunitaires, à la signalisation inflammatoire et au remodelage de la matrice tissulaire ont été fortement activés, en particulier lorsque les animaux ont vieilli de 8 à 12 semaines. Ensemble, ces profils correspondent à un scénario où l’excès de cholestérol augmente le stress des hépatocytes, attire les cellules immunitaires, puis pousse les cellules de soutien à se transformer en cellules productrices de fibres qui déposent une cicatrice permanente.
Comment ce modèle peut accélérer de meilleurs traitements
Aucune souris ne peut parfaitement reproduire la maladie du foie gras humaine — qui survient souvent dans le contexte de l’obésité avec une hyperinsulinémie — mais le modèle STAM affiné capture un élément crucial du problème : l’aggravation des lésions hépatiques liée au cholestérol dans un contexte de diabète avancé. En produisant de manière fiable une inflammation et une fibrose marquées sur une durée définie, ce modèle offre un terrain d’essai plus réaliste pour les médicaments expérimentaux visant à stopper ou inverser la cicatrisation. En termes clairs, l’étude montre que, du moins dans ce contexte, le cholestérol alimentaire n’est pas un simple spectateur ; il contribue à pousser un foie graisseux vers des dommages durables. Cette observation, et le modèle amélioré qui en découle, devraient aider les chercheurs à identifier plus rapidement quelles futures thérapies sont les plus susceptibles de protéger le foie humain des conséquences à long terme des maladies métaboliques.
Citation: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
Mots-clés: maladie du foie gras, cholestérol alimentaire, fibrose hépatique, diabète de type 2, modèles murins de maladie