Clear Sky Science · es
Una dieta rica en colesterol agrava la esteatohepatitis en el modelo murino STAM
Por qué importa esto para la salud cotidiana
La enfermedad del hígado graso ya no es solo una preocupación para las personas que consumen alcohol en exceso; afecta cada vez más a quienes viven con obesidad y diabetes tipo 2. Este estudio plantea una pregunta sorprendentemente práctica: ¿el colesterol de nuestra dieta simplemente eleva los niveles en sangre o puede impulsar activamente al hígado desde una acumulación relativamente silenciosa de grasa hacia un estado mucho más peligroso, con cicatrices e inflamación? Al afinar un modelo murino ampliamente utilizado de diabetes avanzada, los investigadores muestran que añadir colesterol a la dieta empeora de forma notable el daño hepático, ayudando a construir mejores bancos de prueba para futuros fármacos.
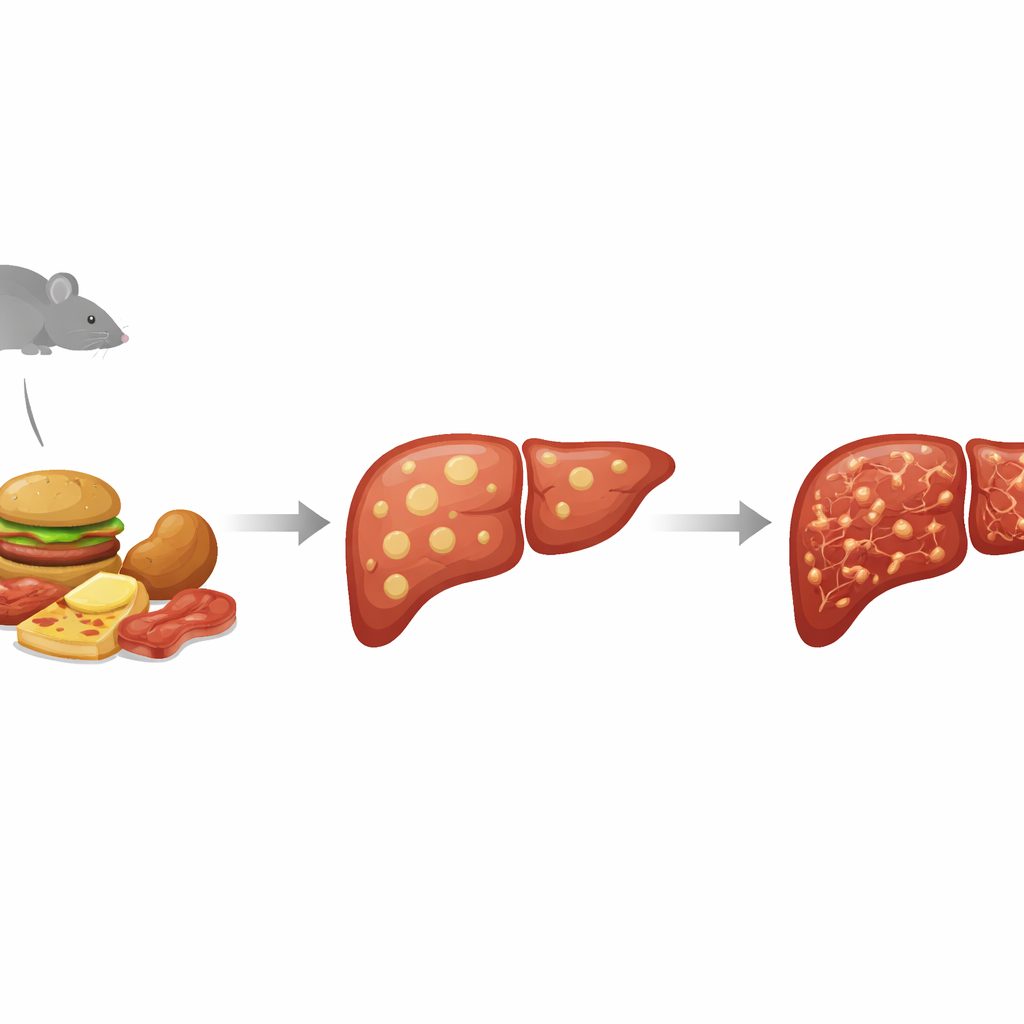
De la grasa simple a un hígado enfermo y cicatrizado
Los médicos agrupan ahora una amplia gama de problemas hepáticos grasos bajo el término enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD). En el extremo leve, las células hepáticas simplemente almacenan demasiada grasa. En el extremo grave, el órgano se inflama y cicatriza, una condición llamada esteatohepatitis asociada a disfunción metabólica (MASH), que puede evolucionar hacia cirrosis y cáncer de hígado. Dado que es difícil y arriesgado estudiar toda esta progresión en personas, los investigadores recurren a modelos animales que imitan tanto los problemas metabólicos de la diabetes como el daño progresivo en el hígado. El modelo murino STAM hace esto dañando químicamente las células productoras de insulina en el páncreas y luego alimentando a los animales con una dieta alta en grasas, empujándolos hacia un estado similar a la diabetes donde la enfermedad hepática se desarrolla rápidamente.
Aumentando el efecto con colesterol adicional
El equipo se preguntó qué ocurre si la dieta alta en grasas estándar en este modelo se sustituye por otra que no solo es rica en grasas sino también en colesterol y ciertos aceites vegetales. A ratones machos se les aplicó el tratamiento STAM o se dejaron sin tratar; luego se alimentaron con la dieta alta en grasas clásica o con la versión alta en grasas y colesterol y se siguieron hasta 16 semanas. Como era de esperar, los ratones STAM desarrollaron hiperglucemia y perdieron grasa corporal, reflejando una diabetes severa. Lo que cambió con la dieta rica en colesterol fue el hígado: estos ratones mostraron hígados más grandes y con mayor contenido graso a una edad más temprana, con una mezcla de gotículas de grasa grandes y pequeñas en sus hepatocitos. Sus puntuaciones globales de enfermedad —que capturan la acumulación de grasa, la inflamación y las células hepáticas lesionadas e hinchadas— fueron más altas en el grupo STAM con alto colesterol.
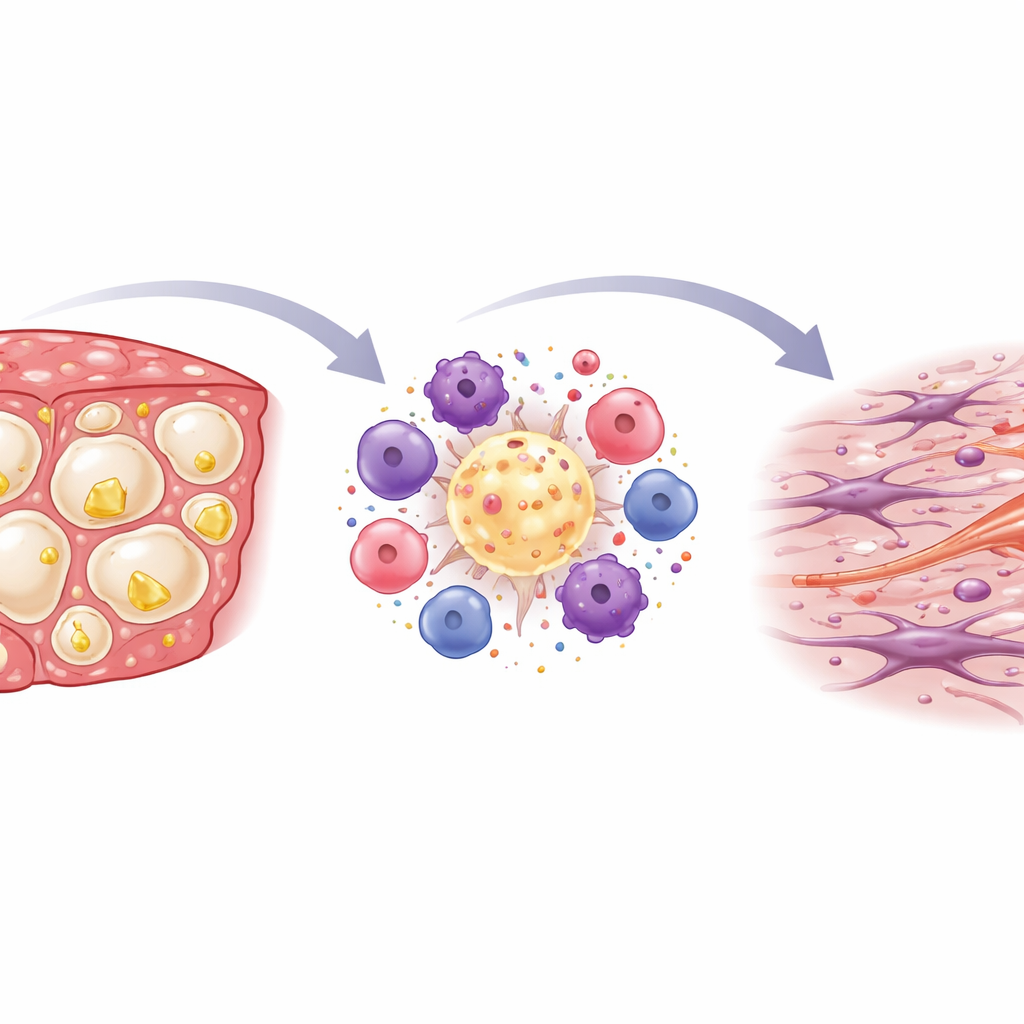
Inflamación y cicatrización dentro del hígado
Cuando los investigadores tiñeron y examinaron cortes de hígado al microscopio, vieron que la dieta rica en colesterol aumentó considerablemente la actividad inmune. Se formaron cúmulos de células inmunes en anillos en forma de corona alrededor de hepatocitos moribundos cargados de grasa, un patrón previamente vinculado con MASH humana agresiva. Los análisis químicos del tejido hepático confirmaron este panorama: los genes que marcan células inmunes y los mensajeros inflamatorios clásicos se activaron con mayor intensidad en los ratones STAM alimentados con alto colesterol. Con el tiempo, esta inflamación fue de la mano con la acumulación de tejido cicatricial. Tinciones específicas revelaron un aumento de fibras de colágeno, especialmente alrededor de estos cúmulos inmunes, y los genes asociados con la fibrosis estaban marcadamente elevados, lo que indica que las células productoras de cicatriz se habían activado.
Qué hace el colesterol a nivel molecular
Para comprender el proceso en mayor profundidad, el equipo analizó qué genes en el hígado cambiaron su actividad según las diferentes dietas. En los ratones STAM, la dieta rica en colesterol modificó el equilibrio de las rutas que controlan cómo el hígado maneja las grasas y el colesterol, de maneras que probablemente favorecen la acumulación de una reserva tóxica de colesterol no neutralizada dentro de las células. Al mismo tiempo, las redes de genes vinculadas a respuestas inmunes, señalización inflamatoria y remodelado de la matriz tisular se activaron con fuerza, particularmente a medida que los animales envejecían de 8 a 12 semanas. En conjunto, estos patrones coinciden con la historia de que el colesterol adicional agrava el estrés sobre los hepatocitos, recluta células inmunes y luego impulsa la transformación de células de soporte en células productoras de fibras que depositan tejido cicatricial permanente.
Cómo este modelo puede acelerar mejores tratamientos
Aunque ningún ratón puede reproducir completamente la enfermedad hepática grasa humana —que a menudo surge en la obesidad con niveles altos de insulina—, el modelo STAM refinado captura una pieza crítica del rompecabezas: el empeoramiento del daño hepático impulsado por el colesterol en el contexto de una diabetes avanzada. Al producir de forma fiable inflamación y fibrosis importantes en un periodo de tiempo definido, este modelo ofrece un terreno de ensayo más realista para fármacos experimentales dirigidos a detener o revertir la cicatrización. En términos sencillos, el estudio muestra que, al menos en este contexto, el colesterol dietético no es un observador inocente; ayuda a empujar un hígado graso hacia un daño duradero. Ese hallazgo, y el modelo mejorado construido en torno a él, deberían ayudar a los investigadores a identificar más rápidamente qué terapias futuras tienen más probabilidades de proteger los hígados humanos de las consecuencias a largo plazo de la enfermedad metabólica.
Cita: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
Palabras clave: enfermedad del hígado graso, colesterol dietético, fibrosis hepática, diabetes tipo 2, modelos murinos de enfermedad