Clear Sky Science · ru
Диета, богатая холестерином, усугубляет стеатогепатит в мышиной модели STAM
Почему это важно для повседневного здоровья
Жировая болезнь печени уже не ограничивается только людьми с алкоголизмом; она всё чаще встречается у людей с ожирением и сахарным диабетом 2‑го типа. В этом исследовании поставлен предельно практичный вопрос: повышает ли холестерин в пище только уровень холестерина в крови или он может активно переводить печень от сравнительно безобидного накопления жира к куда более опасному состоянию со воспалением и рубцеванием? Тонко настроив широко используемую мышиную модель продвинутого диабета, авторы показывают, что добавление диетического холестерина резко ухудшает повреждение печени, создавая более адекватную платформу для испытаний будущих препаратов.
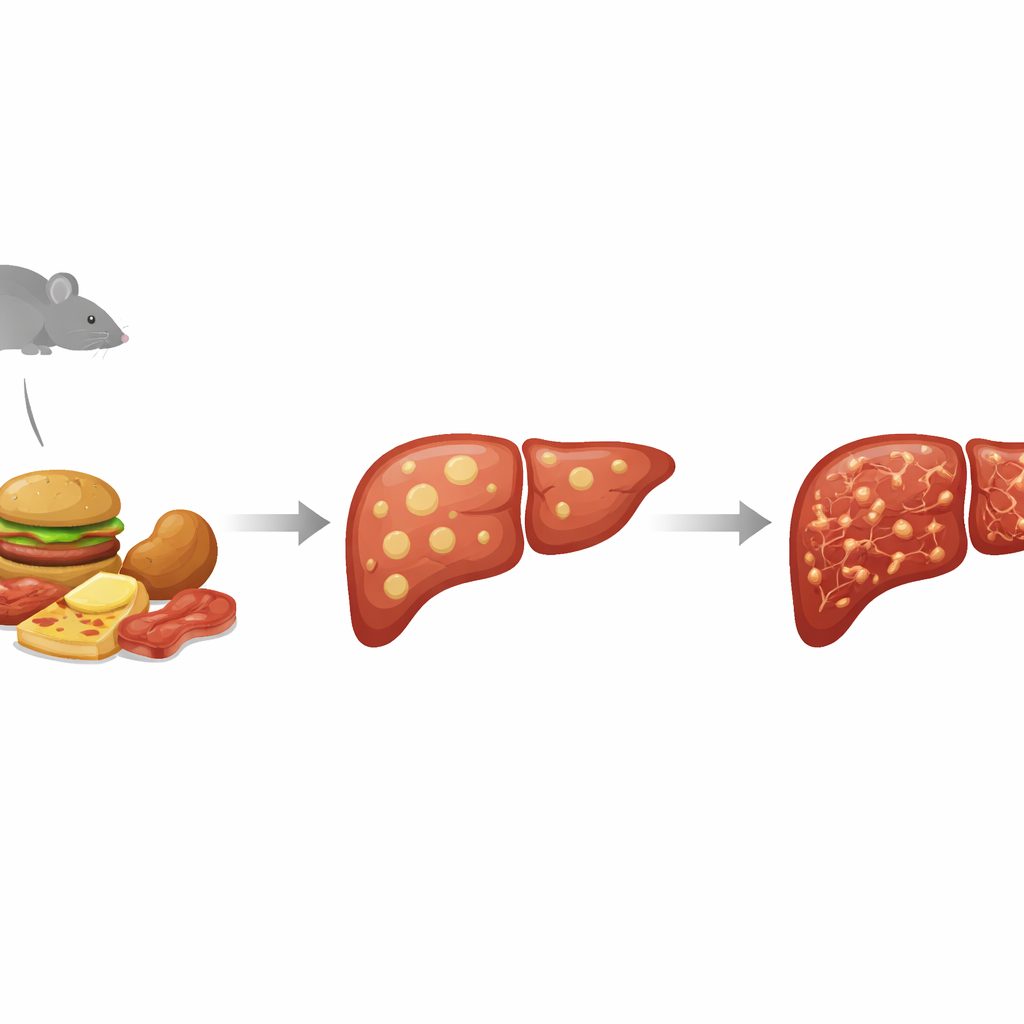
От простого жира к больной, зарубцованной печени
Врачи теперь объединяют широкий спектр проблем с жировой печенью под термином метаболически обусловленное стеатотическое заболевание печени (MASLD). В лёгкой форме клетки печени просто откладывают слишком много жира. В тяжёлой форме орган становится воспалённым и рубцуется — это состояние называется метаболически обусловленным стеатогепатитом (MASH), которое может прогрессировать в цирроз и рак печени. Поскольку изучать этот весь процесс у людей сложно и рискованно, исследователи полагаются на животные модели, имитирующие как метаболические нарушения при диабете, так и последовательное повреждение внутри печени. Модель STAM достигает этого путём химического разрушения инсуно‑продуцирующих клеток поджелудочной железы и последующего кормления животных высокожировой диетой, что переводит их в состояние, напоминающее диабет, при котором заболевание печени развивается быстро.
Усиление эффекта за счёт дополнительного холестерина
Команда изучила, что произойдёт, если стандартную высокожировую диету в этой модели заменить диетой, богатой не только жирами, но и холестерином и некоторыми растительными маслами. Самцам мышей провели процедуру STAM или оставили их без вмешательства, затем кормили либо классической высокожировой диетой, либо версией с высоким содержанием жира и холестерина и наблюдали до 16 недель. Как и ожидалось, у STAM‑мышей развилась гипергликемия и потеря жировой массы тела, что отражает тяжёлый диабет. Изменения, связанные с холестерин‑богатой диетой, наблюдались в печени: у этих животных печень становилась крупнее и жирнее на более ранних этапах, с сочетанием больших и мелких жировых включений в клетках печени. Их общие баллы по шкале поражения — учитывающей накопление жира, воспаление и повреждённые, отёчные печёночные клетки — были наивысшими в группе STAM на диете с высоким содержанием холестерина.
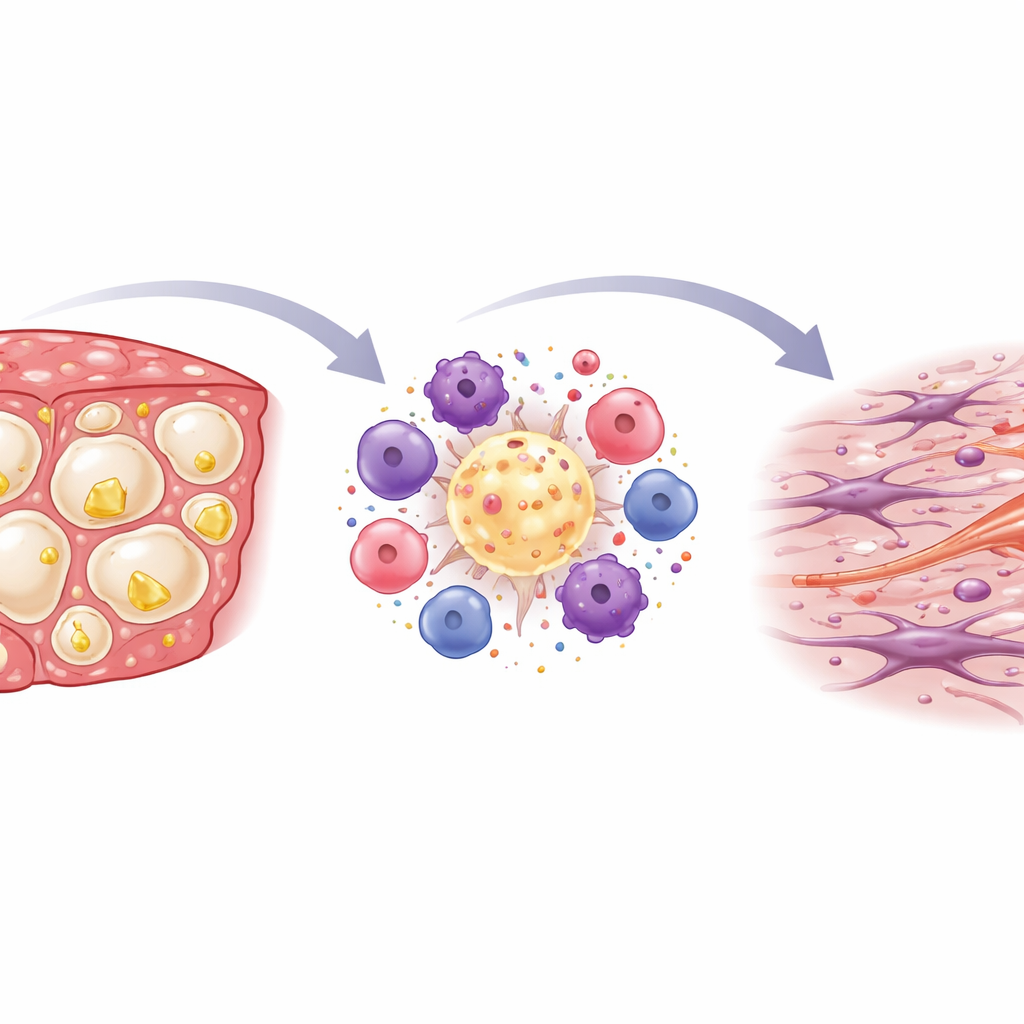
Воспаление и рубцевание внутри печени
При окрашивании и микроскопическом исследовании срезов печени исследователи увидели, что диета, богатая холестерином, значительно усиливала иммунную активность. Кластеры иммунных клеток формировали короноподобные кольца вокруг умирающих, насыщенных жиром печёночных клеток — паттерн, ранее связанный с агрессивным течением MASH у людей. Химические показатели из ткани печени подтверждали эту картину: гены, маркерующие иммунные клетки, и классические провоспалительные медиаторы были наиболее активны у STAM‑мышей на диете с высоким содержанием холестерина. Со временем это воспаление шло в ногу с накоплением рубцовой ткани. Специальные окраски выявили увеличение коллагеновых волокон, особенно вокруг этих иммунных кластеров, а гены, ассоциированные с фиброзом, были значительно повышены, что указывает на активацию клеток, продуцирующих рубцовую ткань.
Что делает холестерин на молекулярном уровне
Чтобы глубже понять процесс, команда проанализировала, какие гены в печени изменяли активность при разных диетах. У STAM‑мышей холестерин‑богатая диета смещала баланс путей, контролирующих обращение с жирами и холестерином в печени, таким образом, что, вероятно, способствовала накоплению токсического, необезвреженного пула холестерина внутри клеток. Одновременно сети генов, связанные с иммунными ответами, провоспалительной сигнализацией и ремоделированием тканевой матрицы, были сильно активированы, особенно по мере старения животных с 8 до 12 недель. В совокупности эти паттерны соответствуют сценарию, в котором дополнительный холестерин усиливает стресс в печёночных клетках, привлекает иммунные клетки и затем стимулирует превращение поддерживающих клеток в волокнообразующие клетки, откладывающие постоянную рубцовую ткань.
Как эта модель может ускорить разработку лучших терапий
Хотя ни одна мышь не может полностью воспроизвести человеческую жировую болезнь печени — которая часто развивается при ожирении с повышенным уровнем инсулина — усовершенствованная модель STAM захватывает критический аспект: усугубление повреждения печени, вызванное холестерином, в условиях выраженного диабета. Надёжно вызывая сильное воспаление и фиброз в определённые сроки, эта модель предоставляет более реалистичную площадку для испытаний экспериментальных препаратов, направленных на остановку или реверсию рубцевания. Проще говоря, исследование показывает, что по крайней мере в этой системе диетический холестерин не является невинным наблюдателем; он способствует переходу жировой печени к постоянному повреждению. Это понимание и улучшенная модель на его основе должны помочь исследователям быстрее выявлять те будущие терапии, которые с наибольшей вероятностью защитят человеческие печёночные клетки от долгосрочных последствий метаболических заболеваний.
Цитирование: Jonas, W., Gottmann, P., Jähnert, M. et al. Cholesterol-rich diet exacerbates steatohepatitis in the STAM mouse model. Sci Rep 16, 11231 (2026). https://doi.org/10.1038/s41598-026-45979-z
Ключевые слова: жировая болезнь печени, пищевой холестерин, фиброз печени, сахарный диабет 2 типа, мышиные модели заболеваний