Clear Sky Science · zh
c-MYC通过与启动子结合增强与1型糖尿病相关基因BATF3的转录
这项研究对家庭有何重要性
儿童1型糖尿病发生于免疫系统错误地破坏胰腺中产生胰岛素的细胞。胰岛素治疗能维持儿童生命,但不能治愈疾病或阻止长期并发症。该研究深入免疫细胞内部,探究促使它们发动攻击的原因,聚焦于两种称为c-MYC和BATF3的分子开关。通过绘制这些开关如何相互作用,研究者希望为疾病活动性的更好标志物提供线索,并最终指向更精确的治疗方法。
深入观察过度活跃的免疫“军队”
在1型糖尿病中,某些被称为T细胞的白细胞在损伤胰腺方面发挥核心作用。研究团队集中研究可直接杀伤其他细胞的子集——CD8 T细胞。早期小鼠研究提示,一种名为BATF3的蛋白有助于形成触发糖尿病的免疫细胞。在本研究中,科学家着眼于BATF3及其调控因子是否在患儿中发生改变。他们分析了儿童患者与健康同龄人的血液样本,并将这些测量与大型公共基因表达数据库结合起来。
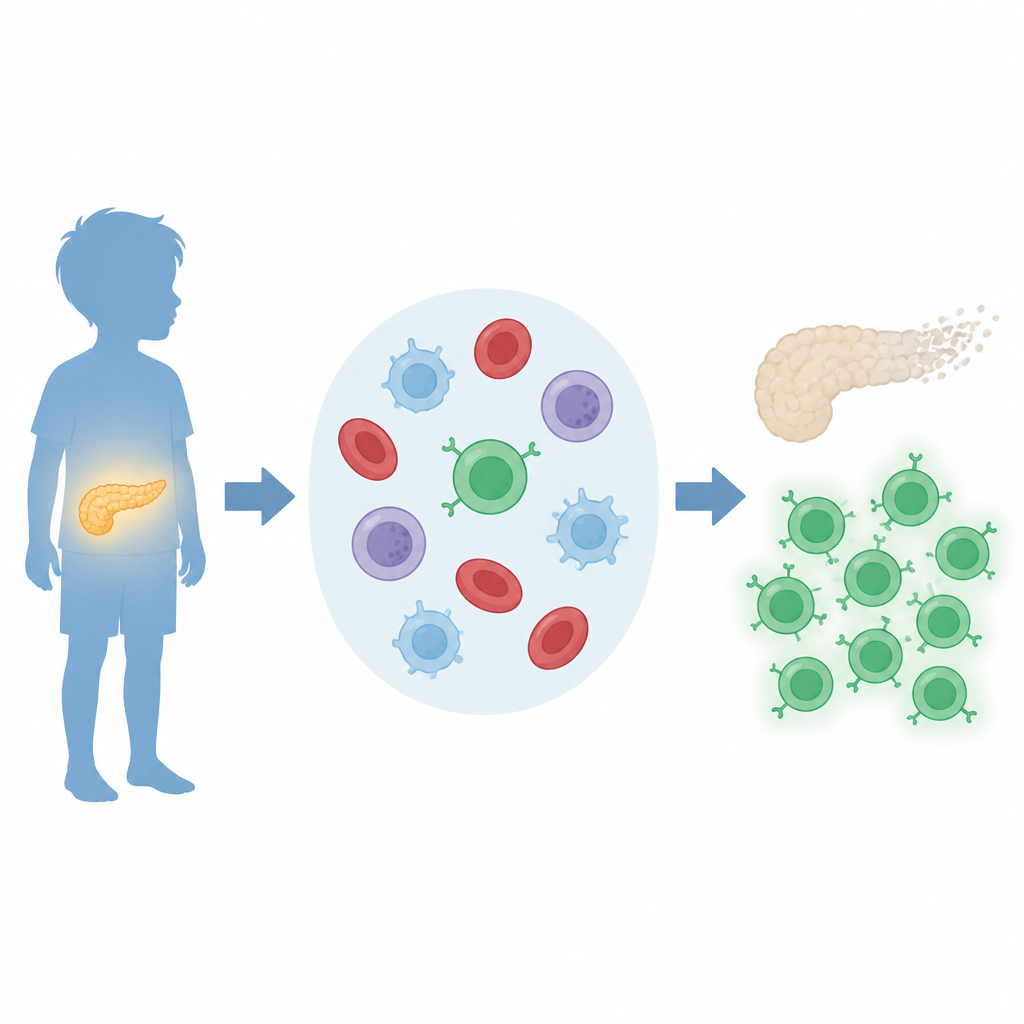
找到关键的分子开关
通过对数千个基因进行计算机筛选,研究者锁定了四个可能激活BATF3的调控因子。其中,c-MYC尤为显著。在来自1型糖尿病儿童的血液免疫细胞中,c-MYC和BATF3的水平均高于健康儿童,而另一个候选因子EGR1则降低。这些模式表明,c-MYC到BATF3的一条链在受影响儿童的免疫系统中处于活跃状态,可能反映了他们持续的自身免疫反应。
c-MYC如何上调BATF3
为检验c-MYC是否真正控制BATF3,团队进行了细胞培养实验。他们将额外的c-MYC基因拷贝导入常用的人肾细胞系并观察结果。当c-MYC水平升高时,BATF3在RNA和蛋白水平上也随之上升。当用小干扰RNA降低c-MYC时,BATF3下降。科学家随后检查了BATF3基因的控制区,显示c-MYC与一段位于BATF3起始读取位点上游约1.2千碱基的特定DNA序列结合,像是在分子层面按下一个开关。
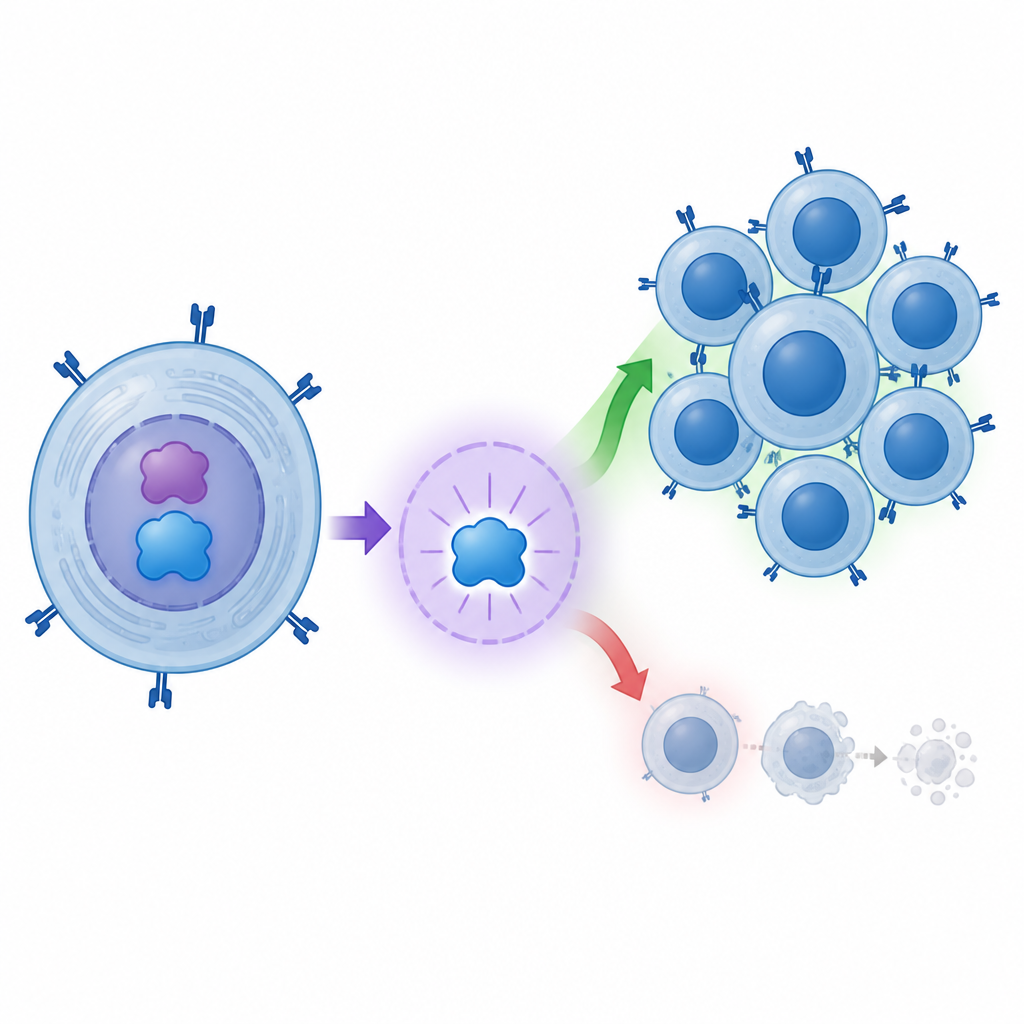
对杀伤性T细胞的影响
事情并不仅限于分子层面。研究组还研究了从血液培养而来的人体CD8 T细胞。当他们在这些细胞中增强c-MYC时,细胞分裂增多且凋亡减少。换言之,c-MYC有助于扩增潜在有害的T细胞库。由于BATF3是c-MYC激活的主要靶点之一,这项工作描绘出一条从c-MYC到BATF3再到更强、更持久的CD8 T细胞的链路。这与持续且具有攻击性的免疫反应促使儿童胰岛素产生细胞丧失的观点相一致。
对未来护理的意义
作者总结认为,过度活跃的c-MYC–BATF3通路很可能是驱动儿童1型糖尿病的机制的一部分。他们的数据尚不能证明阻断该通路会停止疾病进展,且直接抑制c-MYC可能不安全,因为c-MYC对许多正常过程至关重要。尽管如此,在血液中测量c-MYC和BATF3的活性可能有助于追踪疾病进展或评估儿童对新型免疫疗法的反应。从长远看,针对该通路周边步骤而非直接靶向这些开关,可能为在保留免疫系统重要防御功能的同时驯服其异常反应提供新策略。
引用: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
关键词: 1型糖尿病, c-MYC, BATF3, CD8 T细胞, 自身免疫