Clear Sky Science · fr
c-MYC augmente la transcription du gène associé au diabète de type 1 BATF3 via la liaison au promoteur
Pourquoi cette recherche compte pour les familles
Le diabète de type 1 chez l’enfant survient lorsque le système immunitaire détruit par erreur les cellules productrices d’insuline du pancréas. Le traitement par insuline maintient les enfants en vie mais ne guérit pas la maladie ni n’empêche les complications à long terme. Cette étude pénètre à l’intérieur des cellules immunitaires pour comprendre ce qui les pousse à attaquer, en se focalisant sur une paire de « commutateurs » moléculaires appelés c-MYC et BATF3. En cartographiant l’interaction de ces commutateurs, les chercheurs espèrent identifier de meilleurs marqueurs de l’activité de la maladie et, à terme, des traitements plus précis.
Un examen approfondi d’une armée immunitaire hyperactive
Dans le diabète de type 1, certains globules blancs appelés lymphocytes T jouent un rôle central dans l’atteinte du pancréas. L’équipe s’est concentrée sur les lymphocytes T CD8, un sous-groupe capable de tuer directement d’autres cellules. Des travaux antérieurs chez la souris suggéraient qu’une protéine nommée BATF3 contribue à façonner des cellules immunitaires qui déclenchent le diabète. Ici, les scientifiques ont cherché à savoir si BATF3, et les facteurs qui le contrôlent, sont altérés chez des enfants atteints. Ils ont analysé des échantillons de sang de jeunes patients et de pairs sains, et combiné ces mesures avec de larges bases de données publiques d’expression génique.
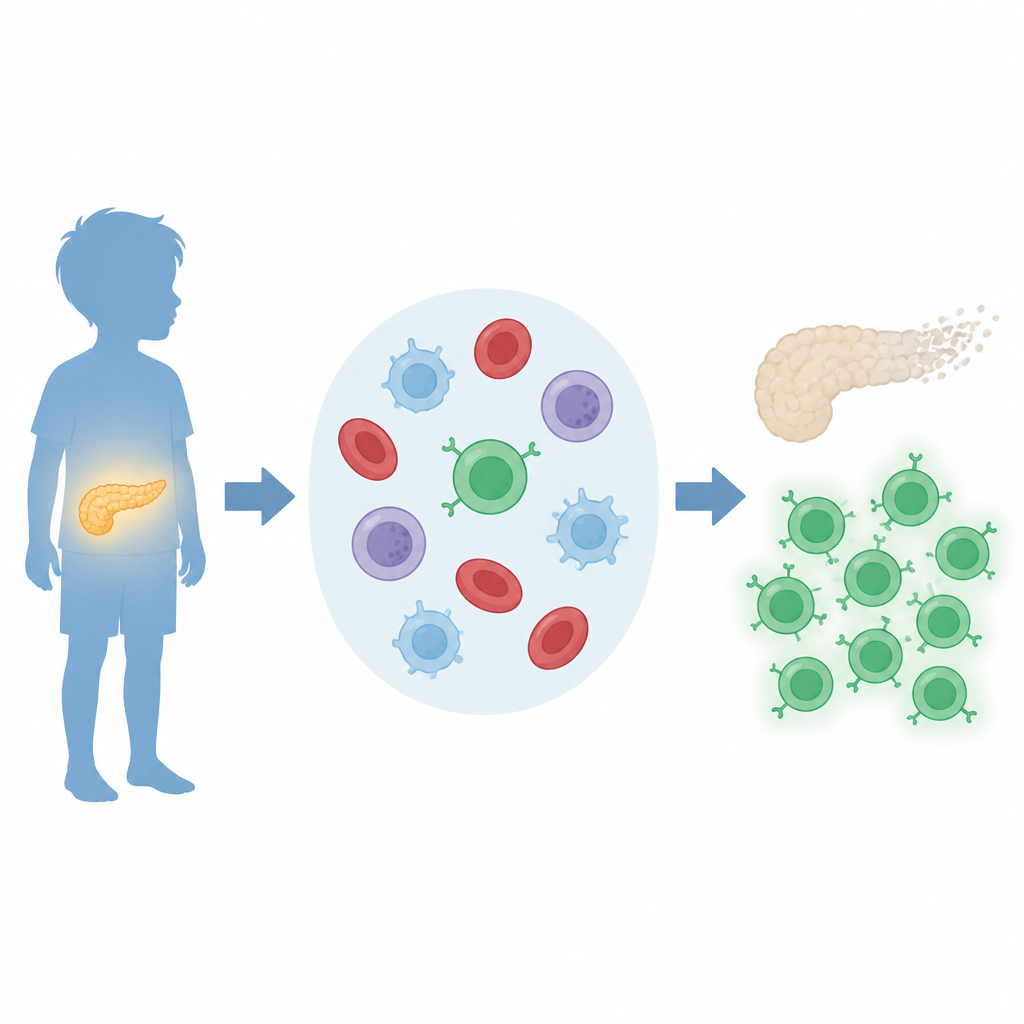
Identification des principaux commutateurs moléculaires
Grâce à un criblage informatique de milliers de gènes, les chercheurs ont retenu quatre régulateurs potentiels susceptibles d’activer BATF3. Parmi eux, c-MYC s’est distingué. c-MYC et BATF3 présentaient des niveaux plus élevés dans les cellules immunitaires sanguines d’enfants atteints de diabète de type 1 que chez les enfants sains, tandis qu’un autre candidat, EGR1, était réduit. Ces profils suggèrent qu’une chaîne d’événements allant de c-MYC à BATF3 est active dans le système immunitaire des enfants concernés et pourrait refléter leur réponse auto-immune en cours.
Comment c-MYC augmente BATF3
Pour vérifier si c-MYC contrôle réellement BATF3, l’équipe a réalisé des expériences en culture cellulaire. Ils ont introduit des copies supplémentaires du gène c-MYC dans des cellules rénales humaines couramment utilisées en laboratoire et observé les conséquences. Lorsque les niveaux de c-MYC augmentaient, ceux de BATF3 augmentaient aussi, tant au niveau de l’ARN que de la protéine. Lorsque c-MYC était réduit par ARN interférent, BATF3 diminuait. Les scientifiques ont ensuite examiné la région de contrôle du gène BATF3 et montré que c-MYC se lie à une séquence d’ADN spécifique située à environ 1,2 kilobases en amont du site de lecture de BATF3, agissant comme un doigt appuyant sur un interrupteur moléculaire.
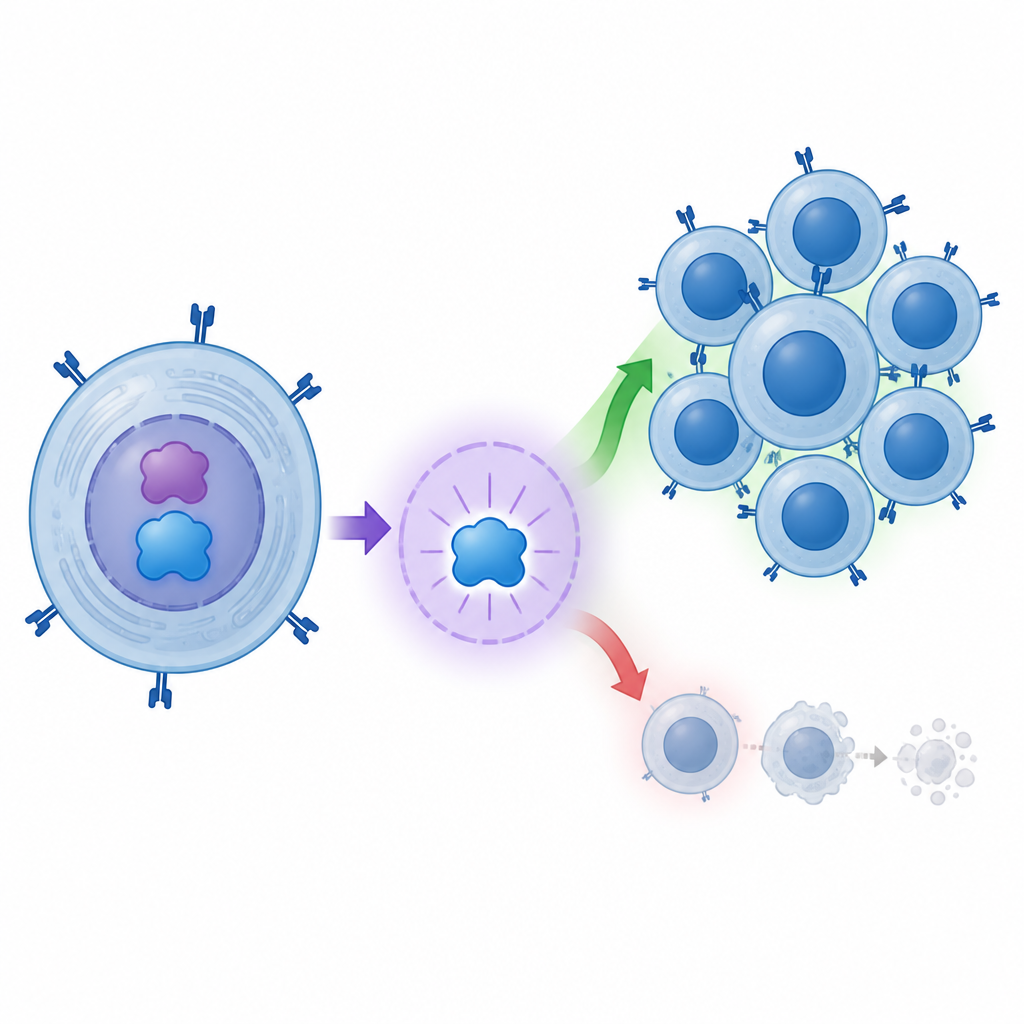
Impact sur les lymphocytes T cytotoxiques
L’histoire ne s’arrête pas aux molécules. Le groupe a également étudié des lymphocytes T CD8 humains cultivés à partir de sang. Lorsqu’ils ont augmenté c-MYC dans ces cellules, celles-ci se sont divisées davantage et sont mortes moins souvent. Autrement dit, c-MYC a contribué à élargir le réservoir de lymphocytes potentiellement nuisibles. Comme BATF3 est l’une des principales cibles activées par c-MYC, ce travail décrit une chaîne allant de c-MYC à BATF3 qui conduit à des lymphocytes CD8 plus puissants et de plus longue durée de vie. Cela corrobore l’idée qu’une attaque immunitaire soutenue et agressive favorise la perte des cellules productrices d’insuline chez les enfants atteints de diabète de type 1.
Ce que cela signifie pour les soins futurs
Les auteurs concluent qu’une voie c-MYC–BATF3 hyperactive fait probablement partie du mécanisme alimentant le diabète de type 1 chez l’enfant. Leurs données ne prouvent pas encore que bloquer cette voie arrêtera la maladie, et inhiber directement c-MYC pourrait être dangereux car il est essentiel à de nombreux processus normaux. Néanmoins, mesurer l’activité de c-MYC et de BATF3 dans le sang pourrait aider à suivre l’évolution de la maladie ou la réponse d’un enfant à de nouvelles thérapies immunitaires. À plus long terme, cibler des étapes autour de cette voie, plutôt que les commutateurs eux-mêmes, pourrait offrir de nouvelles stratégies pour apaiser le système immunitaire tout en préservant ses fonctions protectrices vitales.
Citation: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
Mots-clés: diabète de type 1, c-MYC, BATF3, lymphocytes T CD8, auto-immunité