Clear Sky Science · de
c-MYC erhöht die Transkription des mit Typ‑1‑Diabetes assoziierten Gens BATF3 durch Promotorbindung
Warum diese Forschung für Familien wichtig ist
Typ‑1‑Diabetes bei Kindern entsteht, wenn das Immunsystem irrtümlich die insulinproduzierenden Zellen der Bauchspeicheldrüse zerstört. Insulintherapie erhält das Leben der Kinder, heilt die Krankheit aber nicht und verhindert nicht alle langfristigen Komplikationen. Diese Studie blickt in Immunzellen hinein, um zu verstehen, was sie zum Angriff treibt, und konzentriert sich auf ein Paar molekularer Schalter namens c‑MYC und BATF3. Indem die Forschenden aufzeichnen, wie diese Schalter miteinander interagieren, hoffen sie, Hinweise auf bessere Marker für Krankheitsaktivität und letztlich präzisere Therapien zu liefern.
Ein genauerer Blick auf eine überaktive Immunarmee
Beim Typ‑1‑Diabetes spielen bestimmte weiße Blutkörperchen, die T‑Zellen, eine zentrale Rolle bei der Schädigung der Bauchspeicheldrüse. Das Team konzentrierte sich auf CD8‑T‑Zellen, eine Untergruppe, die andere Zellen direkt töten kann. Frühere Arbeiten an Mäusen deuteten darauf hin, dass das Protein BATF3 Immunzellen formt, die Diabetes auslösen. Hier fragten die Wissenschaftler, ob BATF3 und die Faktoren, die es steuern, bei Kindern mit der Erkrankung verändert sind. Sie analysierten Blutproben von jungen Patientinnen und Patienten sowie gesunden Altersgenossen und kombinierten diese Messwerte mit großen öffentlichen Genexpressionsdatenbanken.
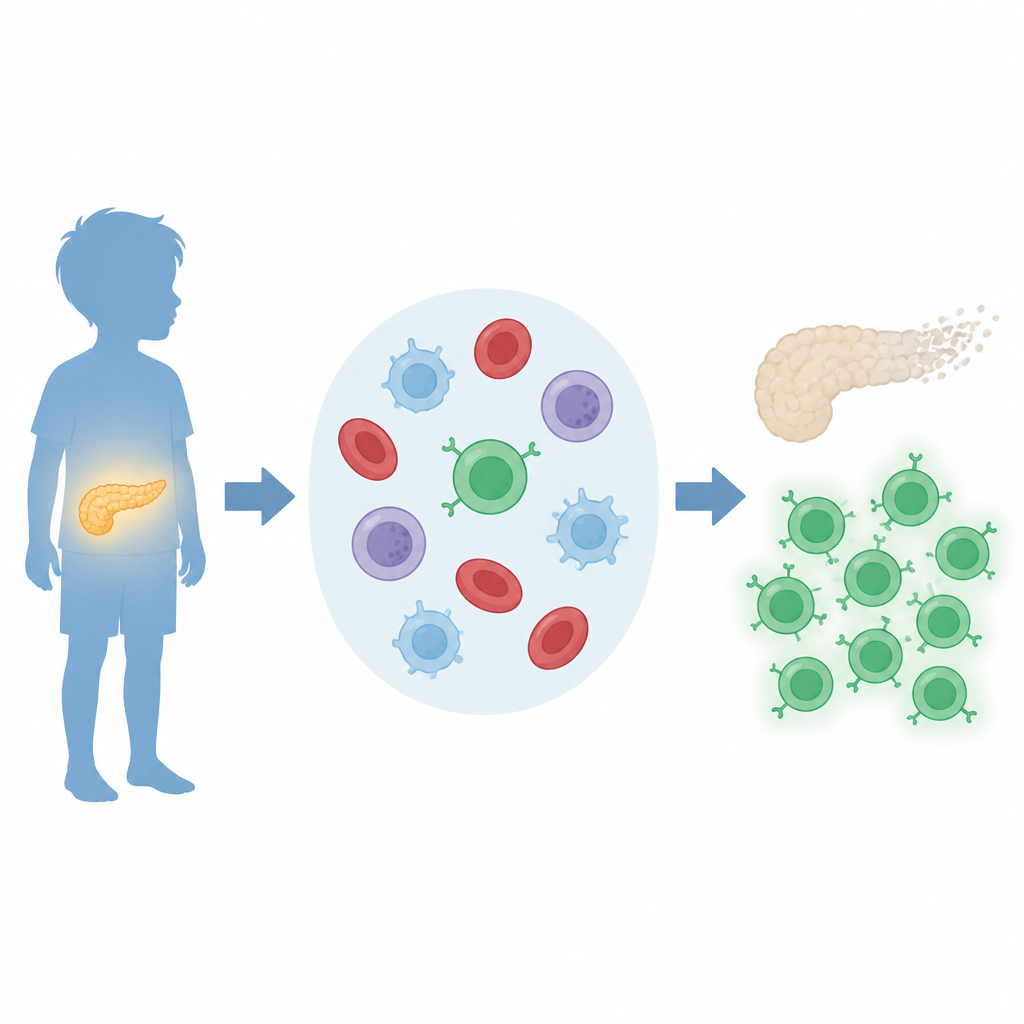
Die Suche nach den entscheidenden molekularen Schaltern
Durch computergestützte Durchsicht von Tausenden Genen grenzten die Forschenden vier potenzielle Regulatoren ein, die BATF3 anschalten könnten. Unter diesen stach c‑MYC hervor. Sowohl c‑MYC als auch BATF3 waren in Immunzellen aus dem Blut von Kindern mit Typ‑1‑Diabetes stärker ausgeprägt als bei gesunden Kindern, während ein anderer Kandidat, EGR1, vermindert war. Diese Muster legen nahe, dass eine c‑MYC‑zu‑BATF3‑Abfolge im Immunsystem betroffener Kinder aktiv ist und möglicherweise deren anhaltende Autoimmunreaktion widerspiegelt.
Wie c‑MYC BATF3 hochreguliert
Um zu testen, ob c‑MYC tatsächlich BATF3 kontrolliert, führten die Forschenden Zellkulturversuche durch. Sie setzten zusätzliche Kopien des c‑MYC‑Gens in menschliche Nierenzellen ein, die im Labor häufig verwendet werden, und beobachteten die Folgen. Steigende c‑MYC‑Werte führten zu erhöhten BATF3‑Werten, sowohl auf RNA‑ als auch auf Proteinebene. Wurde c‑MYC mit kleinen interferierenden RNAs heruntergeregelt, nahm BATF3 ab. Die Wissenschaftler untersuchten dann die Kontrollregion des BATF3‑Gens und zeigten, dass c‑MYC an eine spezifische DNA‑Strecke etwa 1,2 Tausend Basen stromaufwärts des Transkriptionsstarts von BATF3 bindet und dort wie ein Finger auf einen molekularen Lichtschalter wirkt.
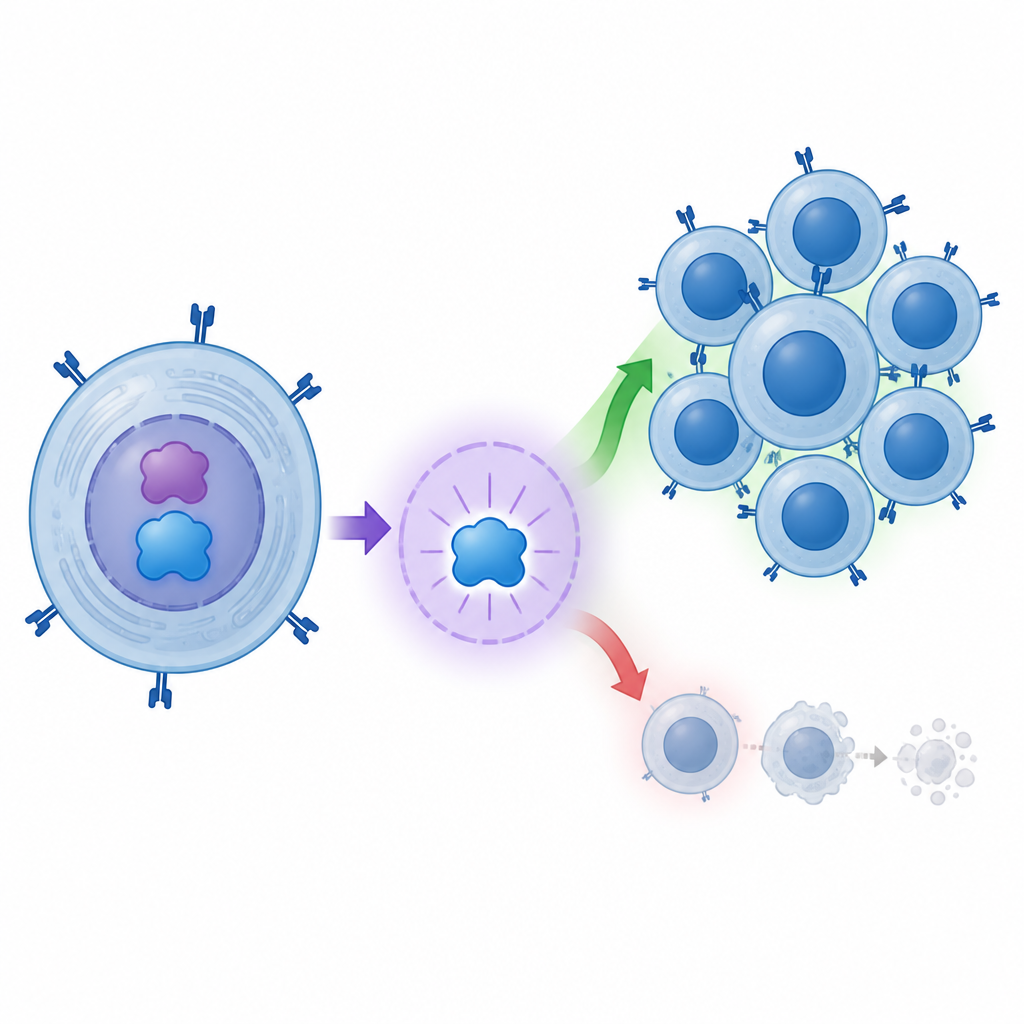
Auswirkung auf Killer‑T‑Zellen
Die Geschichte endet nicht bei den Molekülen. Die Gruppe untersuchte auch aus Blut gewonnene menschliche CD8‑T‑Zellen. Als sie c‑MYC in diesen Zellen verstärkten, teilten sich die Zellen häufiger und starben seltener. Anders gesagt, c‑MYC half, den Pool potenziell schädlicher T‑Zellen zu vergrößern. Da BATF3 eines der Hauptziele ist, die c‑MYC aktiviert, skizziert die Arbeit eine Kette von c‑MYC über BATF3 hin zu kräftigeren, langlebigeren CD8‑T‑Zellen. Das passt zu der Vorstellung, dass ein anhaltend aggressiver Immunangriff zum Verlust der insulinproduzierenden Zellen bei Kindern mit Typ‑1‑Diabetes beiträgt.
Was das für die künftige Versorgung bedeutet
Die Autorinnen und Autoren schließen daraus, dass ein überaktiver c‑MYC–BATF3‑Weg wahrscheinlich Teil der Maschinerie ist, die Typ‑1‑Diabetes bei Kindern antreibt. Ihre Daten beweisen noch nicht, dass das Blockieren dieses Wegs die Krankheit stoppt, und das direkte Abschalten von c‑MYC könnte riskant sein, da es für viele normale Prozesse wichtig ist. Dennoch könnte die Messung der c‑MYC‑ und BATF3‑Aktivität im Blut dabei helfen, den Verlauf der Erkrankung oder die Reaktion eines Kindes auf neue Immuntherapien zu verfolgen. Langfristig könnten gezielte Eingriffe in Schritte entlang dieses Wegs — statt an den Schaltern selbst — neue Strategien bieten, das Immunsystem zu dämpfen und gleichzeitig seine lebenswichtigen Schutzfunktionen zu bewahren.
Zitation: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
Schlüsselwörter: Typ‑1‑Diabetes, c‑MYC, BATF3, CD8‑T‑Zellen, Autoimmunität