Clear Sky Science · ja
c-MYCはプロモーター結合を介して1型糖尿病関連遺伝子BATF3の転写を促進する
この研究が家族にとって重要な理由
小児の1型糖尿病は、免疫系が誤って膵臓のインスリン産生細胞を破壊することで発症します。インスリン療法は子どもの命を守りますが、病気を治すわけではなく長期的合併症を止めることもできません。本研究は免疫細胞の内部に入り込み、何がそれらを攻撃に駆り立てるのかを解明しようとしています。焦点はc-MYCとBATF3という一対の分子スイッチにあり、これらの相互作用をマッピングすることで、病勢のより良いマーカーや、いずれはより精密な治療法への手がかりを示すことを目指しています。
過剰に活性化した免疫軍の詳しい観察
1型糖尿病では、T細胞として知られる一部の白血球が膵臓に対する主要な損傷因子となります。研究チームは、他の細胞を直接殺傷しうるサブセットであるCD8 T細胞に注目しました。以前のマウス研究は、BATF3というタンパク質が糖尿病を引き起こす免疫細胞の性質形成に関与することを示唆していました。本研究では、BATF3とそれを制御する因子が小児の患者で変化しているかを検証しました。研究者らは患者と健常者の若年者から採血し、これらの測定を公的な大規模遺伝子発現データベースと組み合わせて解析しました。
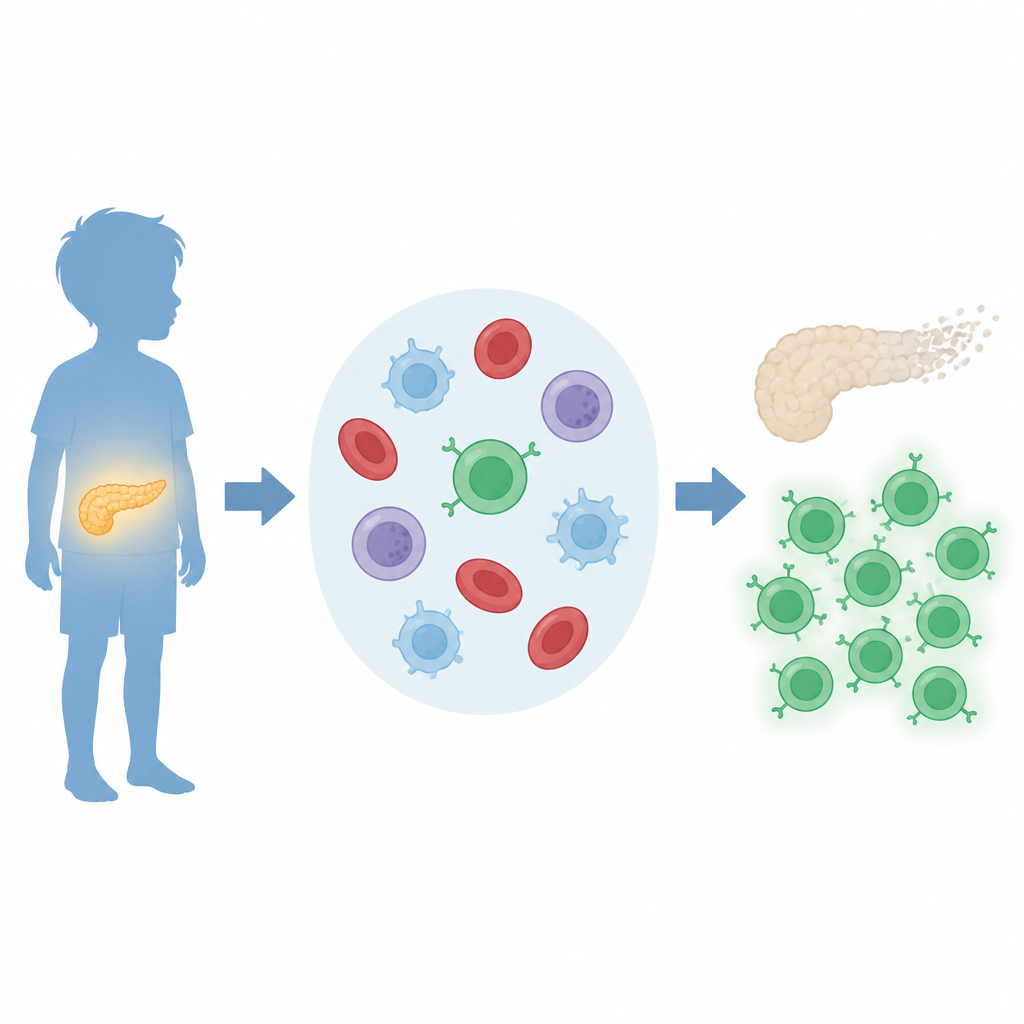
鍵となる分子スイッチの発見
数千の遺伝子をコンピュータでスクリーニングした結果、研究者らはBATF3をONにする可能性のある4つの候補調節因子に絞り込みました。その中でc-MYCが際立っていました。c-MYCとBATF3の両方は、小児の1型糖尿病患者の血中免疫細胞で健常者より高いレベルで存在しており、別の候補であるEGR1は低下していました。これらのパターンは、c-MYCからBATF3への一連の事象が罹患者の免疫系で活発であり、進行中の自己免疫反応を反映している可能性を示唆します。
c-MYCがBATF3をどのように上げるか
c-MYCが実際にBATF3を制御しているかを確かめるため、研究チームは細胞培養実験を行いました。一般的にラボで用いられるヒト腎臓由来細胞にc-MYC遺伝子を余分に導入して経過を観察しました。c-MYCのレベルが上がると、RNAとタンパク質の両段階でBATF3のレベルも上昇しました。逆に、小干渉RNAでc-MYCを抑えるとBATF3は低下しました。さらにBATF3遺伝子の制御領域を調べ、c-MYCがBATF3の読み取り開始点の約1.2キロ塩基上流の特定領域に結合し、分子的なスイッチに指を当てるように作用することを示しました。
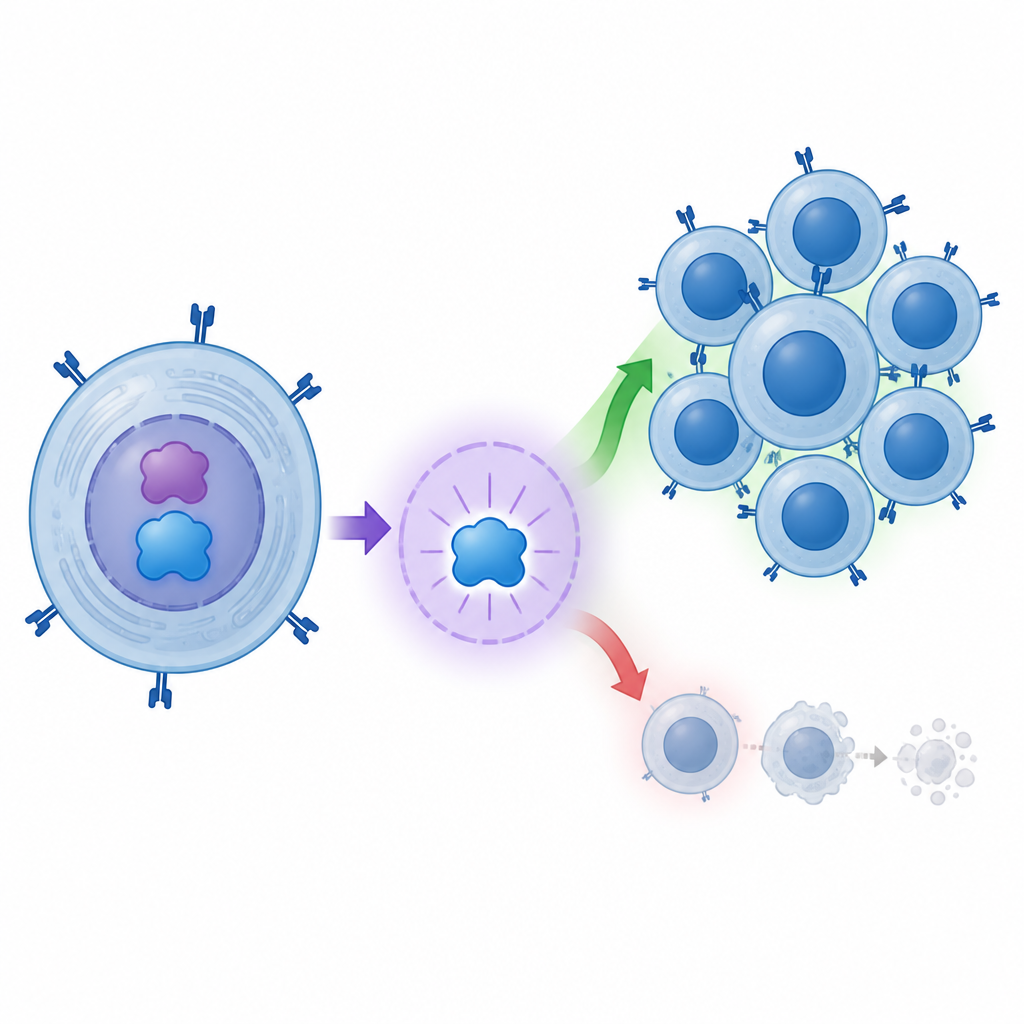
キラーT細胞への影響
話は分子で終わりません。研究グループは血液から培養したヒトCD8 T細胞も解析しました。これらの細胞でc-MYCを増強すると、細胞分裂が増え細胞死が減少しました。言い換えれば、c-MYCは潜在的に有害なT細胞のプールを拡大するのに寄与しました。BATF3がc-MYCの主要な標的の一つであることから、本研究はc-MYC→BATF3→より強力で長命なCD8 T細胞へと続く一連の流れを描きます。これは持続的で攻撃的な免疫応答が小児のインスリン産生細胞の喪失を促進するという考えと整合します。
将来のケアへの意味
著者らは、過剰に活性化したc-MYC–BATF3経路が小児の1型糖尿病を駆動するメカニズムの一部である可能性が高いと結論づけています。現時点のデータはこの経路を阻害すれば病気が止まることを証明するものではなく、c-MYC自体を直接遮断することは多くの正常なプロセスに重要であるため安全性の問題が生じ得ます。とはいえ、血中のc-MYCやBATF3の活性を測定することは、病態の進行や子どもが新しい免疫療法にどのように反応しているかを追跡する手段となり得ます。長期的には、この経路そのものではなく経路を取り巻く段階を標的にすることで、免疫系の重要な防御機能を温存しながら過剰な攻撃性を抑える新たな戦略が開ける可能性があります。
引用: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
キーワード: 1型糖尿病, c-MYC, BATF3, CD8 T細胞, 自己免疫