Clear Sky Science · it
c-MYC aumenta la trascrizione del gene associato al diabete mellito di tipo 1 BATF3 tramite legame al promotore
Perché questa ricerca è importante per le famiglie
Il diabete di tipo 1 nei bambini insorge quando il sistema immunitario distrugge per errore le cellule produttrici di insulina del pancreas. La terapia insulinica mantiene i bambini in vita ma non guarisce la malattia né impedisce le complicanze a lungo termine. Questo studio esamina l’interno delle cellule immunitarie per comprendere cosa le spinge ad attaccare, concentrandosi su una coppia di interruttori molecolari chiamati c-MYC e BATF3. Mappando come questi interruttori interagiscono, i ricercatori sperano di indicare la strada verso marcatori migliori dell’attività della malattia e, col tempo, trattamenti più mirati.
Uno sguardo più vicino a un esercito immunitario iperattivo
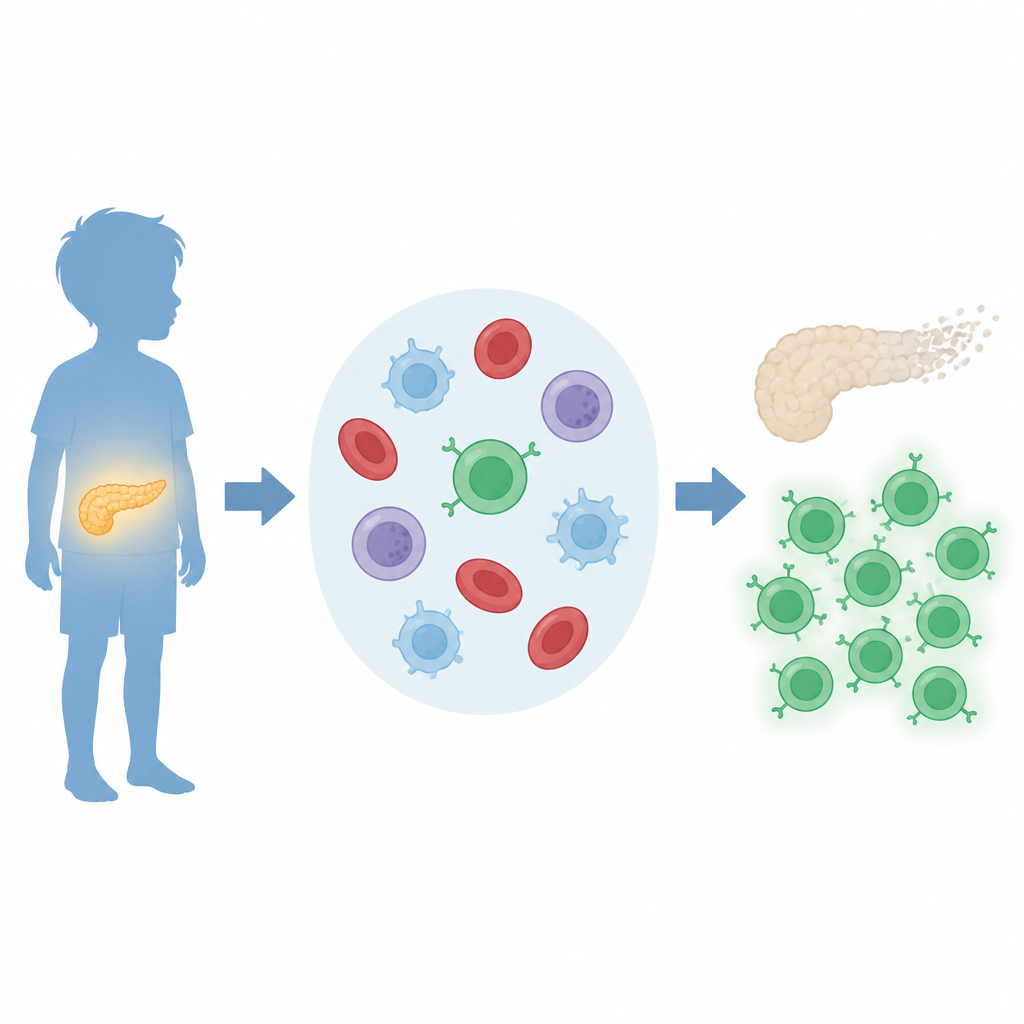
Nel diabete di tipo 1, alcune cellule bianche del sangue note come cellule T svolgono un ruolo centrale nel danneggiare il pancreas. Il gruppo si è concentrato sulle cellule T CD8, un sottogruppo in grado di uccidere direttamente altre cellule. Studi precedenti nei topi suggerivano che una proteina chiamata BATF3 contribuisce a plasmare le cellule immunitarie che scatenano il diabete. In questo lavoro, gli scienziati hanno chiesto se BATF3 e i fattori che lo regolano siano alterati nei bambini con la malattia. Hanno analizzato campioni di sangue di giovani pazienti e coetanei sani, e hanno integrato queste misurazioni con grandi database pubblici di espressione genica.
Identificare gli interruttori molecolari chiave
Usando screening al computer su migliaia di geni, i ricercatori hanno ristretto a quattro i regolatori potenziali in grado di attivare BATF3. Tra questi, c-MYC è emerso come rilevante. Sia c-MYC sia BATF3 risultavano espressi a livelli più alti nelle cellule immunitarie del sangue di bambini con diabete di tipo 1 rispetto ai coetanei sani, mentre un altro candidato, EGR1, era ridotto. Questi schemi suggeriscono che una catena di eventi c-MYC→BATF3 sia attiva nei sistemi immunitari dei bambini colpiti e possa riflettere la loro risposta autoimmune in corso.
Come c-MYC aumenta BATF3
Per verificare se c-MYC controlla effettivamente BATF3, il gruppo ha eseguito esperimenti in colture cellulari. Hanno inserito copie aggiuntive del gene c-MYC in cellule renali umane comunemente usate in laboratorio e osservato cosa accadeva. Quando i livelli di c-MYC aumentavano, aumentavano anche i livelli di BATF3, sia a livello di RNA sia di proteina. Quando c-MYC veniva ridotto tramite RNA interferente, BATF3 diminuiva. Gli scienziati hanno poi esaminato la regione di controllo del gene BATF3 e hanno dimostrato che c-MYC si lega a un tratto specifico di DNA circa 1,2 kilobasi a monte del sito di trascrizione di BATF3, agendo come un dito che preme un interruttore molecolare.
Impatto sulle cellule T citotossiche
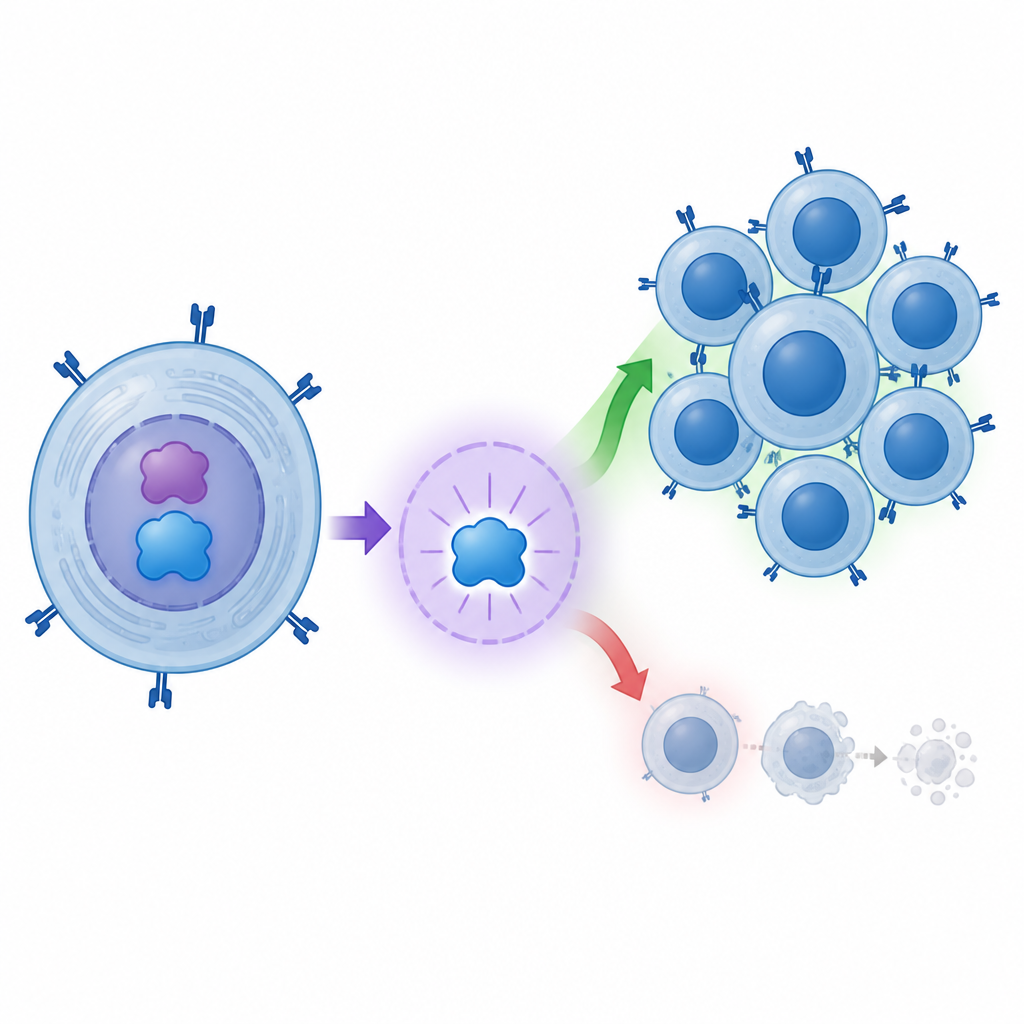
La storia non si ferma alle molecole. Il gruppo ha anche studiato cellule T CD8 umane coltivate a partire dal sangue. Quando hanno aumentato c-MYC in queste cellule, esse si sono divise maggiormente e sono morte meno spesso. In altre parole, c-MYC ha contribuito ad espandere il pool di potenziali cellule T dannose. Poiché BATF3 è uno dei principali bersagli attivati da c-MYC, il lavoro descrive una catena che va da c-MYC a BATF3 verso cellule T CD8 più robuste e di vita più lunga. Questo si allinea con l’idea che un attacco immunitario sostenuto e aggressivo favorisca la perdita delle cellule produttrici di insulina nei bambini con diabete di tipo 1.
Cosa significa per le cure future
Gli autori concludono che una via c-MYC–BATF3 iperattiva è probabilmente parte della macchina che alimenta il diabete di tipo 1 nei bambini. I loro dati non dimostrano ancora che bloccare questa via possa fermare la malattia, e inibire direttamente c-MYC potrebbe essere pericoloso perché è importante per molti processi normali. Tuttavia, misurare l’attività di c-MYC e BATF3 nel sangue potrebbe aiutare a monitorare l’evoluzione della malattia o la risposta di un bambino a nuove terapie immunitarie. A più lungo termine, mirare ai passaggi attorno a questa via, piuttosto che agli interruttori stessi, potrebbe offrire nuove strategie per contenere il sistema immunitario preservandone i ruoli protettivi essenziali.
Citazione: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
Parole chiave: diabete di tipo 1, c-MYC, BATF3, cellule T CD8, autoimmunità