Clear Sky Science · pl
c-MYC zwiększa transkrypcję genu związanego z cukrzycą typu 1, BATF3, poprzez wiązanie z promotorem
Dlaczego te badania mają znaczenie dla rodzin
Cukrzyca typu 1 u dzieci powstaje, gdy układ odpornościowy omyłkowo niszczy komórki trzustki produkujące insulinę. Terapia insulinowa pozwala dzieciom przeżyć, ale nie leczy choroby ani nie zatrzymuje długoterminowych powikłań. W tym badaniu przyjrzano się wnętrzu komórek odpornościowych, aby zrozumieć, co napędza ich atak, ze szczególnym uwzględnieniem pary molekularnych przełączników: c-MYC i BATF3. Mapując interakcje między nimi, badacze mają nadzieję wskazać lepsze markery aktywności choroby i w przyszłości bardziej precyzyjne terapie.
Uważniejsze spojrzenie na nadaktywne wojsko odpornościowe
W cukrzycy typu 1 centralną rolę odgrywają niektóre białe krwinki zwane limfocytami T. Zespół skupił się na limfocytach CD8, podzbiorze zdolnym do bezpośredniego zabijania innych komórek. Wcześniejsze prace na myszach sugerowały, że białko BATF3 pomaga kształtować komórki odpornościowe wywołujące cukrzycę. W tym badaniu naukowcy pytali, czy BATF3 i czynniki go kontrolujące są zmienione u dzieci z chorobą. Przeanalizowali próbki krwi od młodych pacjentów i zdrowych rówieśników oraz połączyli te pomiary z dużymi publicznymi bazami danych ekspresji genów.
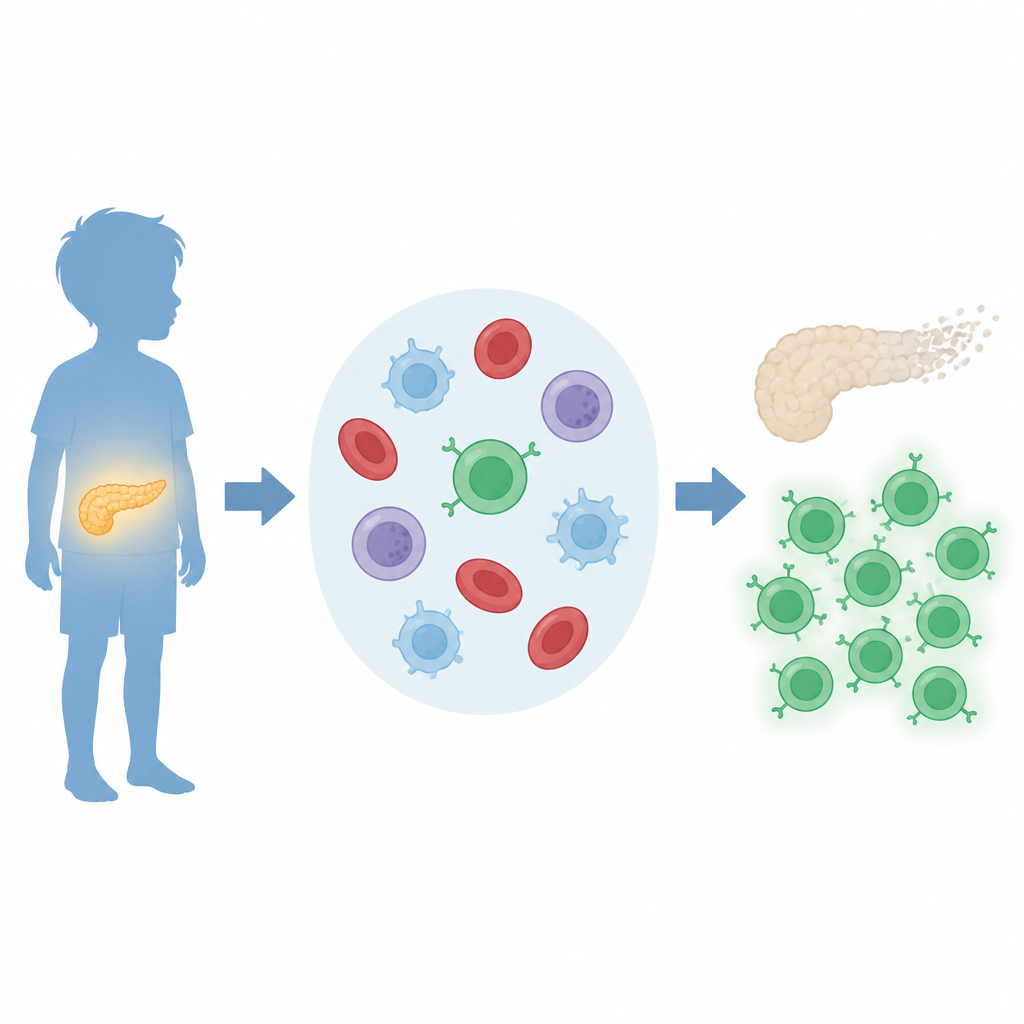
Znajdowanie kluczowych przełączników molekularnych
Wykorzystując komputerowe przesiewanie tysięcy genów, badacze zawęzili listę do czterech potencjalnych regulatorów mogących włączać BATF3. Spośród nich wyróżniał się c-MYC. Zarówno c-MYC, jak i BATF3 występowały na wyższych poziomach w komórkach odpornościowych krwi dzieci z cukrzycą typu 1 niż u zdrowych dzieci, podczas gdy inny kandydat, EGR1, był obniżony. Te wzorce sugerują, że ciąg zdarzeń od c-MYC do BATF3 jest aktywny w układach odpornościowych chorych dzieci i może odzwierciedlać ich trwającą odpowiedź autoimmunologiczną.
W jaki sposób c-MYC zwiększa BATF3
Aby sprawdzić, czy c-MYC faktycznie kontroluje BATF3, zespół przeprowadził eksperymenty na hodowlach komórkowych. Wprowadzili dodatkowe kopie genu c-MYC do ludzkich komórek nerkowych powszechnie używanych w laboratorium i obserwowali efekty. Gdy poziomy c-MYC wzrastały, poziomy BATF3 rosły równocześnie, zarówno na etapie RNA, jak i białka. Gdy c-MYC obniżano za pomocą małego interferującego RNA, BATF3 spadał. Naukowcy zbadali następnie region kontrolny genu BATF3 i pokazali, że c-MYC wiąże się ze specyficznym odcinkiem DNA około 1,2 tysiąca par zasad w górę od miejsca rozpoczęcia transkrypcji BATF3, działając jak palec naciskający molekularny wyłącznik światła.
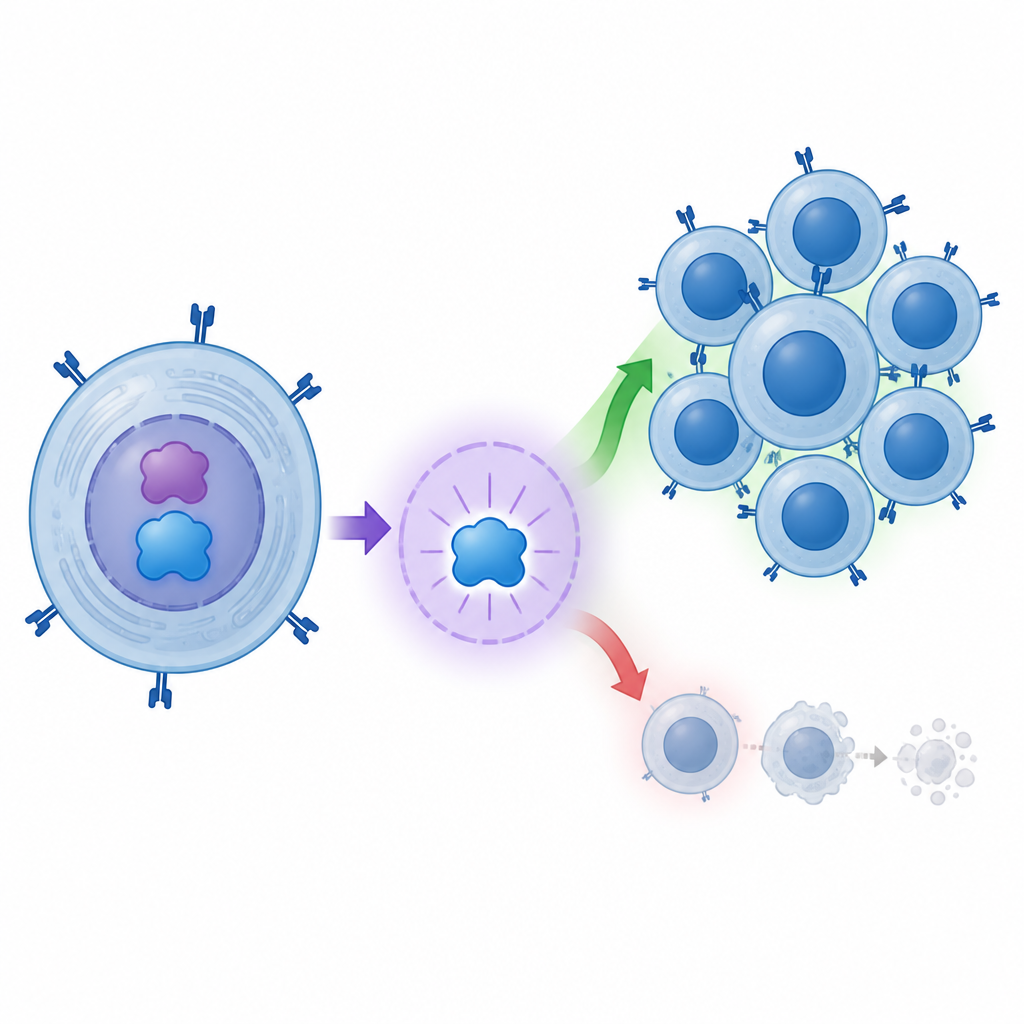
Wpływ na zabójcze limfocyty T
Historia nie kończy się na cząsteczkach. Zespół badał także ludzkie limfocyty CD8 hodowane z krwi. Gdy zwiększano poziom c-MYC w tych komórkach, dzieliły się one częściej i rzadziej umierały. Innymi słowy, c-MYC pomagał powiększyć pulę potencjalnie szkodliwych komórek T. Ponieważ BATF3 jest jednym z głównych celów aktywowanych przez c-MYC, praca układa łańcuch od c-MYC przez BATF3 do bardziej aktywnych, dłużej żyjących limfocytów CD8. Zgodne jest to z koncepcją, że utrzymujący się, agresywny atak immunologiczny przyczynia się do utraty komórek produkujących insulinę u dzieci z cukrzycą typu 1.
Co to oznacza dla przyszłej opieki
Autorzy wnioskują, że nadaktywna ścieżka c-MYC–BATF3 jest prawdopodobnie częścią mechanizmu napędzającego cukrzycę typu 1 u dzieci. Ich dane nie dowodzą jeszcze, że zablokowanie tej ścieżki zatrzyma chorobę, a bezpośrednie wyłączenie c-MYC mogłoby być niebezpieczne, ponieważ uczestniczy on w wielu normalnych procesach. Mimo to mierzenie aktywności c-MYC i BATF3 we krwi może pomóc śledzić przebieg choroby lub odpowiedź dziecka na nowe terapie immunologiczne. W dłuższej perspektywie celowanie w etapy otaczające tę ścieżkę, zamiast samych przełączników, mogłoby zaoferować nowe strategie stłumienia układu odpornościowego przy zachowaniu jego istotnych funkcji ochronnych.
Cytowanie: Zhao, Y., Tang, Z., Tao, Y. et al. c-MYC enhances transcription of the type 1 diabetes mellitus associated gene BATF3 via promoter binding. Sci Rep 16, 14976 (2026). https://doi.org/10.1038/s41598-026-45579-x
Słowa kluczowe: cukrzyca typu 1, c-MYC, BATF3, limfocyty CD8, autoimmunizacja