Clear Sky Science · zh
TRIM29促进肺腺癌的上皮–间质转化、血管生成与基质重塑:在组织学、转录组与蛋白水平的整合验证
这项肺癌研究为何重要
肺癌仍然是癌症死亡的主要原因之一,许多患者无法从现有的靶向药物或免疫疗法中获益。本研究关注一种鲜为人知的蛋白质TRIM29,并提出一个关键问题:它是否助长了肺肿瘤变得更具侵袭性、更难以治疗?通过整合基因数据、真实肿瘤的显微镜图像、细胞实验和药物筛选,研究人员表明TRIM29不仅是一个标记,而且可能推动肺腺癌——这一最常见的肺癌类型——向更危险的表型发展。
肿瘤扩散的隐秘帮手
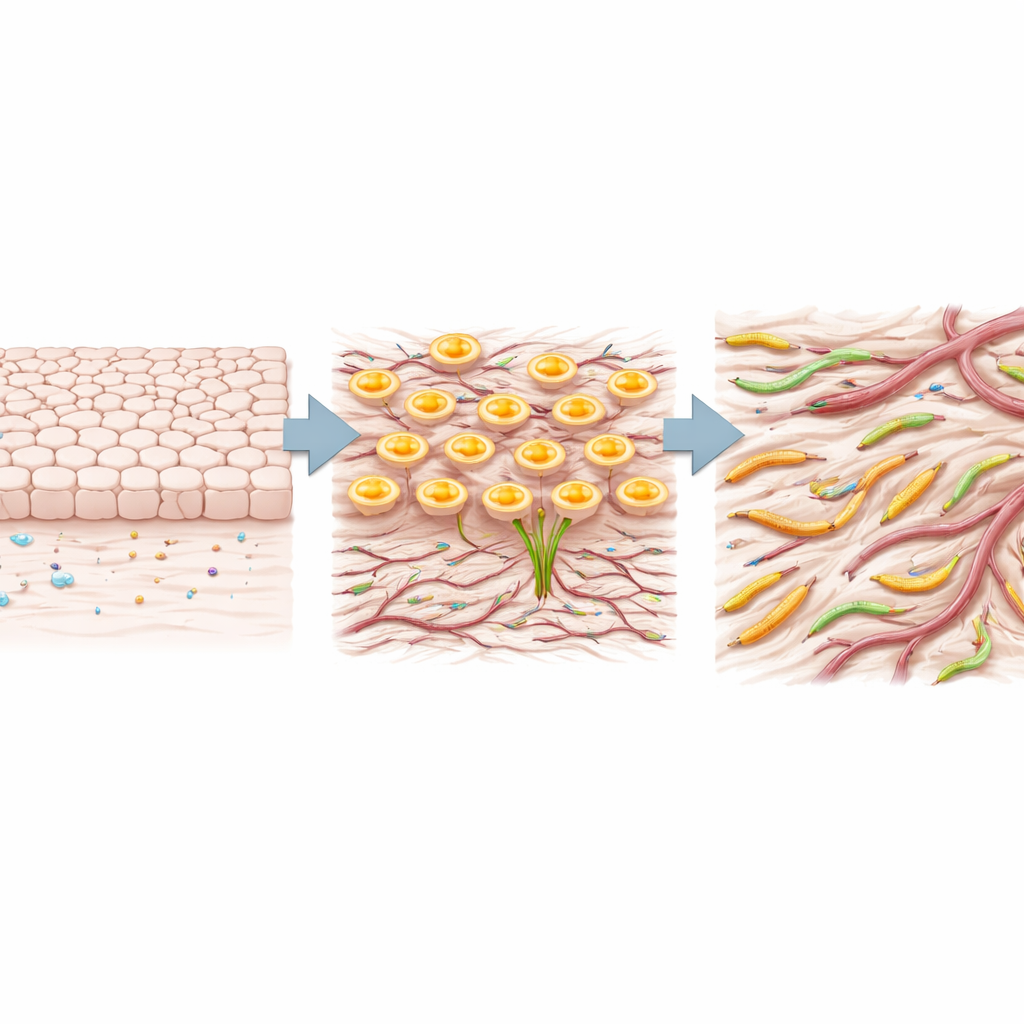
我们的器官由有序的细胞层构成,这些细胞通常固定在原位。癌症致命的关键在于这些细胞松散连接、改变形态并开始迁移——这一过程常被称为细胞“身份转换”。作者发现高表达TRIM29的肺肿瘤与这种转换行为紧密相关。通过分析大型公开的肿瘤RNA数据集,他们证明TRIM29丰富的癌症在基因程序上富集了与失去稳定上皮特征并获得更具移动性和侵袭性的表型相关的信号。肿瘤TRIM29含量较高的患者生存期倾向较短,提示该蛋白是预后不良的标志物。
塑造肿瘤的“邻里”环境
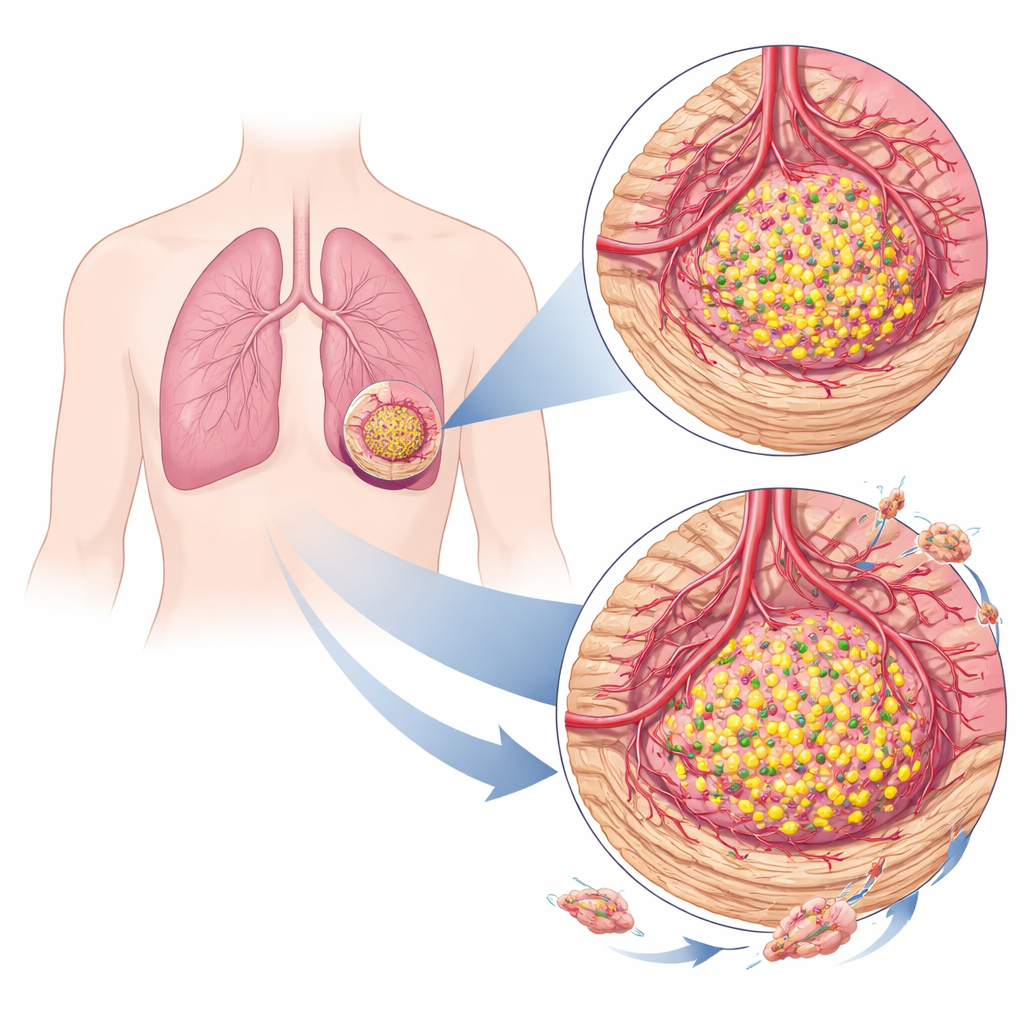
肿瘤并非独自生长;它们会招募血管和支持性细胞,并重塑周围组织。利用能够解析整体肿瘤样本中细胞成分的计算工具,研究团队发现TRIM29高表达的肺肿瘤所处的“邻里”与TRIM29低表达的肿瘤明显不同。富含该蛋白的癌症往往具有更多成纤维细胞——负责沉积疤痕样组织的细胞——以及更多内皮细胞,内皮细胞构成血管内皮层。这些肿瘤在“基质”和“微环境”信号上的得分更高,表明其具有更厚、更活跃的支持组织和更丰富的血供,这些特征都可能促进肿瘤生长与扩散。
显微镜下观察这些信号
为超越计算预测,研究人员检查了在同一家医院接受治疗的200例肺腺癌患者的肿瘤样本。他们对组织进行了TRIM29、调控细胞身份转换的关键因子(SNAIL和TWIST)、微小血管以及支持组织与肿瘤细胞比例的染色。TRIM29更高的肿瘤显示出更多的SNAIL和TWIST、更致密的微血管网络以及更大的基质区域,证实TRIM29与血管丰富、呈瘢痕样的微环境相关。有趣的是,细胞转换终末阶段的经典标志(如E-cadherin丧失和波形蛋白增加)并未显示出同样强的相关性,这提示许多肿瘤可能处于一种“部分”转化状态,单一标志难以完全捕捉。
在癌细胞与药物中检验TRIM29的作用
团队进一步探问TRIM29仅是“路人”标记还是癌细胞中的主动驱动因子。在两种肺腺癌细胞系中,他们用小RNA分子降低了TRIM29的表达。TRIM29下调后,细胞减少了SNAIL和TWIST的表达,黏附分子E-cadherin上调,N-cadherin下降,并且在划痕愈合实验中迁移更慢。这些变化与细胞向更稳定、较少侵袭性的状态逆转一致。最后,通过挖掘大型药物反应数据库,研究人员寻找在TRIM29高表达细胞系中特别有效的化合物。一个清晰的模式浮现:多种mTOR抑制剂在TRIM29高表达细胞中活性更强,提示这些侵袭性肿瘤可能存在可被利用的脆弱点。
对患者意味着什么
综合而言,这项研究将TRIM29描绘为连接细胞身份变化、血管生成与组织重塑的枢纽——同时也是不良预后的标志。尽管仍需在动物模型和临床试验中开展更多工作,研究结果表明检测TRIM29或可帮助识别病情特别侵袭性的患者,并且mTOR抑制药物或许对这类患者更为有效。从长远看,直接针对TRIM29本身或其重塑肿瘤“邻里”方式的策略,可能为减缓或阻止这一常见且致命的癌症类型扩散开辟新途径。
引用: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
关键词: 肺腺癌, TRIM29, 肿瘤微环境, 上皮-间质转化, mTOR抑制剂