Clear Sky Science · de
TRIM29 fördert epithelial-mesenchymale Transition, Angiogenese und stromale Umgestaltung bei Lungenadenokarzinom: integrierte Validierung auf histologischer, transkriptomischer und Proteinebene
Warum diese Lungenkrebsstudie wichtig ist
Lungenkrebs gehört weiterhin zu den häufigsten krebsbedingten Todesursachen, und viele Patienten profitieren nicht von den heute verfügbaren zielgerichteten Therapien oder Immuntherapien. Diese Studie untersucht ein wenig bekanntes Protein namens TRIM29 und stellt eine zentrale Frage: Trägt es dazu bei, dass Lungentumoren aggressiver und schwerer zu behandeln werden? Indem die Autoren genetische Daten, mikroskopische Bilder realer Tumoren, Zellexperimente und Wirkstoffscreenings zusammenführen, zeigen sie, dass TRIM29 ein Kennzeichen — und möglicherweise ein Treiber — einer gefährlicheren Form des Lungenadenokarzinoms, der häufigsten Lungenkrebsart, ist.
Ein verborgener Helfer der Tumorausbreitung
Unsere Organe bestehen aus geordneten Zellschichten, die an ihrem Platz bleiben. Krebs wird dann tödlich, wenn diese Zellen ihre Verbindungen lösen, ihre Gestalt verändern und zu wandern beginnen — ein Prozess, der oft als „Identitätswechsel“ der Zelle bezeichnet wird. Die Autoren fanden heraus, dass Lungentumoren mit hohen TRIM29-Spiegeln stark mit diesem wechselähnlichen Verhalten verknüpft waren. Durch die Analyse großer öffentlicher Tumor-RNA-Datensätze zeigten sie, dass TRIM29-reiche Karzinome für Genprogramme angereichert waren, die mit dem Verlust stabiler epithelialer Eigenschaften und dem Erwerb mobiler, invasiver Merkmale verbunden sind. Patienten mit tumoraler TRIM29‑Hochexpression hatten tendenziell eine kürzere Überlebenszeit, was darauf hindeutet, dass dieses Protein ein Marker für eine schlechte Prognose ist.
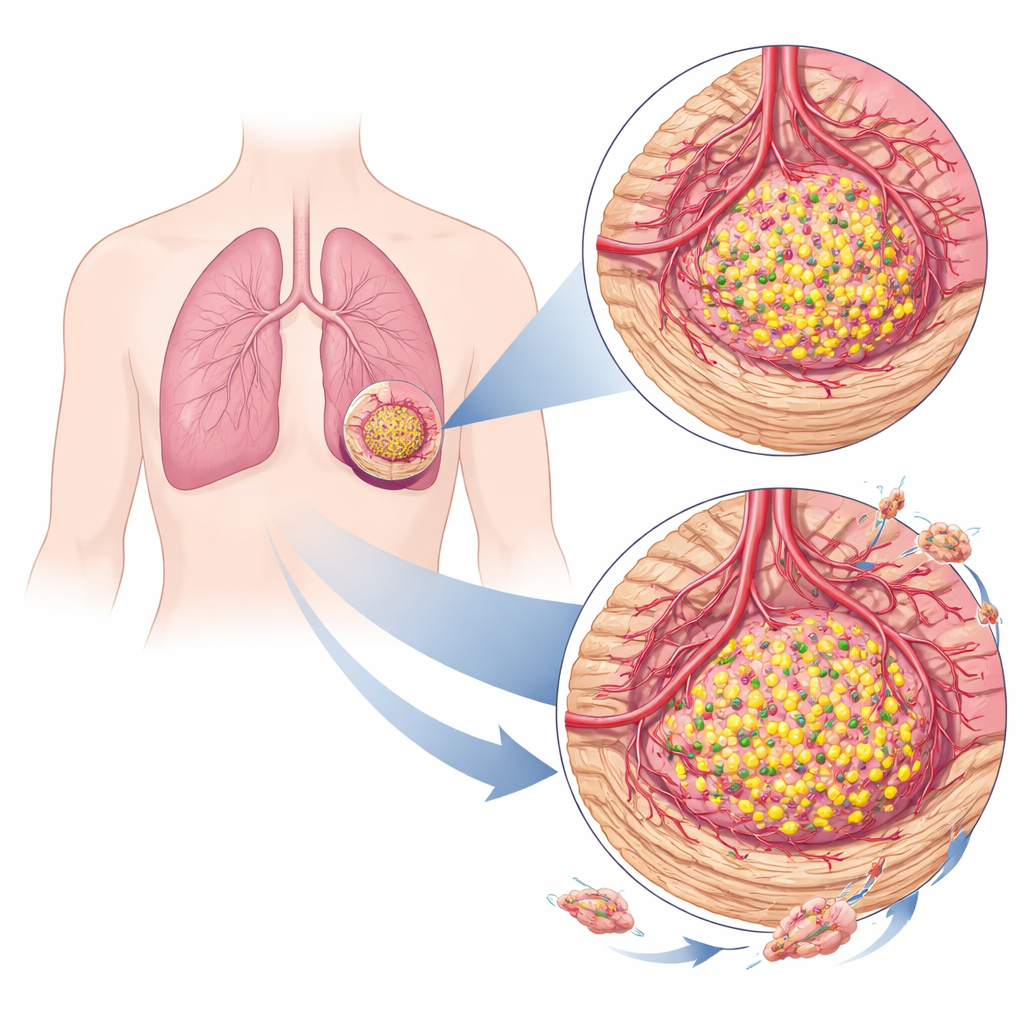
Die Nachbarschaft des Tumors gestalten
Tumoren wachsen nicht allein; sie rekrutieren Blutgefäße und unterstützende Zellen und verändern das umliegende Gewebe. Mit Rechenverfahren, die die Zellmischung in Bulk‑Tumorproben auseinanderlegen, fanden die Forschenden heraus, dass TRIM29-hohe Lungentumoren in einer ganz anderen Mikroumgebung lagen als TRIM29‑niedrige Tumoren. Karzinome mit hohem TRIM29 enthielten häufiger Fibroblasten — Zellen, die narbenähnliches Gewebe bilden — und mehr Endothelzellen, die Blutgefäße auskleiden. Diese Tumoren wiesen höhere Werte für „stromale“ und „Mikroumgebungs“-Signale auf, was auf eine dichtere, reaktivere Stützstruktur und eine reichere Blutversorgung hinweist, die beide Tumorwachstum und -ausbreitung fördern können.
Signale unter dem Mikroskop sehen
Um über computerbasierte Vorhersagen hinauszugehen, untersuchten die Forschenden Tumorproben von 200 Lungenadenokarzinom‑Patienten, die an einem einzigen Krankenhaus behandelt wurden. Sie färbten die Gewebe für TRIM29, Schlüsselregulatoren des Identitätswechsels (SNAIL und TWIST), kleine Blutgefäße und das Verhältnis von Stützgewebe zu Krebszellen. Tumoren mit höherer TRIM29‑Expression zeigten mehr SNAIL und TWIST, dichtere Netzwerke kleiner Blutgefäße und eine größere stromale Fläche, was bestätigt, dass TRIM29 mit einer gefäßreichen, narbenähnlichen Umgebung verbunden ist. Interessanterweise korrelierten klassische Endstadienmarker des Identitätswechsels, wie Verlust von E‑Cadherin und Zunahme von Vimentin, nicht so stark, was darauf hindeutet, dass viele Tumoren sich in einem teilweisen Übergangszustand befinden, den einfache Marker nur schwer erfassen.
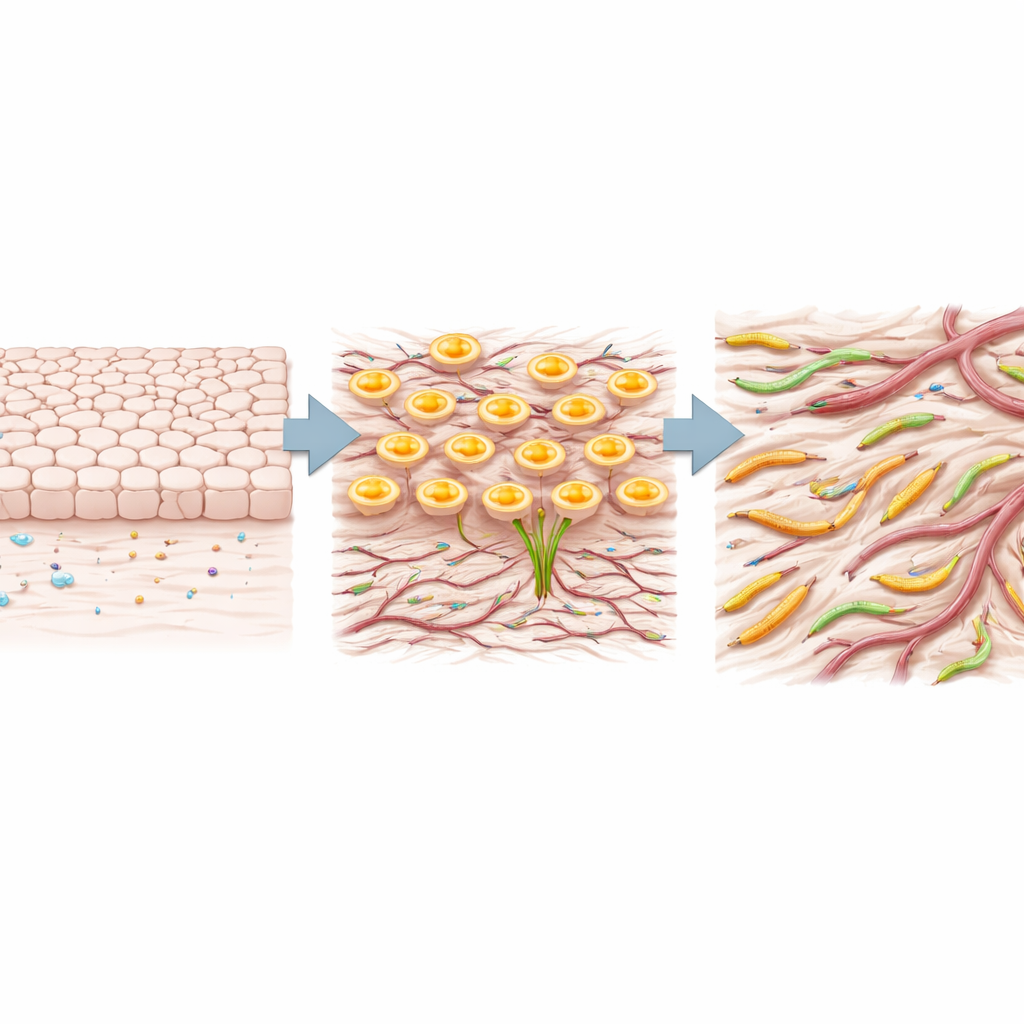
TRIM29s Rolle in Krebszellen und bei Medikamenten testen
Die Gruppe fragte anschließend, ob TRIM29 nur ein Nebenakteur oder ein aktiver Treiber in Krebszellen ist. In zwei Lungenadenokarzinom‑Zelllinien setzten sie kleine RNA‑Moleküle ein, um TRIM29 herunterzuregulieren. Bei Reduktion von TRIM29 verringerten die Zellen SNAIL und TWIST, erhöhten das Adhäsionsmolekül E‑Cadherin, senkten N‑Cadherin und wanderten in Wundheilungsassays langsamer. Diese Veränderungen stimmen mit einem Rückgang hin zu einem sesshafteren, weniger invasiven Zustand überein. Schließlich durchsuchten die Forschenden große Datenbanken zu Wirkstoffantworten nach Substanzen, die in Zelllinien mit hoher TRIM29‑Expression besonders wirksam waren. Ein klares Muster zeigte sich: Mehrere Inhibitoren von mTOR, einem zentralen Wachstums‑ und Überlebensweg, waren in TRIM29‑hohen Zellen aktiver, was auf eine mögliche Schwachstelle dieser aggressiven Tumoren hinweist.
Was das für Patientinnen und Patienten bedeutet
Zusammengefasst zeichnet die Studie TRIM29 als Knotenpunkt, der Zellidentitätsveränderungen, Gefäßbildung und Geweberemodellierung im Lungenadenokarzinom verbindet — und als Marker für schlechtere Ergebnisse. Zwar sind weitere Arbeiten in Tiermodellen und klinische Studien nötig, doch deuten die Befunde darauf hin, dass die Messung von TRIM29 helfen könnte, Patienten mit besonders aggressiver Erkrankung zu identifizieren, und dass mTOR‑blockierende Medikamente für diese Gruppe besonders nützlich sein könnten. Langfristig könnte das gezielte Angreifen von TRIM29 selbst oder der Art und Weise, wie es die Tumornachbarschaft umgestaltet, neue Wege eröffnen, um die Ausbreitung dieser häufigen und tödlichen Krebsform zu verlangsamen oder zu stoppen.
Zitation: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
Schlüsselwörter: Lungenadenokarzinom, TRIM29, Tumormikroumgebung, epithelial-mesenchymale Transition, mTOR-Inhibitoren