Clear Sky Science · pl
TRIM29 promuje przejście nabłonkowo-mezenchymalne, angiogenezę i przebudowę zrębu w gruczolakoraku płuca: zintegrowana walidacja na poziomie histologicznym, transkryptomicznym i białkowym
Dlaczego to badanie raka płuca ma znaczenie
Rak płuca wciąż jest jedną z głównych przyczyn zgonów z powodu nowotworów, a wielu pacjentów nie odnosi korzyści z obecnych terapii celowanych ani immunoterapii. To badanie skupia się na mało poznanym białku o nazwie TRIM29 i stawia ważne pytanie: czy pomaga ono guzom płucnym stać się bardziej agresywnymi i trudniejszymi do leczenia? Łącząc dane genetyczne, obrazy mikroskopowe rzeczywistych guzów, eksperymenty na liniach komórkowych i ekrany lekowe, badacze pokazują, że TRIM29 oznacza — i może wspierać — groźniejszą postać gruczolakoraka płuca, najczęstszej odmiany raka płuca.
Ukryty wspomagacz rozprzestrzeniania się guza
Nasze narządy zbudowane są z uporządkowanych warstw komórek, które pozostają na miejscu. Rak staje się śmiertelny, gdy te komórki rozluźniają więzi, zmieniają kształt i zaczynają migrować — proces często określany jako „zmiana tożsamości” komórkowej. Autorzy stwierdzili, że guzy płuc z wysokim poziomem TRIM29 silnie wiązały się z takim przełącznikowym zachowaniem. Analizując duże publiczne zbiory danych RNA guzów, pokazali, że nowotwory bogate w TRIM29 były wzbogacone w programy genowe związane z utratą stabilnych cech nabłonkowych i nabywaniem cech bardziej ruchliwych, inwazyjnych. Pacjenci, których guzy miały więcej TRIM29, mieli tendencję do krótszego przeżycia, co sugeruje, że to białko jest markerem gorszego rokowania.
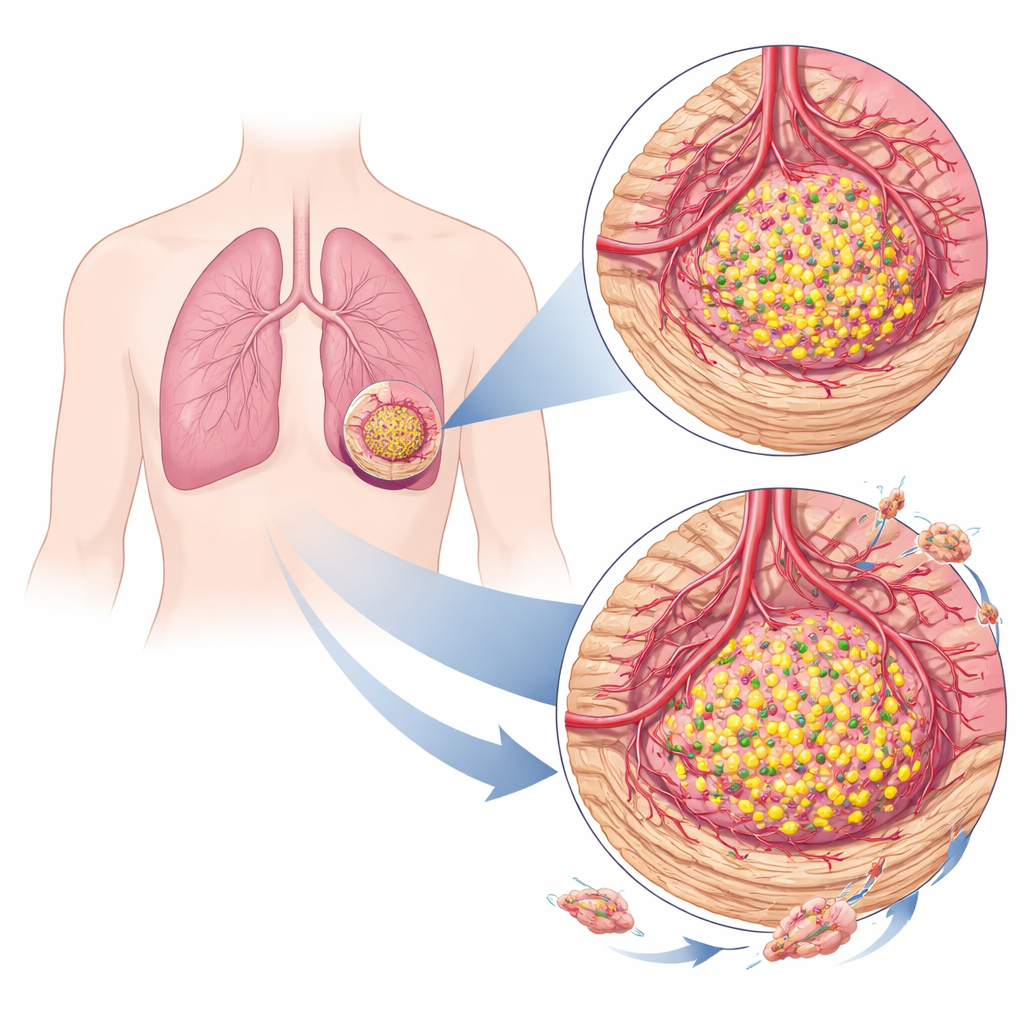
Współkształtowanie otoczenia guza
Guzy nie rosną w izolacji; rekrutują naczynia krwionośne i komórki wspierające oraz przebudowują otaczającą je tkankę. Korzystając z narzędzi obliczeniowych rozdzielających skład mieszanych próbek guza, zespół odkrył, że guzy płuc z wysokim poziomem TRIM29 leżą w zupełnie innym „sąsiedztwie” niż guzy z niskim poziomem TRIM29. Nowotwory bogate w to białko miały tendencję do większej liczby fibroblastów — komórek wytwarzających tkankę podobną do blizny — oraz komórek śródbłonka, które wyściełają naczynia krwionośne. Te guzy uzyskały wyższe wyniki w sygnałach „zrębowych” i „mikrośrodowiskowych”, co wskazuje na gęstsze, bardziej reaktywne tkanki wspierające i bogatsze ukrwienie — oba czynniki mogą sprzyjać wzrostowi i rozprzestrzenianiu się guza.
Widzieć sygnały pod mikroskopem
Aby wyjść poza przewidywania komputerowe, badacze zbadali próbki guzów od 200 pacjentów z gruczolakorakiem płuca leczonych w jednym szpitalu. Barwili tkanki pod kątem TRIM29, kluczowych regulatorów zmiany tożsamości komórkowej (SNAIL i TWIST), drobnych naczyń krwionośnych oraz proporcji tkanki zrębowej do komórek nowotworowych. Guzy z wyższym poziomem TRIM29 wykazywały więcej SNAIL i TWIST, gęstsze sieci drobnych naczyń krwionośnych oraz większy obszar zrębowy, potwierdzając związek TRIM29 ze środowiskiem bogatym w naczynia i przypominającym bliznę. Co ciekawe, klasyczne końcowe markery przejścia komórkowego, takie jak utrata E-kadheryny i wzrost wimentyny, nie korelowały tak silnie, co sugeruje, że wiele guzów może znajdować się w „częściowym” stanie przejściowym, trudnym do uchwycenia prostymi markerami.
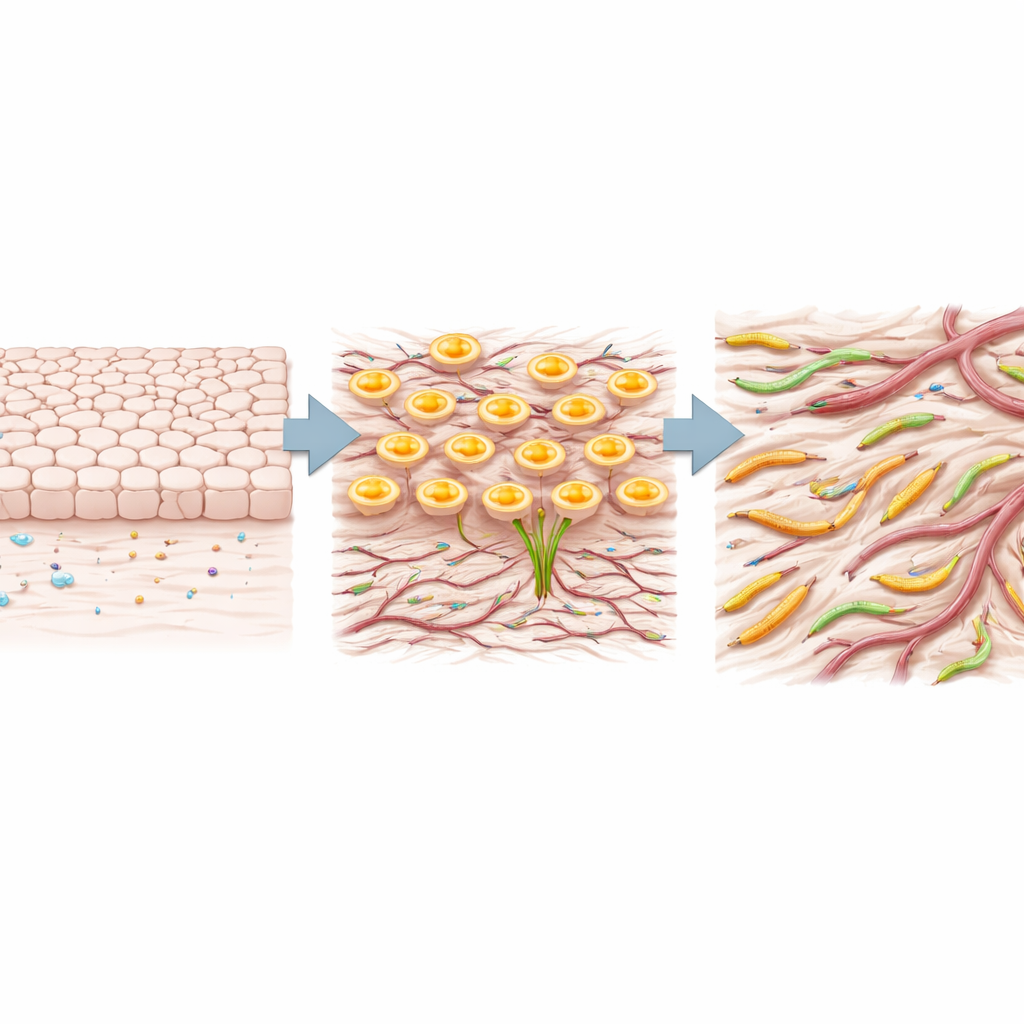
Testowanie roli TRIM29 w komórkach nowotworowych i w kontekście leków
Zespół następnie zapytał, czy TRIM29 jest tylko pasażerem, czy aktywnym kierowcą w komórkach nowotworowych. W dwóch liniach komórkowych gruczolakoraka płuca zastosowali małe cząsteczki RNA do wyciszenia TRIM29. Gdy poziom TRIM29 został obniżony, komórki zmniejszyły ekspresję SNAIL i TWIST, zwiększyły cząsteczkę adhezji E-kadherynę, obniżyły N-kadherynę i poruszały się wolniej w testach gojenia ran. Zmiany te są zgodne z cofnięciem się komórek ku stanowi bardziej osiadłemu, mniej inwazyjnemu. Wreszcie, analizując duże bazy danych odpowiedzi na leki, badacze poszukali związków szczególnie skutecznych w liniach komórkowych z wysokim poziomem TRIM29. Pojawił się wyraźny wzorzec: kilka inhibitorów mTOR, istotnej ścieżki wzrostu i przeżycia, było bardziej aktywnych w komórkach z wysokim TRIM29, wskazując na możliwą słabą stronę tych agresywnych guzów.
Co to oznacza dla pacjentów
Podsumowując, badanie przedstawia TRIM29 jako węzeł łączący zmiany tożsamości komórkowej, wzrost naczyń krwionośnych i przebudowę tkanki w gruczolakoraku płuca — oraz jako marker gorszych wyników. Choć potrzebne są dalsze badania na modelach zwierzęcych i próby kliniczne, wyniki sugerują, że pomiar TRIM29 mógłby pomóc zidentyfikować pacjentów z wyjątkowo agresywną chorobą, a leki blokujące mTOR mogą być szczególnie przydatne w tej grupie. W dłuższej perspektywie ukierunkowanie samego TRIM29 lub sposobu, w jaki kształtuje otoczenie guza, może otworzyć nowe drogi do spowolnienia lub zatrzymania rozprzestrzeniania się tego powszechnego i śmiertelnego rodzaju raka.
Cytowanie: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
Słowa kluczowe: gruczolakorak płuca, TRIM29, mikrośrodowisko guza, przejście nabłonkowo-mezenchymalne, inhibitory mTOR