Clear Sky Science · sv
TRIM29 främjar epitel–mesenkymal övergång, angiogenes och stromal ombyggnad i lungadenokarcinom: integrerad validering på histologisk, transkriptomisk och proteinnivå
Varför denna lungcancerstudie är viktig
Lungcancer är fortfarande en av de främsta orsakerna till cancerrelaterad död, och många patienter får inte nytta av dagens riktade läkemedel eller immunterapier. Denna studie undersöker ett relativt okänt protein kallat TRIM29 och ställer en avgörande fråga: bidrar det till att lungtumörer blir mer aggressiva och svårare att behandla? Genom att förena genetiska data, mikroskopiska bilder av verkliga tumörer, cellförsök och läkemedelsscreeningar visar forskarna att TRIM29 kännetecknar — och kan bidra till — en farligare form av lungadenokarcinom, den vanligaste typen av lungcancer.
En dold hjälpare vid tumörspridning
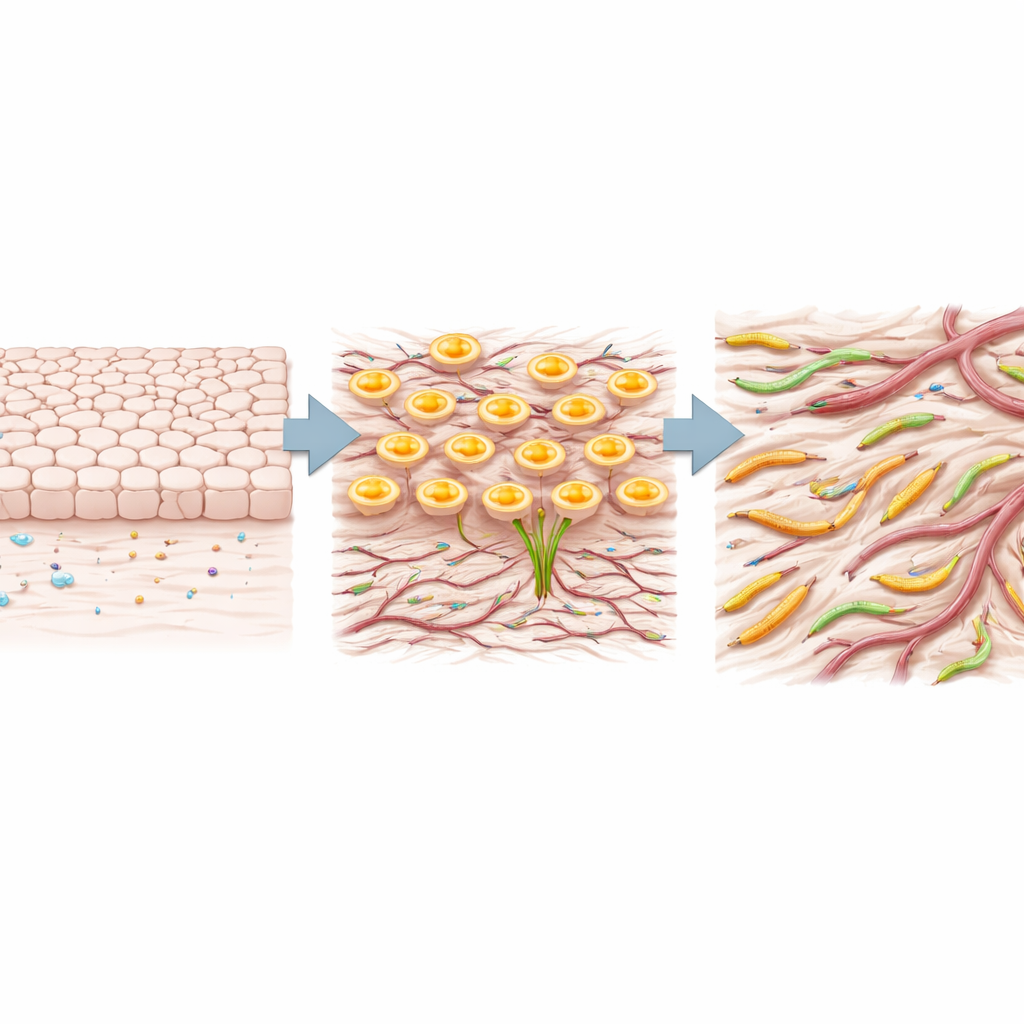
Våra organ är uppbyggda av ordnade skikt av celler som sitter kvar på sina platser. Cancer blir dödlig när dessa celler släpper sina bindningar, ändrar form och börjar migrera — en process ofta kallad en cellers "identitetsväxling." Författarna fann att lungtumörer med höga nivåer av TRIM29 starkt kopplades till detta växlingslika beteende. Genom att analysera stora publika dataset av tumör-RNA visade de att TRIM29-rika cancerformer var berikade för genprogram kopplade till att celler förlorar sina stabila epiteliala egenskaper och får mer rörliga, invasiva egenskaper. Patienter vars tumörer innehöll mer TRIM29 tenderade att leva kortare, vilket tyder på att detta protein är en markör för dålig prognos.
Formar tumörens omgivning
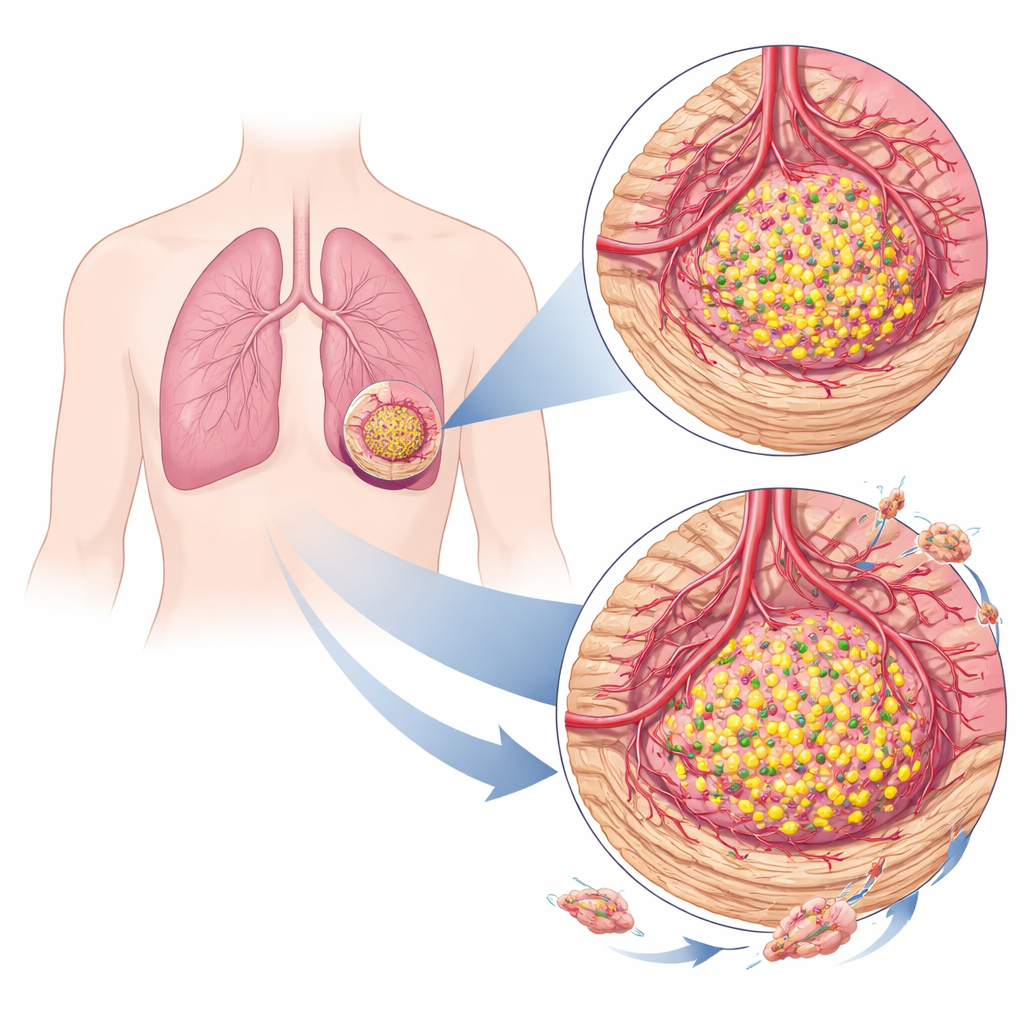
Tumörer växer inte ensamma; de rekryterar blodkärl och stödjeceller och omformar vävnaden runt sig. Med hjälp av beräkningsverktyg som skiljer ut blandningen av celler i bulk-tumörprover fann teamet att TRIM29-höga lungtumörer befann sig i ett mycket annorlunda kvarter än TRIM29-låga tumörer. Cancerformer rika på detta protein tenderade att ha fler fibroblaster — celler som lägger ner ärrliknande vävnad — och fler endotelceller, som bekläder blodkärl. Dessa tumörer fick högre poäng för "stromala" och "mikromiljö"-signaler, vilket indikerar en tjockare, mer reaktiv stödvävnad och rikare blodtillförsel, båda faktorer som kan främja tumörtillväxt och spridning.
Se signalerna i mikroskopet
För att gå bortom datorbaserade prediktioner undersökte forskarna tumörprover från 200 patienter med lungadenokarcinom som behandlats vid ett enda sjukhus. De immunfärgade vävnaderna för TRIM29, nyckelregulatorer av cellens identitetsväxling (SNAIL och TWIST), små blodkärl och andelen stödvävnad kontra cancerceller. Tumörer med högre TRIM29 visade mer SNAIL och TWIST, tätare nätverk av små blodkärl och ett större stromalt område, vilket bekräftar att TRIM29 är kopplat till en blodkärlsrik, ärrliknande miljö. Intressant nog korrelerade inte klassiska slutstegsmarkörer för övergången, såsom förlust av E-cadherin och ökning av vimentin, lika starkt, vilket antyder att många tumörer kan befinna sig i ett "delvis" övergångstillstånd som är svårt att fånga med enkla markörer.
Test av TRIM29:s roll i cancerceller och läkemedel
Teamet frågade därefter om TRIM29 bara är en passagerare eller en aktiv drivkraft i cancerceller. I två lungadenokarcinomcellinjer använde de små RNA-molekyler för att slå ner TRIM29. När TRIM29 minskades sänkte cellerna uttrycket av SNAIL och TWIST, ökade adhesionsmolekylen E-cadherin, minskade N-cadherin och migrerade långsammare i sår-helingsassays. Dessa förändringar är förenliga med att celler återgår mot ett mer stillsamt, mindre invasivt tillstånd. Slutligen, genom att utvinna information från stora databaser över läkemedelssvar, sökte forskarna efter substanser som var särskilt effektiva i cellinjer med högt TRIM29. Ett tydligt mönster framträdde: flera hämmare av mTOR, en central tillväxt- och överlevnadsväg, var mer aktiva i TRIM29-höga celler, vilket pekar på en möjlig svag punkt i dessa aggressiva tumörer.
Vad detta betyder för patienter
Sammantaget målar studien upp TRIM29 som en navpunkt som förenar förändringar i cellidentitet, blodkärlsbildning och vävnadsombyggnad i lungadenokarcinom — och som en markör för sämre utfall. Även om mer arbete i djurmodeller och kliniska prövningar behövs, tyder resultaten på att mätning av TRIM29 kan hjälpa till att identifiera patienter med särskilt aggressiv sjukdom och att mTOR-blockerande läkemedel kan vara särskilt användbara för denna grupp. På längre sikt kan riktade angrepp mot TRIM29 självt, eller mot hur det omformar tumörens omgivning, öppna nya vägar för att bromsa eller stoppa spridningen av denna vanliga och dödliga cancermetastasform.
Citering: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
Nyckelord: lungadenokarcinom, TRIM29, tumörmikromiljö, epitelial mesenkymal övergång, mTOR-hämmare