Clear Sky Science · ar
TRIM29 يعزز الانتقال الظهاري-اللحمي، وتكوين الأوعية، وإعادة تشكيل النسيج الضام في سرطان الغدد الرئوية: تصديق متكامل على المستويات النسيجية، النسخية والبروتينية
لماذا تهم هذه الدراسة عن سرطان الرئة
يبقى سرطان الرئة أحد الأسباب الرئيسية لوفاة المصابين بالسرطان، والعديد من المرضى لا يستفيدون من الأدوية الموجهة أو العلاجات المناعية المتاحة اليوم. تبحث هذه الدراسة بروتينًا غير معروف على نطاق واسع يُدعى TRIM29 وتطرح سؤالًا كبيرًا: هل يساعد هذا البروتين الأورام الرئوية على أن تصبح أكثر عدوانية وأصعب علاجًا؟ من خلال ربط بيانات جينية، ولقطات مجهرية لأورام حقيقية، وتجارب خلوية، وفحوصات للأدوية، يُظهر الباحثون أن TRIM29 يميّز — وقد يساهم في دفع — شكل أكثر خطورة من سرطان غدد الرئة، وهو النوع الأكثر شيوعًا من سرطان الرئة.
مساعد خفي لانتشار الورم
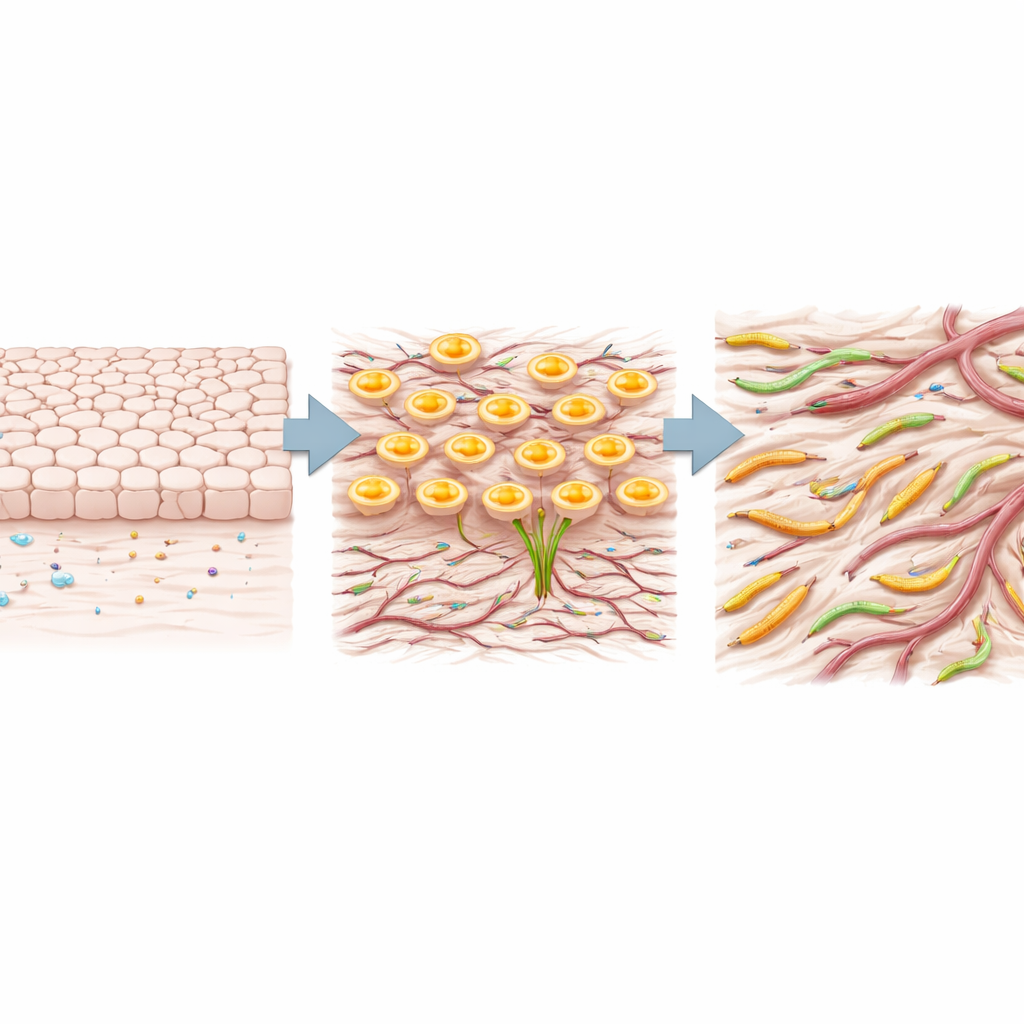
أعضائنا مبنية من صفائح مرتبة من الخلايا تبقى في موضعها. يصبح السرطان مميتًا عندما تضعف هذه الروابط الخلوية، وتغير الخلايا شكلها، وتبدأ في الهجرة — وهي عملية غالبًا ما تُسمى «تبديل هوية الخلية». وجد المؤلفون أن الأورام الرئوية ذات المستويات العالية من TRIM29 كانت مرتبطة بشدة بهذا السلوك الشبيه بالتبديل. من خلال تحليل مجموعات بيانات عامة كبيرة لرنا الأورام، أظهروا أن السرطانات الغنية بـTRIM29 كانت معززة لبرامج جينية مرتبطة بفقدان الخلايا لميزات ظهارية مستقرة واكتسابها لخصائص أكثر حركة وغزوًا. كان المرضى الذين تحتوي أورامهم على مزيد من TRIM29 يميلون إلى العيش لفترة أقصر، مما يشير إلى أن هذا البروتين علامة على تدهور النتيجة المتوقعة.
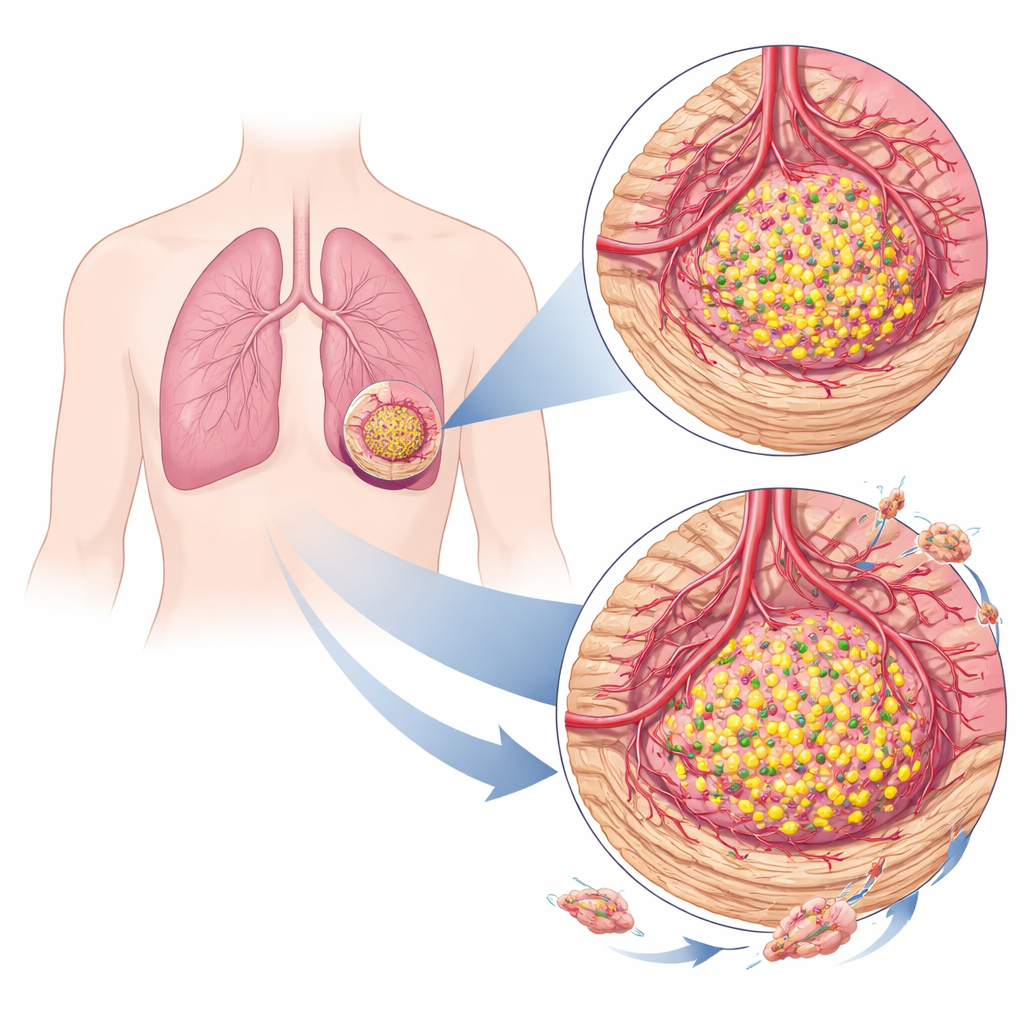
تشكيل حيٍّ الورم
الأورام لا تنمو بمفردها؛ فهي تستدعي الأوعية الدموية والخلايا الداعمة، وتعِدّل النسيج المحيط بها. باستخدام أدوات حاسوبية تفصل مزيج الخلايا في عينات أورام كلية، وجد الفريق أن الأورام الرئوية العالية في TRIM29 كانت تقع في حي مختلف جدًا عن الأورام المنخفضة فيه. السرطانات الغنية بهذا البروتين كانت تميل إلى احتواء مزيد من الأرومات الليفية — الخلايا التي تضع نسيجًا شبيهاً بالندبة — ومزيد من الخلايا البطانية التي تبطن الأوعية الدموية. سجلت هذه الأورام درجات أعلى لإشارات «النسيج الضام» و«البيئة الميكروية»، مما يشير إلى نسيج داعم أكثر سمكًا وتفاعلية وإمداد دموي أغنى، وكلاهما يمكن أن يعزز نمو الورم وانتشاره.
مشاهدة الإشارات تحت المجهر
للانتقال إلى ما وراء التنبؤات الحاسوبية، فحص الباحثون عينات ورم من 200 مريض بسرطان غدد الرئة عولجوا في مستشفى واحد. صبغوا الأنسجة لـTRIM29، والمنظمات الرئيسية لتبديل هوية الخلية (SNAIL وTWIST)، والأوعية الدموية الصغيرة، ونسبة النسيج الداعم مقارنة بخلايا الورم. أظهرت الأورام ذات TRIM29 الأعلى مزيدًا من SNAIL وTWIST، وشبكات أكثر كثافة من الأوعية الدقيقة الصغيرة، ومنطقة نسيج ضام أكبر، مؤكدة أن TRIM29 مرتبط ببيئة غنية بالأوعية وذات طابع شبيه بالندبة. ومن المثير للاهتمام أن علامات النهاية التقليدية لمرحلة الانتقال الخلوي، مثل فقدان E-cadherin واكتساب فيمنتين، لم ترتبط بنفس القوة، ما يوحي بأن العديد من الأورام قد تكون في حالة «انتقال جزئي» يصعب رصدها بعلامات بسيطة.
اختبار دور TRIM29 في الخلايا والدواء
سأل الفريق بعد ذلك ما إذا كان TRIM29 مجرد مرافق أم سائق نشط في خلايا السرطان. في خطين خلويين من سرطان غدد الرئة، استخدموا جزيئات رنا صغيرة لتثبيط TRIM29. عندما قلّ TRIM29، قلّت مستويات SNAIL وTWIST، وزاد جزيء التصاق E-cadherin، وانخفض N-cadherin، وتحركت الخلايا أبطأ في اختبارات شفاء الجروح. هذه التغيرات تتوافق مع عودة الخلايا إلى حالة أكثر استقرارًا وأقل غزوًا. أخيرًا، من خلال التنقيب في قواعد بيانات استجابة الأدوية الكبيرة، بحث الباحثون عن مركبات كانت فعالة بشكل خاص في الخطوط الخلوية عالية TRIM29. ظهر نمط واضح: عدة مثبطات لمسار mTOR، وهو مسار رئيسي للنمو والبقاء، كانت أكثر نشاطًا في الخلايا الغنية بـTRIM29، مما يشير إلى نقطة ضعف محتملة في هذه الأورام العدوانية.
ماذا يعني هذا للمرضى
مجملاً، تصوّر الدراسة TRIM29 كمحور يربط تغييرات هوية الخلايا، ونمو الأوعية الدموية، وإعادة تشكيل النسيج في سرطان غدد الرئة — وكمؤشر لنتائج أسوأ. بينما هناك حاجة للمزيد من العمل في نماذج حيوانية وتجارب سريرية، تشير النتائج إلى أن قياس TRIM29 قد يساعد في تمييز المرضى ذوي الأمراض الأكثر عدوانية، وأن أدوية حاصرات mTOR قد تكون مفيدة بشكل خاص لهذه الفئة. على المدى الطويل، قد يفتح استهداف TRIM29 نفسه، أو الطريقة التي يعيد بها تشكيل حي الورم، طرقًا جديدة لإبطاء أو إيقاف انتشار هذا النوع الشائع والفتاك من السرطان.
الاستشهاد: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
الكلمات المفتاحية: سرطان غدد الرئة, TRIM29, البيئة الميكروية للورم, الانتقال الظهاري إلى اللحمي, مثبطات mTOR