Clear Sky Science · fr
TRIM29 favorise la transition épithélio–mésenchymateuse, l’angiogenèse et le remodelage stromal dans l’adénocarcinome pulmonaire : validation intégrée aux niveaux histologique, transcriptomique et protéique
Pourquoi cette étude sur le cancer du poumon est importante
Le cancer du poumon reste l’une des principales causes de mortalité par cancer, et de nombreux patients ne bénéficient pas des traitements ciblés ou des immunothérapies disponibles aujourd’hui. Cette étude examine une protéine peu connue appelée TRIM29 et pose une question majeure : contribue‑t‑elle à rendre les tumeurs pulmonaires plus agressives et plus difficiles à traiter ? En reliant données génétiques, images microscopiques de tumeurs réelles, expériences cellulaires et criblages médicamenteux, les chercheurs montrent que TRIM29 identifie — et pourrait favoriser — une forme plus dangereuse d’adénocarcinome pulmonaire, le type de cancer du poumon le plus fréquent.
Un facilitateur caché de la dissémination tumorale
Nos organes sont constitués de couches ordonnées de cellules qui restent en place. Le cancer devient mortel lorsque ces cellules relâchent leurs liens, changent de forme et commencent à migrer — un processus souvent appelé « basculement d’identité cellulaire ». Les auteurs ont constaté que les tumeurs pulmonaires présentant des niveaux élevés de TRIM29 étaient fortement associées à ce comportement de type basculement. En analysant de larges jeux de données publics d’ARN tumoral, ils ont montré que les cancers riches en TRIM29 étaient enrichis en programmes géniques liés à la perte des caractéristiques épithéliales stables et à l’acquisition de traits plus mobiles et invasifs. Les patients dont les tumeurs présentaient plus de TRIM29 avaient tendance à avoir une survie plus courte, ce qui suggère que cette protéine est un marqueur de mauvais pronostic.
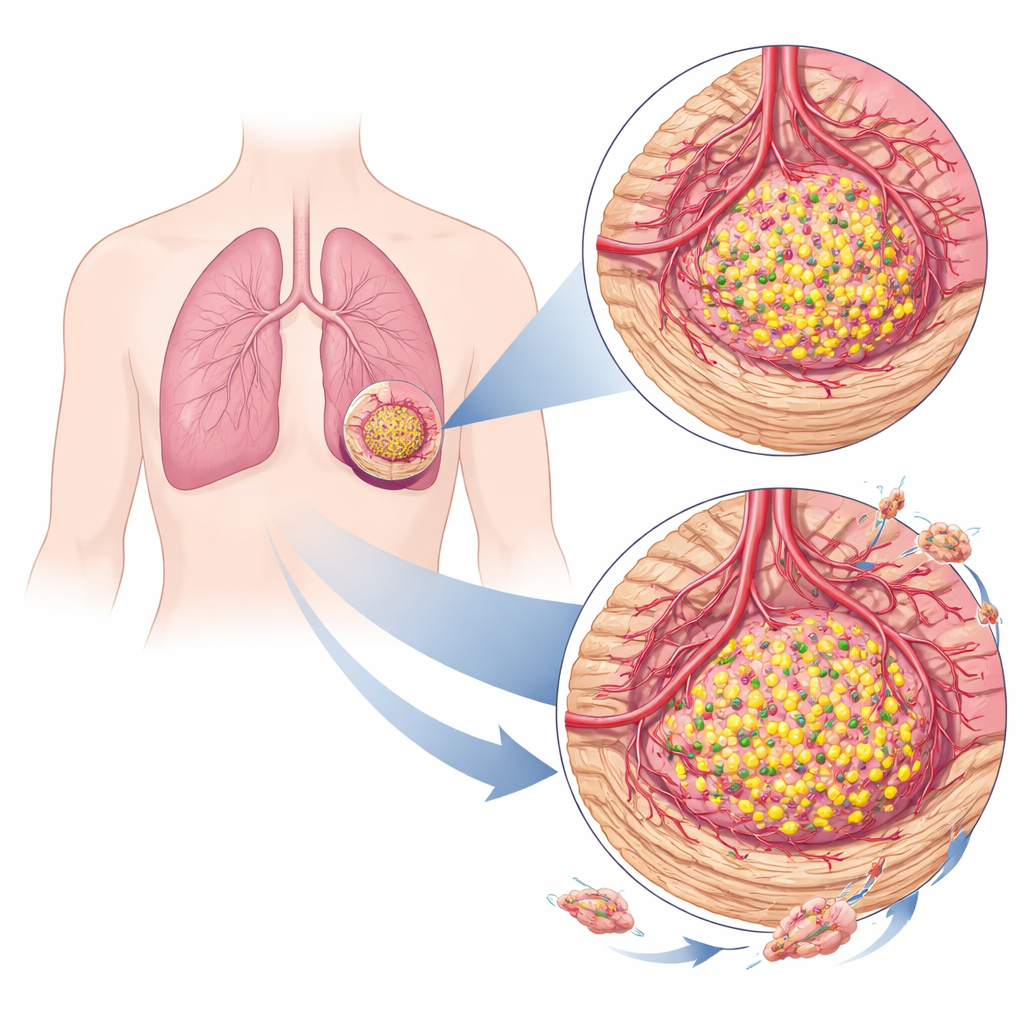
Façonner le voisinage tumoral
Les tumeurs ne se développent pas seules ; elles recrutent des vaisseaux sanguins et des cellules de soutien, et remodelent les tissus qui les entourent. En utilisant des outils computationnels capables de dissocier le mélange cellulaire dans des échantillons tumoraux en vrac, l’équipe a trouvé que les tumeurs pulmonaires à forte expression de TRIM29 se situaient dans un voisinage très différent de celui des tumeurs à faible expression. Les cancers riches en cette protéine avaient tendance à contenir plus de fibroblastes — des cellules qui déposent un tissu cicatriciel — et davantage de cellules endothéliales, qui tapissent les vaisseaux sanguins. Ces tumeurs présentaient des scores plus élevés pour des signatures « stromales » et de « microenvironnement », indiquant un tissu de soutien plus dense et réactif et un apport sanguin plus riche, deux facteurs qui peuvent favoriser la croissance et la dissémination tumorales.
Visualiser les signaux au microscope
Pour dépasser les prédictions informatiques, les chercheurs ont examiné des échantillons tumoraux de 200 patients atteints d’adénocarcinome pulmonaire traités dans un même hôpital. Ils ont coloré les tissus pour TRIM29, des régulateurs clés du basculement d’identité cellulaire (SNAIL et TWIST), les petits vaisseaux sanguins et la proportion de tissu de soutien par rapport aux cellules cancéreuses. Les tumeurs à expression élevée de TRIM29 présentaient plus de SNAIL et TWIST, des réseaux plus denses de petits vaisseaux, et une surface stromale plus grande, confirmant que TRIM29 est associé à un environnement riche en vaisseaux sanguins et de type cicatriciel. Fait intéressant, des marqueurs classiquement associés à l’état final du basculement, comme la perte d’E‑cadhérine et le gain de vimentine, n’étaient pas aussi fortement corrélés, ce qui suggère que de nombreuses tumeurs peuvent se trouver dans un état de transition « partielle » difficile à capter avec des marqueurs simples.
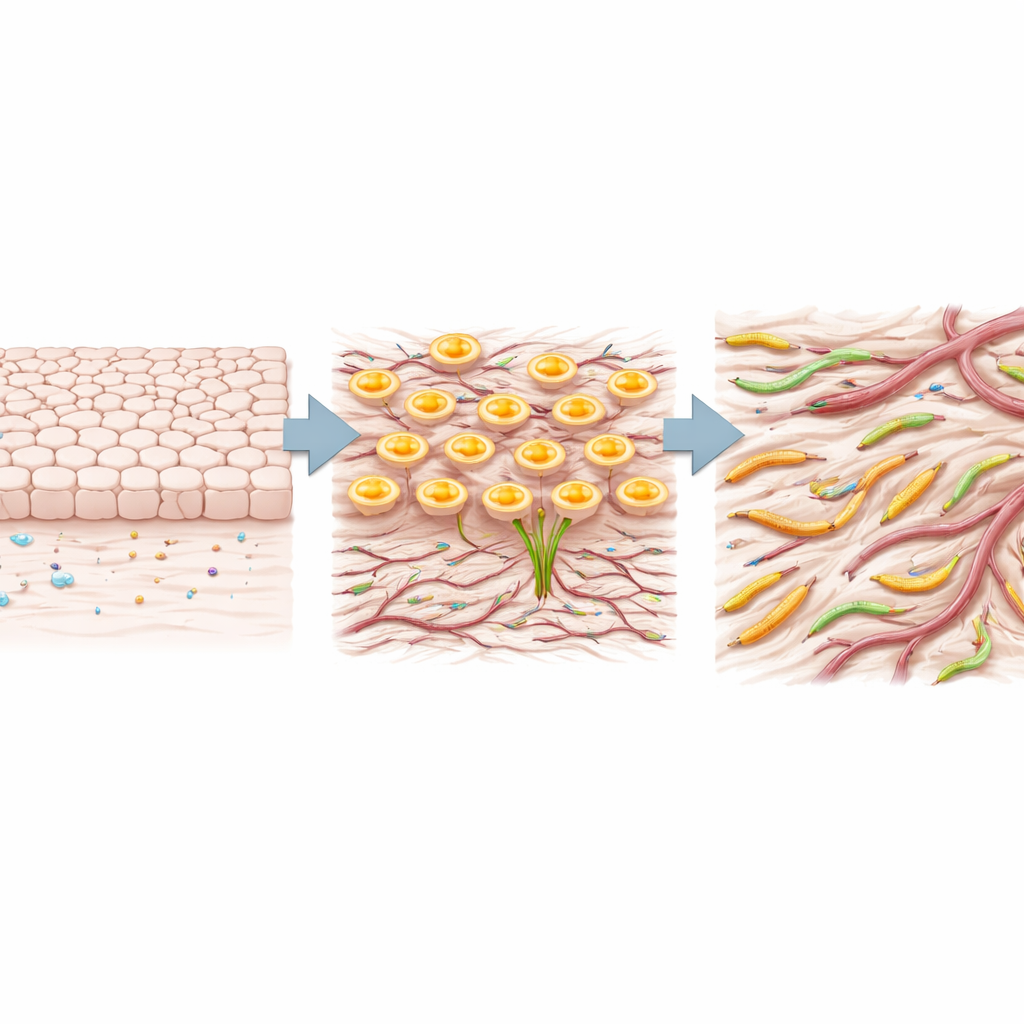
Tester le rôle de TRIM29 dans les cellules cancéreuses et vis‑à‑vis des médicaments
L’équipe a ensuite cherché à savoir si TRIM29 est un simple passager ou un acteur actif dans les cellules cancéreuses. Dans deux lignées cellulaires d’adénocarcinome pulmonaire, ils ont utilisé de petits ARN pour réduire l’expression de TRIM29. Lorsque TRIM29 a été diminué, les cellules ont réduit SNAIL et TWIST, augmenté la molécule d’adhésion E‑cadhérine, diminué la N‑cadhérine et migré plus lentement dans des essais de cicatrisation. Ces changements sont cohérents avec un retour des cellules vers un état plus stable et moins invasif. Enfin, en exploitant de grandes bases de données de réponses médicamenteuses, les chercheurs ont recherché des composés particulièrement efficaces dans les lignées cellulaires à forte expression de TRIM29. Un schéma clair est apparu : plusieurs inhibiteurs de mTOR, une voie majeure de croissance et de survie, étaient plus actifs dans les cellules riches en TRIM29, pointant vers une faiblesse potentielle de ces tumeurs agressives.
Ce que cela signifie pour les patients
Dans l’ensemble, l’étude présente TRIM29 comme un nœud reliant les changements d’identité cellulaire, la croissance vasculaire et le remodelage tissulaire dans l’adénocarcinome pulmonaire — et comme un marqueur d’un pronostic défavorable. Bien que des travaux supplémentaires en modèles animaux et des essais cliniques soient nécessaires, les résultats suggèrent que la mesure de TRIM29 pourrait aider à repérer les patients présentant une maladie particulièrement agressive et que les médicaments bloquant mTOR pourraient être particulièrement utiles pour ce groupe. À plus long terme, cibler TRIM29 lui‑même, ou la manière dont il reconfigure le voisinage tumoral, pourrait ouvrir de nouvelles voies pour ralentir ou arrêter la dissémination de ce type de cancer courant et meurtrier.
Citation: Hwang, Y., Han, JH., Haam, S. et al. TRIM29 promotes epithelial–mesenchymal transition, angiogenesis, and stromal remodeling in lung adenocarcinoma: integrated validation at histologic, transcriptomic, and protein levels. Sci Rep 16, 14505 (2026). https://doi.org/10.1038/s41598-026-45469-2
Mots-clés: adénocarcinome pulmonaire, TRIM29, microenvironnement tumoral, transition épithélio-mésenchymateuse, inhibiteurs de mTOR