Clear Sky Science · zh
利用 AlphaFold、分子对接与分子动力学对药用植物查尔酮合酶的综合结构与理化特性表征
植物如何合成有益天然化合物
许多存在于茶、草药和水果中的有益健康化合物都依赖于一种关键的植物酶——查尔酮合酶。这一分子“主力”帮助植物制造黄酮类化合物——具有抗氧化、抗炎甚至抗癌活性的天然产物。本文所基于的研究使用包括 AlphaFold 在内的现代计算工具来研究来自多种药用植物的查尔酮合酶,提出了一个看似简单的问题:这些酶有多相似?这对在营养学、医学和生物技术中利用它们意味着什么?
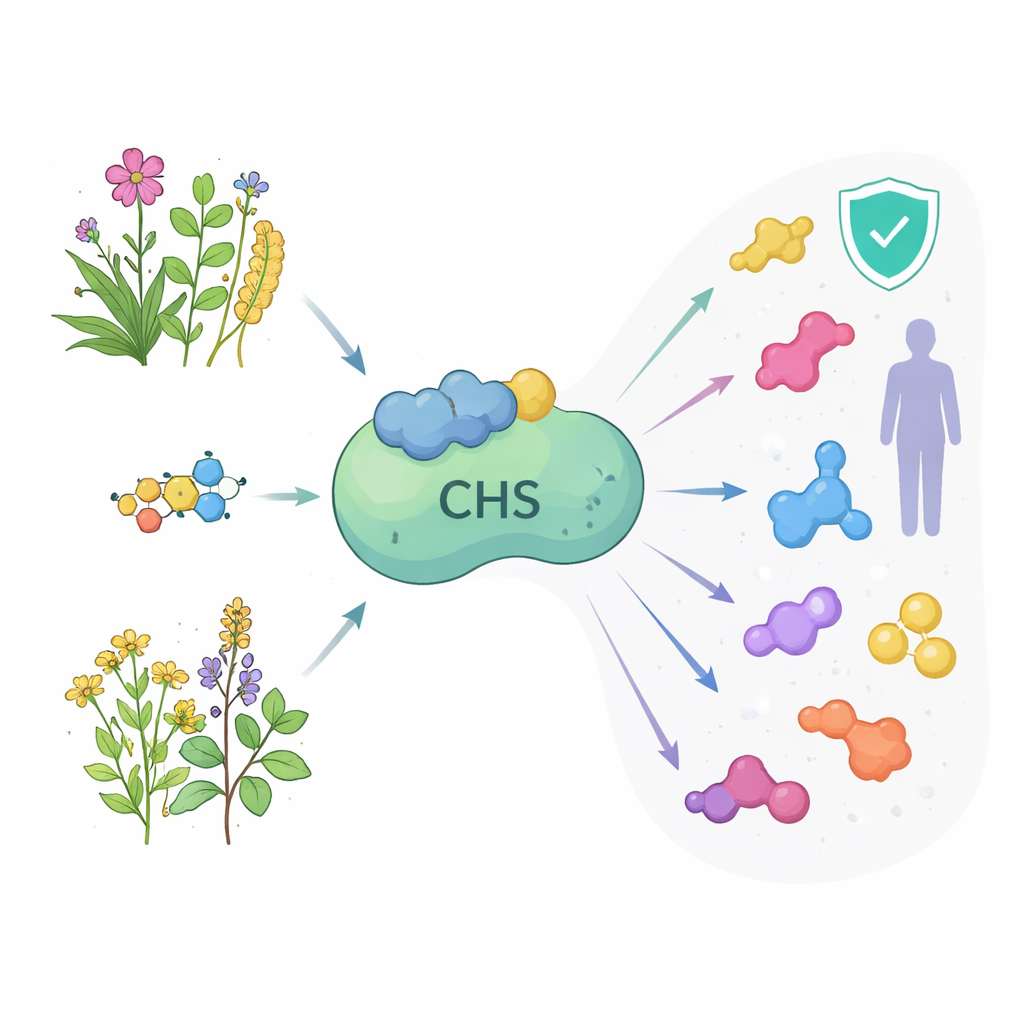
位于繁忙合成线起点的酶
查尔酮合酶位于黄酮合成通路的第一个限制性步骤。它以来自常见植物代谢的起始分子为底物,与三个小构件连接,生成柚皮素查尔酮(naringenin chalcone),这是通向多种黄酮的入口。下游产物为花果着色、保护叶片免受紫外线伤害、抵御微生物入侵,并作为与土壤细菌的化学信号。在人类健康研究中,这些分子被用于研究心脏健康、脑保护、抗感染疗法和抗癌等作用。由于单一酶决定了进入该途径的物质量,了解其在药用植物间的构象与行为,可能为提升或重新定向有价值天然产物提供新途径。
跨药用植物的比较
研究者收集了来自 13 种药用植物的查尔酮合酶蛋白序列,并以模式植物拟南芥作为参考。他们对这些序列进行比对并构建了家族树以评估亲缘关系。尽管这些植物来自许多不同的科,但酶的关键特征高度保守:由三种氨基酸组成的“催化三联体”以及决定活性通道形状的短特征基序。物种之间的大多数差异集中在蛋白末端或表面环区,而非核心催化部位。该模式表明,进化严格保护了基本反应,同时允许微妙的调整来调节各植物的黄酮化学特性。
计算模型揭示的构象与稳定性
研究团队使用 AlphaFold 和相关工具预测了每种酶的三维结构,并将它们与两种研究良好的物种的高质量晶体结构进行比较。比对结果非常接近——主链位置的差异小于十分之一纳米——这证实了预测模型在细节分析中的可靠性。所有查尔酮合酶版本都采用了该酶家族特有的折叠,但在承载底物的通道的形状和开放性上出现了小而具物种特异性的差异。简单计算还表明在预测的热稳定性、总体电荷以及亲水/疏水特性等方面存在适度差别。这些性状可能影响每种酶在实验室中的表达难易或在不同细胞与环境中的稳健性。
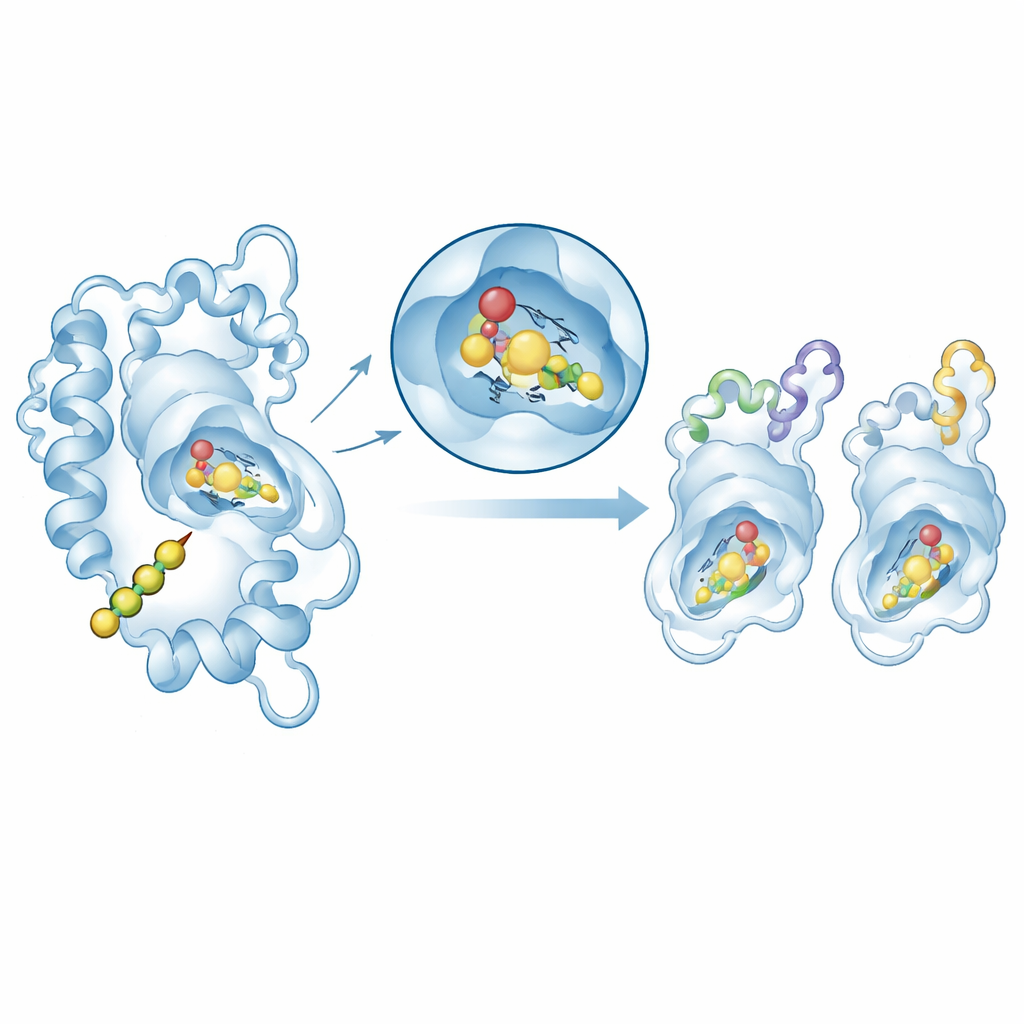
测试酶如何抓握其底物
为了将结构与功能联系起来,作者使用分子对接方法将天然起始分子对羟基桂酰辅酶 A(p-coumaroyl-CoA)置入所选查尔酮合酶模型的活性位点。在所有情况下,底物都嵌入到靠近保守催化三联体的类似口袋中,结合能处于典型酶–底物复合物的中等有利范围。对两个代表性酶(拟南芥和观赏植物马齿苋属 Matthiola)的更详细后续研究使用分子动力学模拟在虚拟水环境中观察蛋白–底物复合物运动态 100 纳秒。两个体系均保持结构稳定,关键活性位点区域几乎不发生摆动。能量计算显示,紧密的表面间接触(范德华力)是结合的主要贡献者,静电相互作用给予辅助。
这对未来药物与作物意味什么
综合来看,该研究表明来自多样药用植物的查尔酮合酶具有深度保守的催化核心,但在活性通道周围存在精细的结构和理化差异。这些微小差异可能有助于解释为何不同植物产生各异的黄酮“香气组合”,并为工程改造提供潜在手段。尽管本研究基于仍需实验验证的计算模型,但它提供了一个可直接使用的框架,用于挑选有前景的酶变体、设计定点突变以及对新型查尔酮类似化合物进行虚拟筛选。在实际层面上,这或许有助于未来设计富含健康有益黄酮的作物,或简化微生物生产植物源药物的流程。
引用: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
关键词: 查尔酮合酶, 黄酮生物合成, 药用植物, AlphaFold 建模, 酶工程