Clear Sky Science · fr
Caractérisation intégrative structurale et physico-chimique des chalcone synthases d’ plantes médicinales par AlphaFold, docking moléculaire et dynamique moléculaire
Comment les plantes fabriquent des composés naturels utiles
Beaucoup des composés bénéfiques pour la santé présents dans les thés, les herbes et les fruits proviennent d’une enzyme végétale cruciale appelée chalcone synthase. Cet élément moléculaire central permet aux plantes de produire des flavonoïdes — des composés naturels aux propriétés antioxydantes, anti-inflammatoires et parfois anticancéreuses. L’étude décrite ici utilise des outils informatiques modernes, dont AlphaFold, pour examiner la chalcone synthase provenant de diverses plantes médicinales, en posant une question apparemment simple : dans quelle mesure ces enzymes se ressemblent-elles et qu’est-ce que cela implique pour leur exploitation en nutrition, médecine et biotechnologie ?
L’enzyme au début d’une chaîne de montage chargée
La chalcone synthase se situe à l’étape engagée initiale de la chaîne de production des flavonoïdes. Elle capte un précurseur issu du métabolisme courant des plantes et l’assemble avec trois petits blocs de construction pour former la naringénine chalcone, porte d’entrée vers de nombreux flavonoïdes différents. Ces produits en aval colorent les fleurs et les fruits, protègent les feuilles des ultraviolets, défendent contre les microbes et servent de signaux chimiques pour les bactéries du sol. Chez l’humain, ces mêmes molécules sont étudiées pour leurs rôles potentiels dans la santé cardiovasculaire, la protection cérébrale, les thérapies anti-infectieuses et le traitement du cancer. Parce qu’une seule enzyme contrôle la quantité de matière qui entre dans la voie, comprendre sa forme et son comportement à travers les plantes médicinales pourrait ouvrir de nouvelles voies pour augmenter ou réorienter la production de ces composés naturels précieux.
Un panorama à travers les plantes médicinales
Les chercheurs ont rassemblé des séquences protéiques de chalcone synthase provenant de 13 plantes médicinales, plus l’espèce modèle Arabidopsis comme référence. Ils ont aligné ces séquences et construit un arbre de parenté pour évaluer leur degré d’affinité. Malgré l’appartenance des plantes à de nombreuses familles botaniques différentes, les caractéristiques clés de l’enzyme étaient remarquablement conservées : une « triade catalytique » en trois parties d’acides aminés et un court motif signature qui façonnent le tunnel actif où la chimie a lieu. La plupart des différences entre espèces apparaissaient aux extrémités de la protéine ou dans des boucles en surface, et non dans le cœur catalytique. Ce schéma suggère que l’évolution a fortement préservé la réaction de base, tout en autorisant des ajustements subtils susceptibles d’affiner la manière dont chaque plante gère sa chimie des flavonoïdes.
Ce que révèlent les modèles informatiques sur la forme et la stabilité
En utilisant AlphaFold et des outils associés, l’équipe a prédit des structures tridimensionnelles pour chaque enzyme et les a comparées à des structures cristallographiques de haute qualité issues de deux espèces bien étudiées. Les correspondances étaient extrêmement proches — jusqu’à moins d’un dixième de nanomètre en position de l’épine dorsale — confirmant que les modèles prédits sont fiables pour une analyse détaillée. Toutes les versions de la chalcone synthase adoptaient le même repli caractéristique observé dans cette famille d’enzymes, mais elles présentaient de petites variations spécifiques aux espèces dans la forme et l’ouverture du tunnel accueillant le substrat. Des calculs simples ont aussi suggéré des différences modestes dans des traits comme la thermostabilité prédite, la charge globale et le caractère hydrophile versus hydrophobe. Ces propriétés peuvent influencer la facilité de production de chaque enzyme en laboratoire ou leur robustesse à l’intérieur de cellules et d’environnements différents.
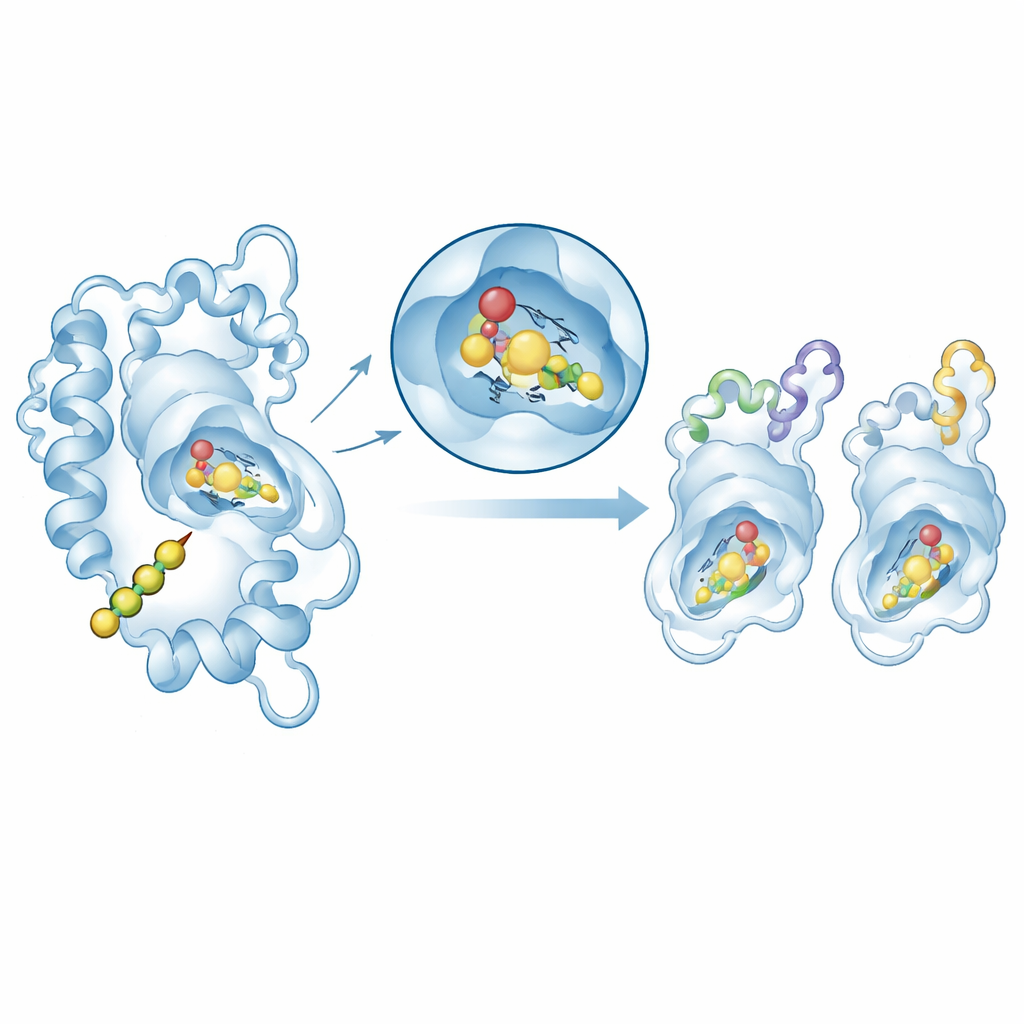
Tester la façon dont les enzymes saisissent leur substrat
Pour relier structure et fonction, les auteurs ont utilisé le docking moléculaire pour positionner la molécule naturelle de départ, le p-coumaroyl-CoA, dans le site actif de modèles sélectionnés de chalcone synthase. Dans tous les cas, le substrat s’insérait dans une poche similaire proche de la triade catalytique conservée, avec des énergies de liaison modérément favorables dans la plage typique des complexes enzyme–substrat. Un approfondissement détaillé sur deux enzymes représentatives — une d’Arabidopsis et une de la plante ornementale Matthiola — a recours à des simulations de dynamique moléculaire pour observer les complexes protéine–substrat évoluer dans une eau virtuelle pendant 100 nanosecondes. Les deux systèmes sont restés structurellement stables et la région clé du site actif a à peine vacillé. Les calculs d’énergie ont montré que le contact serré face-à-face (forces de van der Waals) est le principal contributeur à la liaison, soutenu par des interactions électrostatiques.
Pourquoi cela importe pour les médicaments et les cultures de demain
Dans l’ensemble, les résultats montrent que la chalcone synthase de plantes médicinales diverses partage un noyau catalytique profondément conservé mais diffère par de fins détails structuraux et physico-chimiques autour du tunnel actif. Ces petites différences peuvent aider à expliquer pourquoi différentes plantes produisent des bouquets distincts de flavonoïdes et offrent des leviers potentiels pour l’ingénierie. Bien que tout cela repose sur des modèles informatiques qui nécessitent encore une validation expérimentale, l’étude fournit un cadre prêt à l’emploi pour choisir des variantes enzymatiques prometteuses, concevoir des mutations ciblées et mener des criblages virtuels de nouveaux composés proches des chalcones. Concrètement, cela pourrait un jour aider les scientifiques à concevoir des cultures enrichies en flavonoïdes bénéfiques pour la santé ou à rationaliser la production microbienne de médicaments d’origine végétale.
Citation: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
Mots-clés: chalcone synthase, biosynthèse des flavonoïdes, plantes médicinales, modélisation AlphaFold, ingénierie enzymatique