Clear Sky Science · pt
Caracterização estrutural e físico-química integrativa de enzimas chalcona sintase de plantas medicinais usando AlphaFold, docking molecular e dinâmica molecular
Como as plantas produzem compostos naturais úteis
Muitos dos compostos benéficos à saúde presentes em chás, ervas e frutas provêm de uma única enzima vegetal crucial chamada chalcona sintase. Essa peça molecular ajuda as plantas a sintetizar flavonoides — compostos naturais com atividade antioxidante, anti-inflamatória e até anticancerígena. O estudo por trás deste artigo utiliza ferramentas computacionais modernas, incluindo o AlphaFold, para examinar a chalcona sintase em uma variedade de plantas medicinais, fazendo uma pergunta aparentemente simples: quão semelhantes são essas enzimas e o que isso significa para aproveitá-las na nutrição, medicina e biotecnologia?
A enzima no início de uma linha de montagem movimentada
A chalcona sintase atua na primeira etapa comprometida da via de montagem dos flavonoides. Ela recebe uma molécula inicial derivada do metabolismo vegetal comum e a condensa com três pequenos blocos de construção para formar naringenina chalcona, a porta de entrada para muitos flavonoides diferentes. Esses produtos a jusante colorem flores e frutos, protegem folhas da luz ultravioleta, defendem contra micróbios e atuam como sinais químicos com bactérias do solo. Em humanos, as mesmas moléculas são estudadas por papéis na saúde cardíaca, proteção cerebral, terapias anti-infecciosas e tratamento do câncer. Como essa única enzima controla quanto material entra na via, compreender sua forma e comportamento entre plantas medicinais pode abrir novas maneiras de aumentar ou redirecionar produtos naturais valiosos.
Observando através de plantas medicinais
Os pesquisadores reuniram sequências proteicas de chalcona sintase de 13 plantas medicinais, além da espécie-modelo Arabidopsis como referência. Eles alinharam essas sequências e construíram uma árvore genealógica para ver o grau de relação entre elas. Apesar das plantas pertencerem a várias famílias botânicas diferentes, as características-chave da enzima mostraram-se surpreendentemente conservadas: uma “tríade catalítica” de três aminoácidos e um curto motivo assinatura que moldam o túnel ativo onde a química ocorre. A maioria das diferenças entre espécies apareceu nas extremidades da proteína ou em regiões de loop na superfície, não na maquinaria catalítica central. Esse padrão sugere que a evolução protegeu rigidamente a reação básica, permitindo ajustes sutis que podem sintonizar como cada planta lida com sua química de flavonoides.
O que modelos computacionais revelam sobre forma e estabilidade
Usando AlphaFold e ferramentas relacionadas, a equipe previu estruturas tridimensionais para cada enzima e as comparou com estruturas cristalográficas de alta qualidade de duas espécies bem estudadas. As correspondências foram extremamente próximas — até menos de um décimo de nanômetro na posição do backbone — confirmando que os modelos previstos são confiáveis para análises detalhadas. Todas as versões da chalcona sintase adotaram o mesmo dobramento característico visto nessa família de enzimas, mas exibiram pequenas variações específicas de espécie na forma e na abertura do túnel que acomoda o substrato. Cálculos simples também sugeriram diferenças modestas em características como estabilidade térmica prevista, carga global e caráter hidrofílico versus hidrofóbico. Esses traços podem influenciar com que facilidade cada enzima pode ser produzida em laboratório ou quão robusta ela é dentro de diferentes células e ambientes.
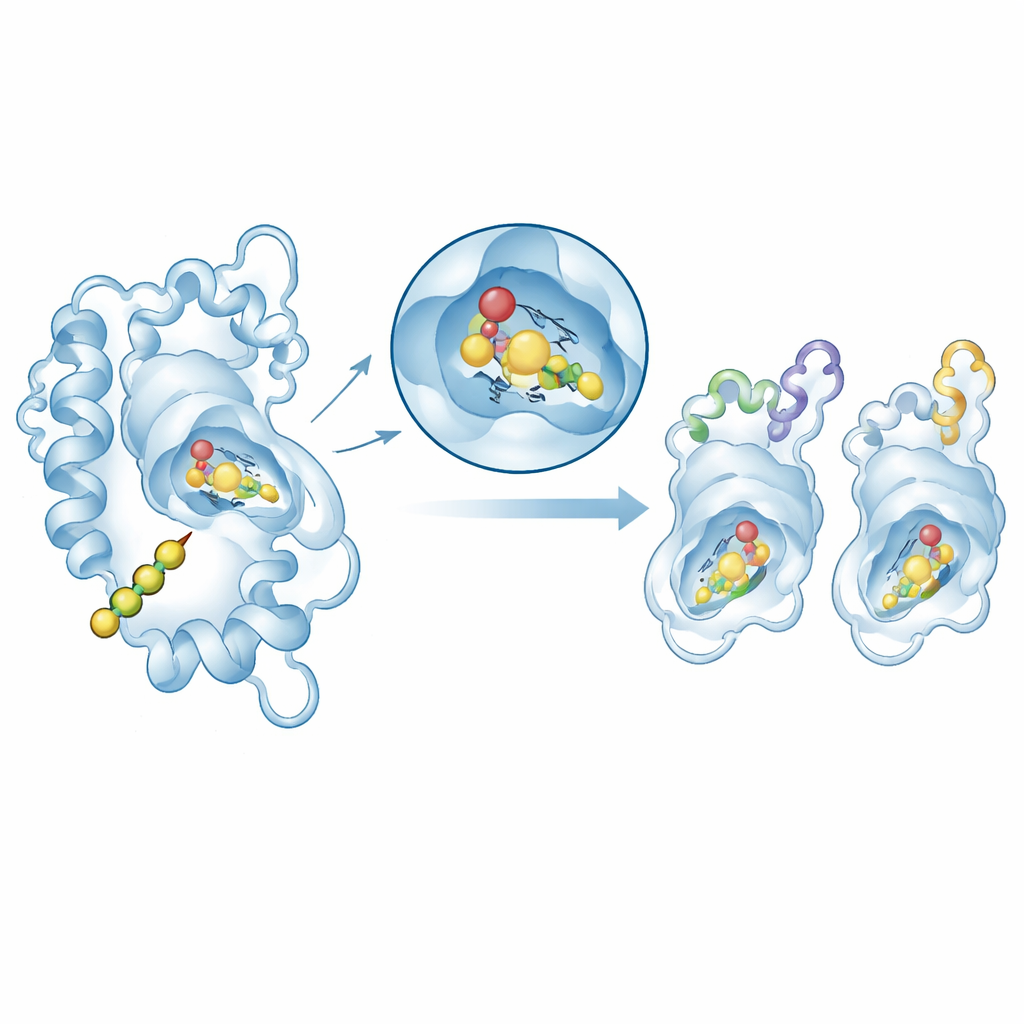
Testando como as enzimas acomodam seu substrato
Para conectar estrutura e função, os autores usaram docking molecular para posicionar a molécula inicial natural, p-cumaroil-CoA, no sítio ativo de modelos selecionados de chalcona sintase. Em todos os casos, o substrato acomodou-se em um bolso similar próximo à tríade catalítica conservada, com energias de ligação moderadamente favoráveis, dentro da faixa típica para complexos enzima–substrato. Um acompanhamento mais detalhado em duas enzimas representativas — uma de Arabidopsis e outra da planta ornamental Matthiola — utilizou simulações de dinâmica molecular para observar os complexos proteína–substrato em água virtual por 100 bilionésimos de segundo. Ambos os sistemas permaneceram estruturalmente estáveis, e a região chave do sítio ativo praticamente não oscilou. Cálculos de energia mostraram que o contato íntimo superfície a superfície (forças de van der Waals) é o principal contribuinte para a interação, apoiado por interações eletrostáticas.
Por que isso importa para futuras medicinas e cultivos
Em conjunto, o trabalho demonstra que a chalcona sintase de plantas medicinais diversas compartilha um núcleo catalítico profundamente conservado, mas difere em detalhes fino-estruturais e físico-químicos ao redor do túnel ativo. Essas pequenas diferenças podem ajudar a explicar por que plantas distintas produzem buquês diferentes de flavonoides e oferecem alavancas potenciais para engenharia. Embora tudo aqui se baseie em modelos computacionais que ainda precisam de testes experimentais, o estudo fornece um arcabouço pronto para escolher variantes de enzimas promissoras, projetar mutações direcionadas e rodar triagens virtuais de novos compostos semelhantes a chalconas. Em termos práticos, isso poderia um dia ajudar cientistas a projetar cultivos com flavonoides aprimorados promotores de saúde ou a otimizar a produção microbiana de fármacos derivados de plantas.
Citação: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
Palavras-chave: chalcona sintase, biossíntese de flavonoides, plantas medicinais, modelagem AlphaFold, engenharia de enzimas