Clear Sky Science · nl
Integratieve structurele en fysisch‑chemische karakterisering van chalcone synthase‑enzymen uit medicinale planten met AlphaFold, moleculair docken en moleculaire dynamica
Hoe planten nuttige natuurlijke stoffen maken
Veel van de gezondheidsbevorderende verbindingen in theeën, kruiden en vruchten worden gevormd dankzij één cruciaal planteneiwit, chalcone synthase. Deze moleculaire krachtpatser helpt planten bij de productie van flavonoïden—natuurlijke stoffen met antioxidant-, ontstekingsremmende en zelfs antikankereigenschappen. De studie achter dit artikel gebruikt moderne computationele middelen, waaronder AlphaFold, om chalcone synthase uit een reeks medicinale planten te onderzoeken en stelt een op het eerste gezicht eenvoudige vraag: hoe gelijk zijn deze enzymen, en wat betekent dat voor het benutten ervan in voeding, geneeskunde en biotechnologie?
Het enzym aan het begin van een drukke productielijn
Chalcone synthase zit op de eerste toegewijde stap van de flavonoïde‑productielijn. Het neemt een startmolecuul uit het algemene plantenmetabolisme en verbindt dit met drie kleine bouwstenen om naringenine‑chalcone te vormen, de poort naar veel verschillende flavonoïden. Deze downstream‑producten kleuren bloemen en vruchten, beschermen bladeren tegen ultraviolette straling, verdedigen tegen microben en fungeren als chemische signalen naar bodem‑bacteriën. Bij mensen worden dezelfde moleculen bestudeerd vanwege hun mogelijke rol bij hartgezondheid, hersenbescherming, anti‑infectieuze therapieën en kankerbehandeling. Omdat dit ene enzym bepaalt hoeveel materiaal de route in gaat, kan inzicht in de vorm en het gedrag ervan over medicinale planten heen nieuwe mogelijkheden openen om waardevolle natuurlijke producten te versterken of om te leiden.
Kijken over medicinale planten heen
De onderzoekers verzamelden eiwitsequenties van chalcone synthase uit 13 medicinale planten, plus de modelsoort Arabidopsis als referentie. Ze wezen deze sequenties op elkaar uit en bouwden een familieboom om te zien hoe verwant ze zijn. Ondanks dat de planten uit veel verschillende botanische families komen, waren de sleutelkenmerken van het enzym opvallend behouden: een driedelige ‘‘katalytische triade’’ van aminozuren en een kort signatuurmotief die de actieve tunnel vormen waar de chemie plaatsvindt. De meeste verschillen tussen soorten traden op aan de uiteinden van het eiwit of in lusregio’s aan het oppervlak, niet in de kern van het katalytische apparaat. Dit patroon suggereert dat de evolutie de basale reactie streng heeft beschermd, terwijl subtiele aanpassingen zijn toegestaan die kunnen bijsturen hoe elke plant zijn flavonoïdechemie regelt.
Wat computermodellen onthullen over vorm en stabiliteit
Met AlphaFold en verwante tools voorspelden de onderzoekers driedimensionale structuren voor elk enzym en vergeleken die met hoogwaardige kristalstructuren van twee goed bestudeerde soorten. De overeenkomsten waren buitengewoon nauw—tot minder dan een tiende van een nanometer in de ruggraatpositie—wat bevestigt dat de voorspelde modellen betrouwbaar zijn voor gedetailleerde analyse. Alle varianten van chalcone synthase namen dezelfde karakteristieke vouwing aan die kenmerkend is voor deze enzymfamilie, maar ze vertoonden kleine, soortspecifieke variaties in de vorm en de openheid van de tunnel die het substraat vasthoudt. Eenvoudige berekeningen suggereerden ook bescheiden verschillen in eigenschappen zoals voorspelde thermostabiliteit, totale lading en waterminnende versus waterafstotende kenmerken. Deze eigenschappen kunnen beïnvloeden hoe gemakkelijk elk enzym in het laboratorium geproduceerd kan worden of hoe robuust het is binnen verschillende cellen en omgevingen.
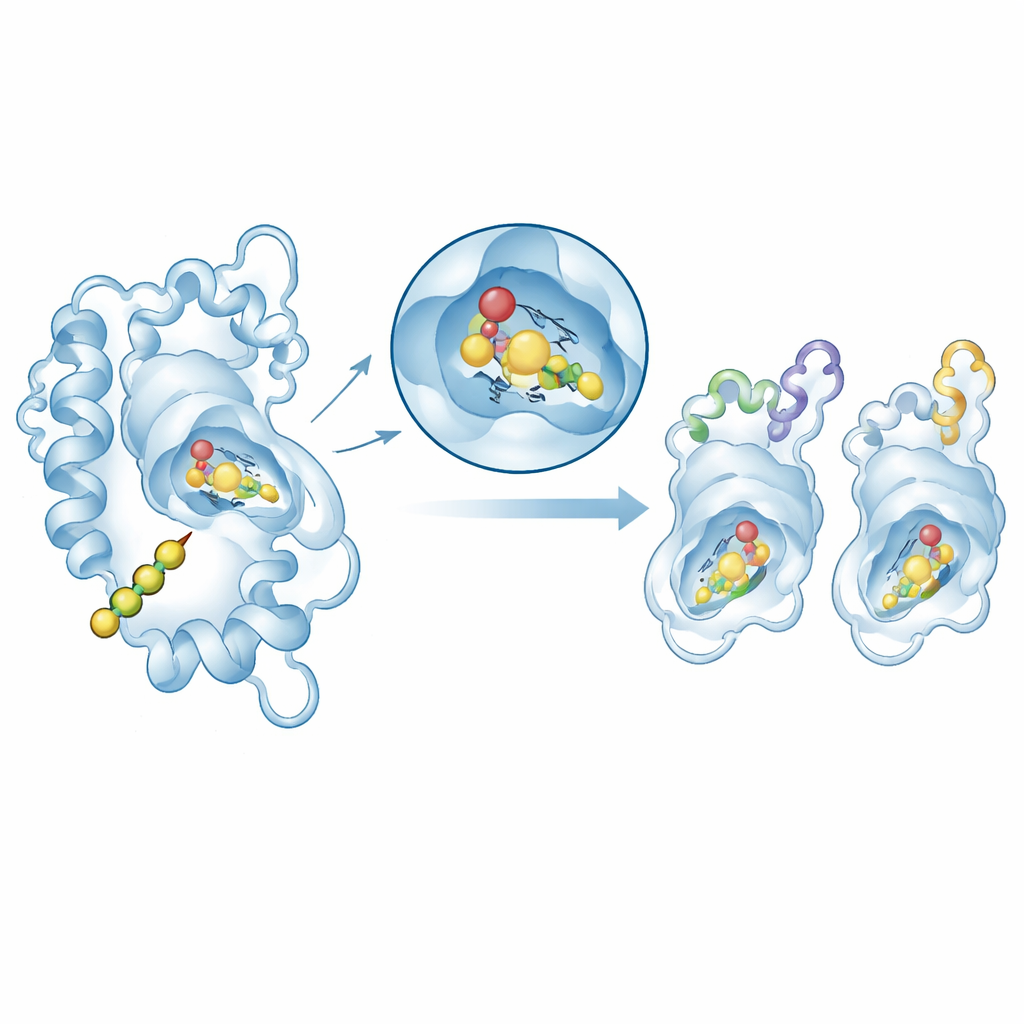
Testen hoe de enzymen hun substraat vastgrijpen
Om structuur aan functie te koppelen, plaatsten de auteurs met moleculair docken het natuurlijke startmolecuul, p‑coumaroyl‑CoA, in het actieve domein van geselecteerde chalcone synthase‑modellen. In alle gevallen nestelde het substraat zich in een vergelijkbaar pocket nabij de geconserveerde katalytische triade, met matig gunstige bindingsenergieën die binnen het bereik vallen dat typisch is voor enzym‑substraatcomplexen. Een meer gedetailleerde vervolgstudie op twee representatieve enzymen—één van Arabidopsis en één van de sierplant Matthiola—gebruikt moleculaire dynamicasimulaties om de eiwit‑substraatcomplexen gedurende 100 miljardsten van een seconde in virtueel water te observeren. Beide systemen bleven structureel stabiel en het sleutelgebied in het actieve centrum wiebelde nauwelijks. Energieberekeningen toonden aan dat nauw contact van oppervlak tot oppervlak (van der Waals‑krachten) de belangrijkste bijdrage aan de binding levert, ondersteund door elektrostatische interacties.
Waarom dit belangrijk is voor toekomstige medicijnen en gewassen
Samengevat laat het werk zien dat chalcone synthase uit diverse medicinale planten een diep geconserveerde katalytische kern deelt, maar dat er verschillen bestaan in fijne structurele en fysisch‑chemische details rond de actieve tunnel. Die kleine verschillen kunnen helpen verklaren waarom verschillende planten verschillende bloemlezingen van flavonoïden produceren, en ze bieden potentiële aangrijpingspunten voor engineering. Hoewel alles hier gebaseerd is op computermodellen die nog experimenteel getest moeten worden, levert de studie een kant‑en‑klaar kader voor het kiezen van veelbelovende enzymvarianten, het ontwerpen van gerichte mutaties en het uitvoeren van virtuele screens van nieuwe chalcone‑achtige verbindingen. In praktische zin kan dat op termijn onderzoekers helpen gewassen te ontwerpen met verbeterde gezondheidsbevorderende flavonoïden of de microbiele productie van plantaardige geneesmiddelen te vereenvoudigen.
Bronvermelding: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
Trefwoorden: chalcone synthase, flavonoïde‑biosynthese, medicinale planten, AlphaFold‑modellering, enzymengineering