Clear Sky Science · de
Integrative strukturelle und physikochemische Charakterisierung von Chalcon-Synthase-Enzymen aus Heilpflanzen mithilfe von AlphaFold, molekularem Docking und Molekulardynamik
Wie Pflanzen nützliche Naturstoffe herstellen
Viele der gesundheitsfördernden Verbindungen in Tees, Kräutern und Früchten stammen von einem einzigen, zentralen Pflanzenenzym: der Chalcon-Synthase. Diese molekulare Arbeitspferd hilft Pflanzen bei der Herstellung von Flavonoiden – natürlichen Substanzen mit antioxidativen, entzündungshemmenden und teils auch krebshemmenden Eigenschaften. Die Studie hinter diesem Artikel nutzt moderne Computerwerkzeuge, darunter AlphaFold, um Chalcon-Synthasen aus verschiedenen Heilpflanzen zu untersuchen und eine auf den ersten Blick einfache Frage zu stellen: Wie ähnlich sind diese Enzyme, und was bedeutet das für ihre Nutzung in Ernährung, Medizin und Biotechnologie?
Das Enzym am Beginn einer geschäftigen Produktionslinie
Die Chalcon-Synthase steht am ersten festgelegten Schritt der Flavonoid-Biosynthese. Sie nimmt ein Startermolekül aus der üblichen Pflanzenstoffwechselweg und verknüpft es mit drei kleinen Bausteinen zu Naringenin-Chalcon, dem Tor zu vielen verschiedenen Flavonoiden. Diese nachgeschalteten Produkte färben Blüten und Früchte, schützen Blätter vor ultraviolettem Licht, verteidigen gegen Mikroben und fungieren als chemische Signale mit Bodenbakterien. Beim Menschen werden dieselben Moleküle hinsichtlich Herzgesundheit, Schutz des Gehirns, antiinfektiöser Therapien und Krebstherapien untersucht. Da dieses eine Enzym steuert, wie viel Material in den Weg einfließt, könnte das Verständnis seiner Struktur und seines Verhaltens in Heilpflanzen neue Wege eröffnen, wertvolle Naturstoffe zu steigern oder umzulenken.
Blick über verschiedene Heilpflanzen hinweg
Die Forscher sammelten Proteinsequenzen der Chalcon-Synthase aus 13 Heilpflanzen sowie aus der Modellpflanze Arabidopsis als Referenz. Sie alignierten diese Sequenzen und erstellten einen Stammbaum, um Verwandtschaftsverhältnisse zu ermitteln. Obwohl die Pflanzen aus vielen verschiedenen Pflanzenfamilien stammen, waren die Schlüsselfunktionen des Enzyms auffallend konserviert: eine dreiteilige „katalytische Triade“ aus Aminosäuren und ein kurzes Signaturmotiv, die den aktiven Tunnel formen, in dem die Chemie stattfindet. Die meisten Unterschiede zwischen den Arten traten an den Proteinenden oder in Schleifenregionen an der Oberfläche auf, nicht in der Kernkatalysmaschinerie. Dieses Muster deutet darauf hin, dass die Evolution die Grundreaktion streng geschützt hat, während sie subtile Anpassungen zulässt, die das Flavonoidmanagement jeder Art feintunen könnten.
Was Computermodelle über Form und Stabilität verraten
Mithilfe von AlphaFold und verwandten Werkzeugen sagten die Autoren die dreidimensionalen Strukturen jedes Enzyms voraus und verglichen sie mit hochwertigen Kristallstrukturen aus zwei gut untersuchten Arten. Die Übereinstimmungen waren extrem eng – bis auf weniger als ein Zehntel Nanometer in der Rückgratposition – und bestätigen, dass die vorhergesagten Modelle für detaillierte Analysen zuverlässig sind. Alle Varianten der Chalcon-Synthase nahmen die charakteristische Faltung an, die für diese Enzymfamilie typisch ist, zeigten jedoch kleine, artspezifische Unterschiede in Form und Offenheit des Tunnels, der das Substrat aufnimmt. Einfache Berechnungen deuteten außerdem auf modest Unterschiede bei Eigenschaften wie vorhergesagter Thermostabilität, Gesamtladung und hydrophilen versus hydrophoben Charakter hin. Diese Merkmale können beeinflussen, wie leicht sich ein Enzym im Labor produzieren lässt oder wie robust es in verschiedenen Zellen und Umgebungen ist.
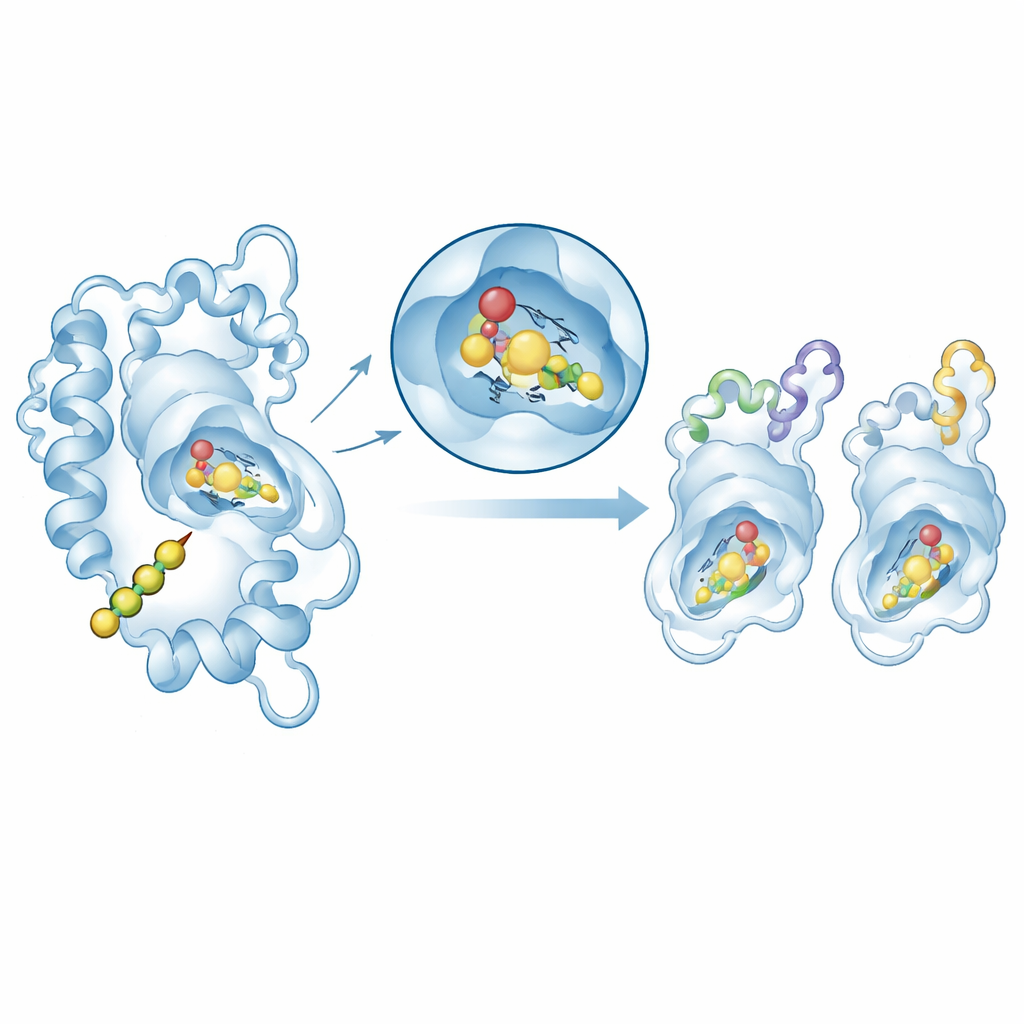
Prüfung, wie die Enzyme ihr Substrat fassen
Um Struktur und Funktion zu verbinden, setzten die Autoren molekulares Docking ein, um das natürliche Startermolekül p-Coumaroyl-CoA in die aktive Seite ausgewählter Chalcon-Synthase-Modelle zu platzieren. In allen Fällen nestelte sich das Substrat in eine ähnliche Tasche nahe der konservierten katalytischen Triade, mit mäßig günstigen Bindungsenergien, die im Bereich typischer Enzym–Substrat-Komplexe liegen. Eine detailliertere Nachfolgeuntersuchung an zwei repräsentativen Enzymen – einem aus Arabidopsis und einem aus der Zierpflanze Matthiola – nutzte Molekulardynamik-Simulationen, um die Protein–Substrat-Komplexe für 100 Nanosekunden in virtuellem Wasser zu beobachten. Beide Systeme blieben strukturell stabil, und die Schlüsselregion des aktiven Zentrums schwankte kaum. Energieanalysen zeigten, dass eng anliegender Oberflächenkontakt (van-der-Waals-Kräfte) der Hauptbeitrag zur Bindung ist, unterstützt durch elektrostatische Wechselwirkungen.
Warum das für zukünftige Arzneien und Nutzpflanzen wichtig ist
Zusammengefasst zeigt die Arbeit, dass Chalcon-Synthasen aus verschiedenen Heilpflanzen einen tief konservierten katalytischen Kern teilen, sich jedoch in feinen strukturellen und physikochemischen Details rund um den aktiven Tunnel unterscheiden. Diese kleinen Unterschiede können helfen zu erklären, warum verschiedene Pflanzen unterschiedliche Flavonoidmischungen produzieren, und sie bieten potenzielle Ansatzpunkte für das Engineering. Obwohl all dies auf Computermodellen beruht, die noch experimentell überprüft werden müssen, liefert die Studie ein gebrauchsfertiges Rahmenwerk zur Auswahl vielversprechender Enzymvarianten, zum Entwurf gezielter Mutationen und zum Durchführen virtueller Screenings neuer chalconähnlicher Verbindungen. Praktisch könnte das eines Tages helfen, Pflanzen mit verstärkten gesundheitsfördernden Flavonoiden zu entwickeln oder die mikrobielle Produktion pflanzlicher Arzneistoffe zu optimieren.
Zitation: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
Schlüsselwörter: Chalcon-Synthase, Flavonoid-Biosynthese, Heilpflanzen, AlphaFold-Modellierung, Enzymtechnik