Clear Sky Science · pl
Integralna strukturalna i fizykochemiczna charakterystyka enzymów chalcone synthase z roślin leczniczych przy użyciu AlphaFold, dokowania molekularnego i dynamiki molekularnej
Jak rośliny wytwarzają użyteczne związki naturalne
Wiele z korzystnych dla zdrowia związków obecnych w herbatach, ziołach i owocach pochodzi z jednego kluczowego enzymu roślinnego nazwanego chalcone synthase. Ten molekularny „robotnik” pomaga roślinom produkować flawonoidy — naturalne związki o działaniu przeciwutleniającym, przeciwzapalnym, a nawet przeciwnowotworowym. Badanie opisane w tym artykule wykorzystuje nowoczesne narzędzia komputerowe, w tym AlphaFold, do analizy chalcone synthase z różnych roślin leczniczych, stawiając pozornie proste pytanie: jak podobne są te enzymy i co to oznacza dla wykorzystania ich w żywieniu, medycynie i biotechnologii?
Enzym na początku zatłoczonej linii montażowej
Chalcone synthase zajmuje pierwsze etap zaangażowany w linii montażowej flawonoidów. Pobiera cząsteczkę startową pochodzącą z podstawowego metabolizmu roślin i łączy ją z trzema małymi blokami budulcowymi, tworząc naringenin chalcone — bramę do wielu różnych flawonoidów. Produkty powstałe dalej barwią kwiaty i owoce, chronią liście przed promieniowaniem UV, bronią przed mikroorganizmami i pełnią rolę sygnałów chemicznych w relacjach z bakteriami glebowymi. U ludzi te same związki są badane pod kątem wpływu na zdrowie serca, ochronę mózgu, terapie przeciwzakaźne oraz leczenie raka. Ponieważ ten pojedynczy enzym kontroluje, ile materiału trafia do szlaku, zrozumienie jego kształtu i zachowania w różnych roślinach leczniczych może otworzyć nowe sposoby zwiększania lub przekierowywania produkcji cennych naturalnych produktów.
Przegląd roślin leczniczych
Naukowcy zebrali sekwencje białkowe chalcone synthase z 13 roślin leczniczych oraz sekwencję modelowego gatunku Arabidopsis jako punkt odniesienia. Wyrównali te sekwencje i zbudowali drzewo filogenetyczne, aby ocenić ich powiązania. Pomimo że rośliny pochodziły z wielu różnych rodzin botanicznych, kluczowe cechy enzymu były zaskakująco zachowane: trójczłonowy „triada katalityczna” aminokwasów oraz krótki motyw sygnaturowy kształtujący aktywny tunel, w którym zachodzi reakcja. Większość różnic między gatunkami pojawiała się na końcach białka lub w pętlach na jego powierzchni, a nie w rdzeniu katalitycznym. Ten wzorzec sugeruje, że ewolucja ściśle chroni podstawową reakcję, jednocześnie pozwalając na drobne adaptacje, które mogą modulować sposób, w jaki każda roślina zarządza swoją chemią flawonoidów.
Co modele komputerowe ujawniają o kształcie i stabilności
Wykorzystując AlphaFold i powiązane narzędzia, zespół przewidział trójwymiarowe struktury dla każdego enzymu i porównał je z wysokiej jakości strukturami krystalicznymi z dwóch dobrze zbadanych gatunków. Dopasowania były wyjątkowo bliskie — do wartości poniżej jednej dziesiątej nanometra w położeniu łańcucha głównego — potwierdzając, że przewidywane modele są wiarygodne do analizy szczegółowej. Wszystkie warianty chalcone synthase przyjmowały ten sam charakterystyczny fałd obserwowany w tej rodzinie enzymów, lecz wykazywały drobne, specyficzne dla gatunku różnice w kształcie i stopniu otwartości tunelu mieszczącego substrat. Proste obliczenia sugerowały również umiarkowane różnice w cechach takich jak przewidywana termostabilność, ładunek całkowity oraz hydrofilowość kontra hydrofobowość. Te właściwości mogą wpływać na to, jak łatwo dany enzym można wyprodukować w laboratorium lub jak stabilny jest w różnych komórkach i środowiskach.
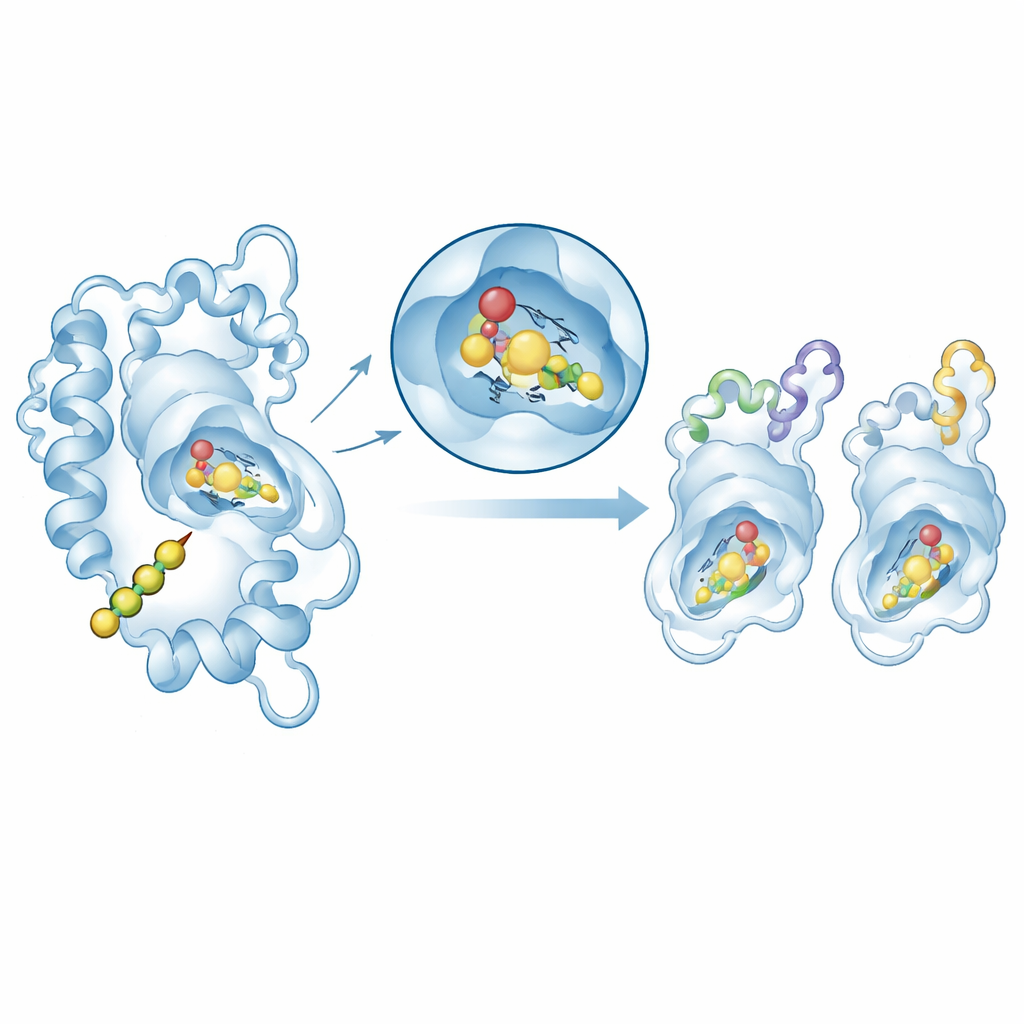
Testowanie, jak enzymy chwytają swój substrat
Aby powiązać strukturę z funkcją, autorzy użyli dokowania molekularnego, aby umieścić naturalną cząsteczkę startową, p-cumaroyl-CoA, w miejscu aktywnym wybranych modeli chalcone synthase. We wszystkich przypadkach substrat zagnieździł się w podobnej kieszeni w pobliżu zachowanej triady katalitycznej, z umiarkowanie korzystnymi energiami wiązania mieszczącymi się w zakresie typowym dla kompleksów enzym–substrat. Bardziej szczegółowa analiza dwóch reprezentatywnych enzymów — jednego z Arabidopsis i jednego z ozdobnej rośliny Matthiola — użyła symulacji dynamiki molekularnej, aby obserwować ruch kompleksów białko–substrat w wirtualnej wodzie przez 100 nanosekund (100 miliardowych części sekundy). Oba systemy pozostały strukturalnie stabilne, a kluczowy region miejsca aktywnego tylko minimalnie się poruszał. Obliczenia energetyczne wykazały, że ciasny kontakt powierzchnia–powierzchnia (siły van der Waalsa) jest głównym wkładem do wiązania, wspieranym przez oddziaływania elektrostatyczne.
Dlaczego ma to znaczenie dla przyszłych leków i upraw
Podsumowując, praca pokazuje, że chalcone synthase z różnorodnych roślin leczniczych dzieli głęboko zachowany rdzeń katalityczny, lecz różni się w subtelnych szczegółach strukturalnych i fizykochemicznych wokół aktywnego tunelu. Te małe różnice mogą pomóc wyjaśnić, dlaczego różne rośliny produkują odrębne bukiety flawonoidów, i oferują potencjalne dźwignie do inżynierii. Chociaż wszystko opisane tutaj opiera się na modelach komputerowych, które nadal wymagają testów eksperymentalnych, badanie dostarcza gotowego ramienia roboczego do wyboru obiecujących wariantów enzymów, projektowania ukierunkowanych mutacji i prowadzenia wirtualnych przesiewów nowych związków chalconopodobnych. W praktycznym ujęciu może to kiedyś pomóc naukowcom projektować uprawy o zwiększonej zawartości korzystnych flawonoidów lub usprawnić mikrobiologiczną produkcję leków pochodzenia roślinnego.
Cytowanie: Muflikhati, Z., Mangindaan, D. & Enyi, C.U. Integrative structural and physicochemical characterization of chalcone synthase enzymes from medicinal plants using AlphaFold, molecular docking, and molecular dynamics. Sci Rep 16, 14624 (2026). https://doi.org/10.1038/s41598-026-45190-0
Słowa kluczowe: chalcone synthase, biosynteza flawonoidów, rośliny lecznicze, modelowanie AlphaFold, inżynieria enzymów