Clear Sky Science · zh
阿达帕林(RAR激动剂)通过RARβ介导的信号通路调节巨噬细胞极化,从而发挥抗炎作用
为何一种皮肤药物关系到全身健康
阿达帕林最为人所知的是一种局部治疗痤疮的凝胶,但这项研究表明它可能具有更广泛的作用。研究人员显示,在小鼠中口服给药时,阿达帕林能抑制过度活跃的免疫细胞、保护肝脏免受严重感染和高脂饮食损伤,甚至在败血症模型中改善存活率。对于关心如何将常见皮肤科药物重新定位用于对抗威胁生命的炎症和代谢疾病的读者,这项工作提供了一个有趣的视角。
能造成伤害也能促愈的前线免疫细胞
我们的身体依赖巨噬细胞——免疫系统中巡逻的“大吃者”——来探测病原、清除碎屑并协调炎症反应。这些细胞可以采取两种广义模式。在M1或促炎模式下,它们产生大量攻击性分子,帮助杀灭微生物,但如果失控也会损伤自身组织。在M2或抗炎与修复模式下,它们有助于消除炎症并支持愈合。在肥胖、败血症和脂肪肝疾病中,巨噬细胞倾向于向M1状态偏移,助长慢性低度炎症,进而促成胰岛素抵抗和组织瘢痕化。因此,寻找将巨噬细胞引导回平衡或偏向M2状态的方法,成为重要的治疗目标。
免疫细胞内与维生素A相关的开关
维生素A及其衍生物(统称视黄醇类)通过与细胞内的视黄酸受体(RARs)结合来调控许多基因。阿达帕林是一种合成视黄醇类,强烈作用于其中一种受体——RARβ。作者探讨了用阿达帕林激活RARβ是否能重新调节暴露于脂多糖(LPS,一种能触发强烈炎症反应的细菌成分)的巨噬细胞。在小鼠巨噬细胞系中,LPS明显增加了典型的炎性信使和酶。加入微量阿达帕林后,这些信号以浓度依赖的方式被抑制,同时与温和、修复相关的M2状态有关的标志物得到增强。流式细胞术分析证实,细胞群体的表面表型从更像M1的模式向更像M2的模式转移。
关闭炎症电路并开启修复程序
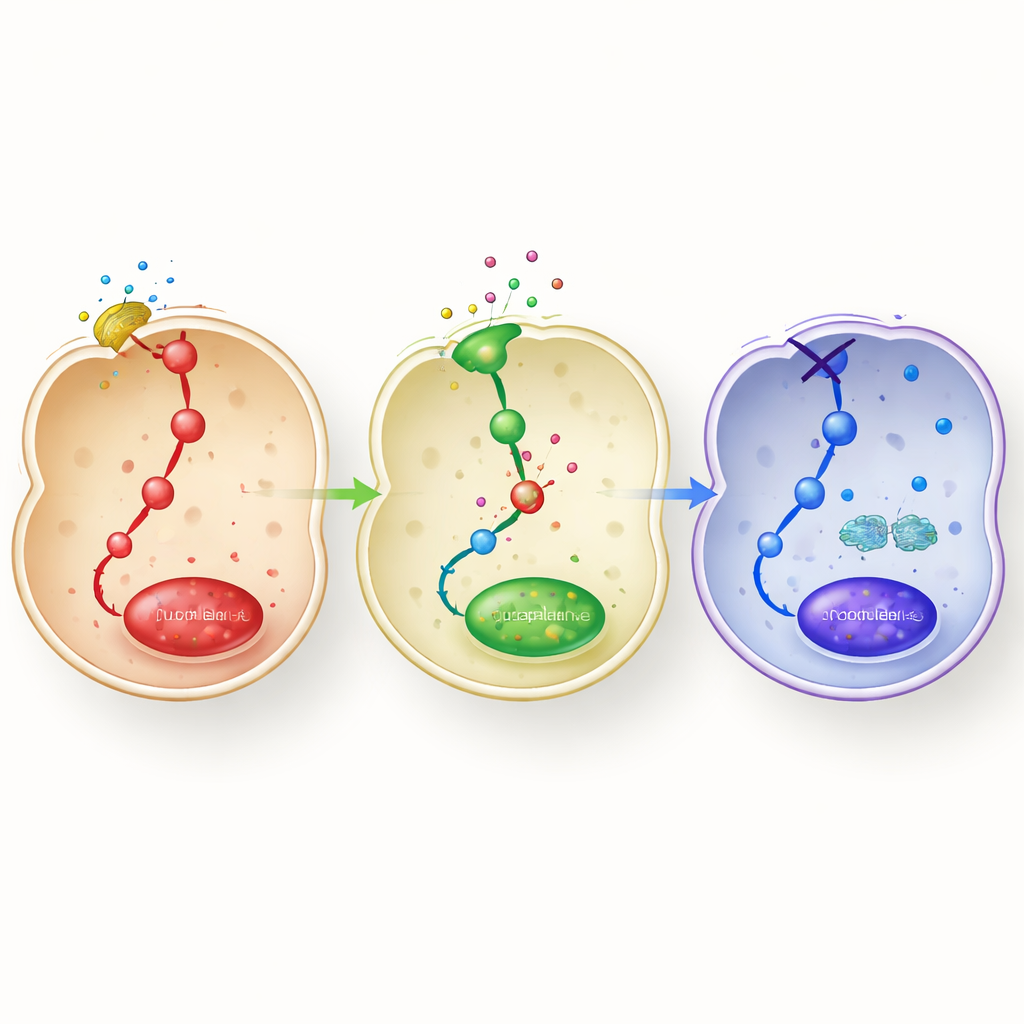
深入研究表明,团队绘制了阿达帕林如何重接巨噬细胞内分子电路图。LPS通常会激活若干激酶通路(MAPK和PI3K/Akt)以及炎症主开关NF‑κB,后者进入细胞核以激活炎症基因。阿达帕林显著降低了这些通路的激活并限制了NF‑κB进入细胞核。与此同时,它增加了STAT3的磷酸化——一种已知促进M2型行为的信号蛋白。当研究者通过基因手段降低RARβ水平,或用选择性拮抗剂阻断其功能时,阿达帕林的这些效应大多消失:炎性标志物再次升高,抑制性M2标志下降,信号通路重新被激活。这将RARβ定位为阿达帕林发挥双重作用的关键内部开关——一方面抑制炎症回路,另一方面促进修复程序。
从培养皿到病变肝脏与整只动物
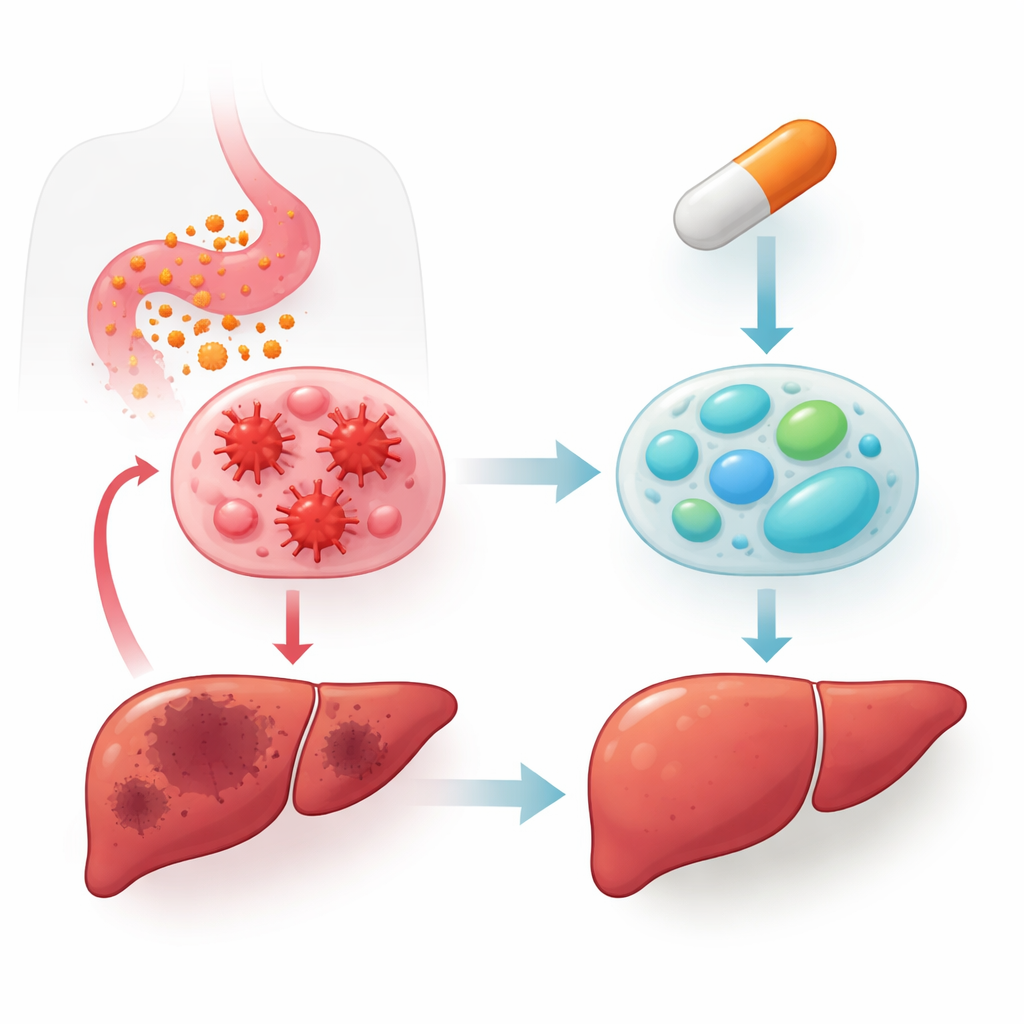
为了检验这些细胞培养中的发现是否在活体中具有意义,作者采用了急性和慢性炎症的小鼠模型。在一项严重的LPS诱导败血症模型中,口服阿达帕林降低了血液和肝脏中的炎性细胞因子,减少了肝损伤标志物,改善了显微镜下的肝组织结构,并将几近致死的存活率显著提升至较高水平。在以高脂饮食使小鼠肥胖的模型中,数周口服阿达帕林减少了肝脏炎性标志物,增加了与M2相关的标志物,抑制了相同激酶通路的活化,并减轻了与脂肪肝和纤维化相关的脂肪与胶原沉积。在这些模型中,肝脏中RARβ水平选择性上升,进一步强化了该受体的中心作用。
对未来治疗的潜在意义
简而言之,该研究表明阿达帕林可作为巨噬细胞的内部调节器:通过激活RARβ并抑制下游信号级联反应,它既抑低破坏性的炎性反应,又增强修复性反应。在小鼠中,这表现为对致命败血症的保护、肝脏炎症的减轻以及肥胖相关脂肪肝的瘢痕减少。尽管阿达帕林目前仅被批准用于皮肤治疗,但这些发现提出了这样的可能性:若今后在人类中证实安全且剂量可控,系统性使用阿达帕林或可通过重新教育机体自身的免疫细胞,成为治疗炎症和代谢性疾病的一种策略。
引用: Lee, N.H., Choi, M.J., Ji, S.M. et al. Adapalene, an RAR agonist, exerts anti-inflammatory effects by regulating macrophage polarization through RAR\(\upbeta\)-mediated signaling pathways. Sci Rep 16, 11385 (2026). https://doi.org/10.1038/s41598-026-44454-z
关键词: 巨噬细胞极化, 阿达帕林, 炎症, 败血症, 脂肪肝疾病