Clear Sky Science · fr
L’adapalène, agoniste des RAR, exerce des effets anti‑inflammatoires en régulant la polarisation des macrophages via des voies de signalisation médiées par RAR $$\upbeta$$
Pourquoi un médicament pour la peau importe pour la santé de tout l’organisme
L’adapalène est mieux connu comme un gel topique contre l’acné, mais cette étude suggère qu’il pourrait discrètement avoir des pouvoirs beaucoup plus larges. Les auteurs montrent que, administré par voie orale chez la souris, l’adapalène peut calmer des cellules immunitaires hyperactives, protéger le foie contre une infection sévère et les dommages d’un régime riche en graisses, et même améliorer la survie dans un modèle de septicémie. Pour les lecteurs qui s’intéressent à la façon dont un médicament dermatologique courant pourrait être réutilisé pour combattre des inflammations potentiellement mortelles et des maladies métaboliques, ce travail ouvre une fenêtre intrigante.
Des cellules immunitaires de première ligne qui peuvent nuire ou guérir
Notre organisme dépend des macrophages — ces « grands mangeurs » mobiles du système immunitaire — pour détecter les germes, éliminer les débris et orchestrer l’inflammation. Ces cellules peuvent adopter deux grands modes. En mode M1, ou pro‑inflammatoire, elles sécrètent des molécules agressives qui aident à tuer les microbes mais peuvent aussi endommager nos propres tissus si elles restent incontrôlées. En mode M2, anti‑inflammatoire et réparateur, elles contribuent à résoudre l’inflammation et à soutenir la guérison. Dans l’obésité, la septicémie et la stéatose hépatique, les macrophages basculent vers l’état M1, alimentant une inflammation chronique de faible intensité qui contribue à la résistance à l’insuline et à la fibrose tissulaire. Trouver des moyens de pousser les macrophages vers un état plus équilibré ou pro‑M2 est donc un objectif thérapeutique majeur.
Un interrupteur lié à la vitamine A à l’intérieur des cellules immunitaires
La vitamine A et ses apparentés, appelés rétinoïdes, contrôlent de nombreux gènes en se liant aux récepteurs de l’acide rétinoïque (RAR) à l’intérieur des cellules. L’adapalène est un rétinoïde synthétique qui cible fortement l’un de ces récepteurs, RARβ. Les auteurs ont étudié si l’activation de RARβ par l’adapalène pouvait réorienter des macrophages exposés au lipopolysaccharide (LPS), un composant bactérien qui déclenche une puissante réponse inflammatoire. Dans des cellules macrophagiques de souris, le LPS augmentait fortement les médiateurs et enzymes inflammatoires classiques. L’ajout de très faibles quantités d’adapalène a atténué ces signaux de manière dépendante de la concentration, tout en renforçant les marqueurs associés à l’état M2, plus doux et orienté vers la réparation tissulaire. Des analyses en cytométrie en flux ont confirmé que la population cellulaire s’était déplacée d’un profil de surface proche de M1 vers un profil proche de M2.
Éteindre les circuits inflammatoires et activer la réparation
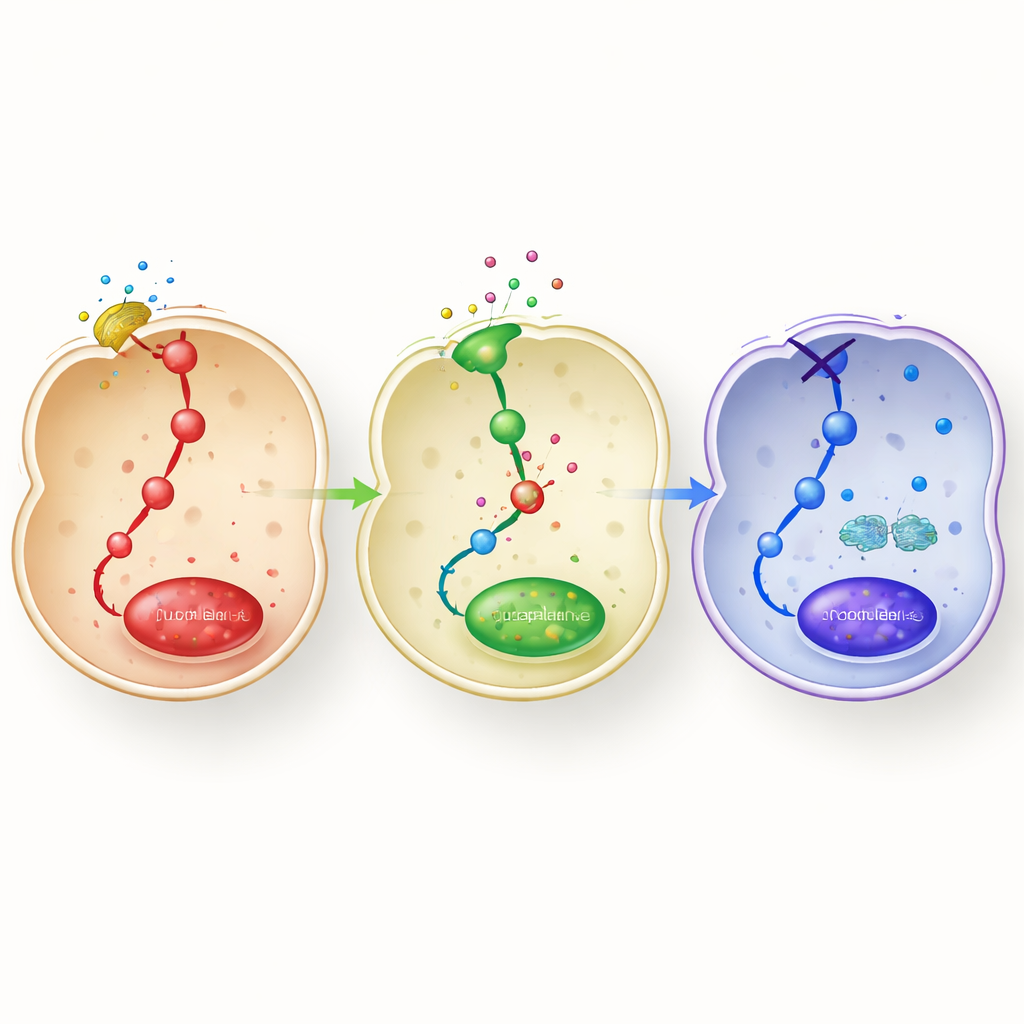
En approfondissant, l’équipe a cartographié comment l’adapalène reprogramme les circuits moléculaires à l’intérieur des macrophages. Le LPS active normalement plusieurs voies de kinases (MAPK et PI3K/Akt) ainsi que l’interrupteur inflammatoire maître NF‑κB, qui migre ensuite vers le noyau pour activer des gènes inflammatoires. L’adapalène a considérablement réduit l’activation de ces voies et limité l’entrée de NF‑κB dans le noyau. Parallèlement, il augmentait la phosphorylation de STAT3, une protéine de signalisation connue pour favoriser le comportement de type M2. Lorsque les chercheurs ont réduit les niveaux de RARβ par des outils génétiques, ou l’ont bloqué avec un antagoniste sélectif, l’adapalène a pour l’essentiel perdu ces effets : les marqueurs inflammatoires ont de nouveau augmenté, les marqueurs calmants de type M2 ont chuté et les voies de signalisation se sont réactivées. Cela identifie RARβ comme l’interrupteur interne clé par lequel l’adapalène exerce sa double action — atténuer les circuits inflammatoires tout en promouvant les programmes de réparation.
Des boîtes de culture aux foies malades et aux animaux entiers
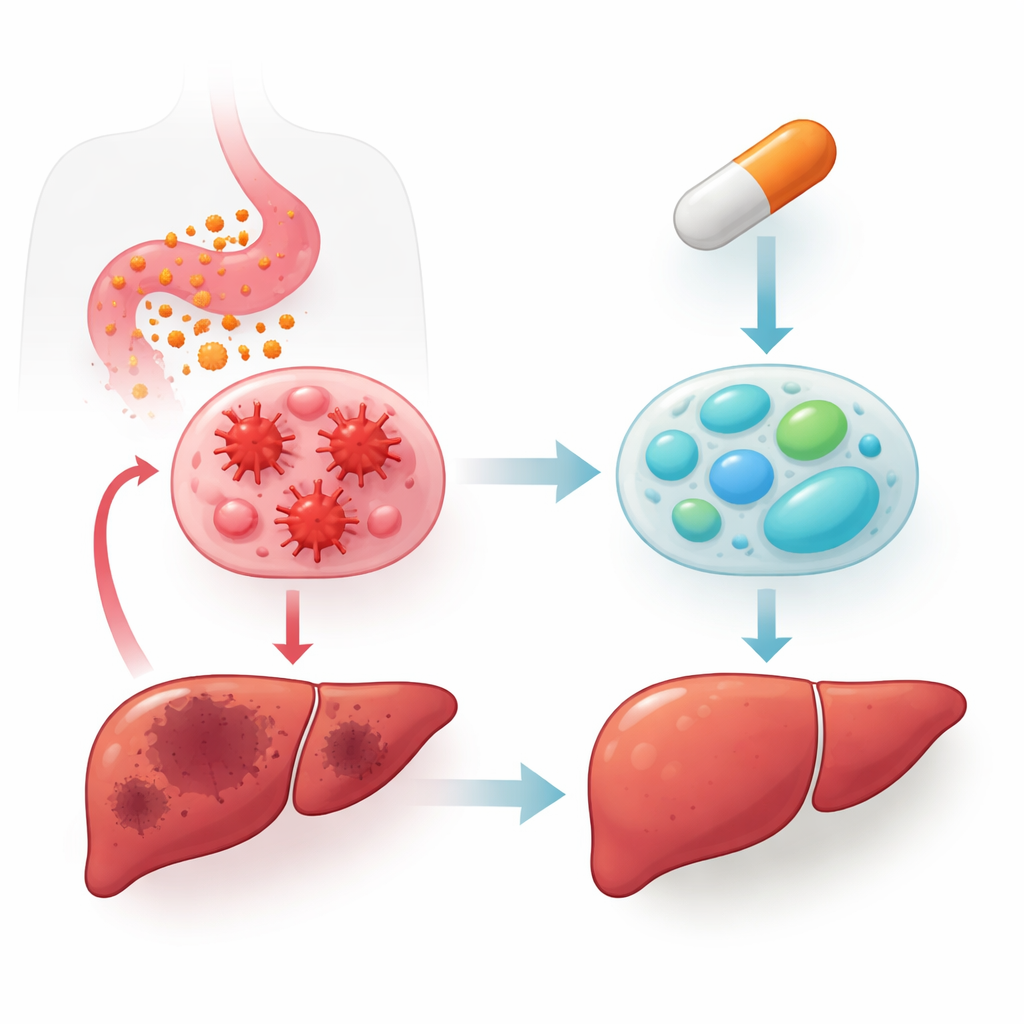
Pour vérifier si ces observations en culture cellulaire sont pertinentes in vivo, les auteurs ont utilisé des modèles murins d’inflammation aiguë et chronique. Dans un modèle sévère de septicémie induite par LPS, l’adapalène administré par voie orale a réduit les cytokines inflammatoires dans le sang et le foie, diminué les marqueurs de lésion hépatique, amélioré la structure du tissu hépatique à l’examen microscopique et amélioré de façon spectaculaire la survie, passant d’un taux de mortalité quasi certain à des taux de survie élevés. Chez des souris rendues obèses par un régime riche en graisses, plusieurs semaines d’adapalène oral ont réduit les marqueurs inflammatoires hépatiques, augmenté les marqueurs associés au M2, diminué l’activation des mêmes voies de kinases et réduit l’accumulation de graisse et de collagène associée à la stéatose hépatique et à la fibrose. Dans ces modèles, les niveaux hépatiques de RARβ étaient sélectivement augmentés, renforçant le rôle central de ce récepteur.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, l’étude suggère que l’adapalène peut agir comme un rhéostat interne pour les macrophages : il abaisse les réponses inflammatoires destructrices tout en augmentant les réponses réparatrices, principalement en activant RARβ et en calmant les cascades de signalisation en aval. Chez la souris, cela se traduit par une protection contre une septicémie létale, une réduction de l’inflammation hépatique et moins de cicatrisation dans la stéatose liée à l’obésité. Bien que l’adapalène soit actuellement approuvé uniquement comme traitement cutané, ces résultats soulèvent la possibilité que des formulations systémiques, soigneusement dosées et si elles sont sûres chez l’humain, puissent un jour aider à traiter des troubles inflammatoires et métaboliques en rééduquant les cellules immunitaires de l’organisme.
Citation: Lee, N.H., Choi, M.J., Ji, S.M. et al. Adapalene, an RAR agonist, exerts anti-inflammatory effects by regulating macrophage polarization through RAR\(\upbeta\)-mediated signaling pathways. Sci Rep 16, 11385 (2026). https://doi.org/10.1038/s41598-026-44454-z
Mots-clés: polarisation des macrophages, adapalène, inflammation, septicémie, stéatose hépatique