Clear Sky Science · it
Adapalene, un agonista RAR, esercita effetti anti-infiammatori regolando la polarizzazione dei macrofagi tramite vie di segnalazione mediate da RAR $$\upbeta$$
Perché un farmaco per la pelle conta per la salute dell’intero organismo
L’adapalene è noto soprattutto come gel topico per l’acne, ma questo studio suggerisce che potrebbe avere inaspettatamente poteri più ampi. I ricercatori mostrano che, somministrato per via orale nei topi, l’adapalene può calmare cellule immunitarie iperattive, proteggere il fegato da infezioni gravi e dai danni provocati da una dieta ricca di grassi e persino migliorare la sopravvivenza in un modello di sepsi. Per i lettori interessati a come un comune farmaco dermatologico potrebbe essere riproposto per combattere infiammazioni potenzialmente letali e malattie metaboliche, questo lavoro apre una finestra intrigante.
Cellule immunitarie di prima linea che possono danneggiare o guarire
Il nostro organismo si affida ai macrofagi — i grandi “mangiatori” del sistema immunitario — per rilevare germi, rimuovere detriti e coordinare l’infiammazione. Queste cellule possono adottare due modalità ampie. In uno stato M1, o pro-infiammatorio, producono molecole aggressive che aiutano a uccidere i microrganismi ma che possono anche danneggiare i tessuti se non controllate. In uno stato M2, o anti-infiammatorio e di riparazione, contribuiscono a risolvere l’infiammazione e a sostenere la guarigione. Nell’obesità, nella sepsi e nella malattia del fegato grasso, i macrofagi tendono a polarizzarsi verso lo stato M1, alimentando un’infiammazione cronica a bassa intensità che contribuisce alla resistenza all’insulina e alla fibrosi tissutale. Trovare modi per spostare i macrofagi verso uno stato più equilibrato o incline all’M2 è quindi un importante obiettivo terapeutico.
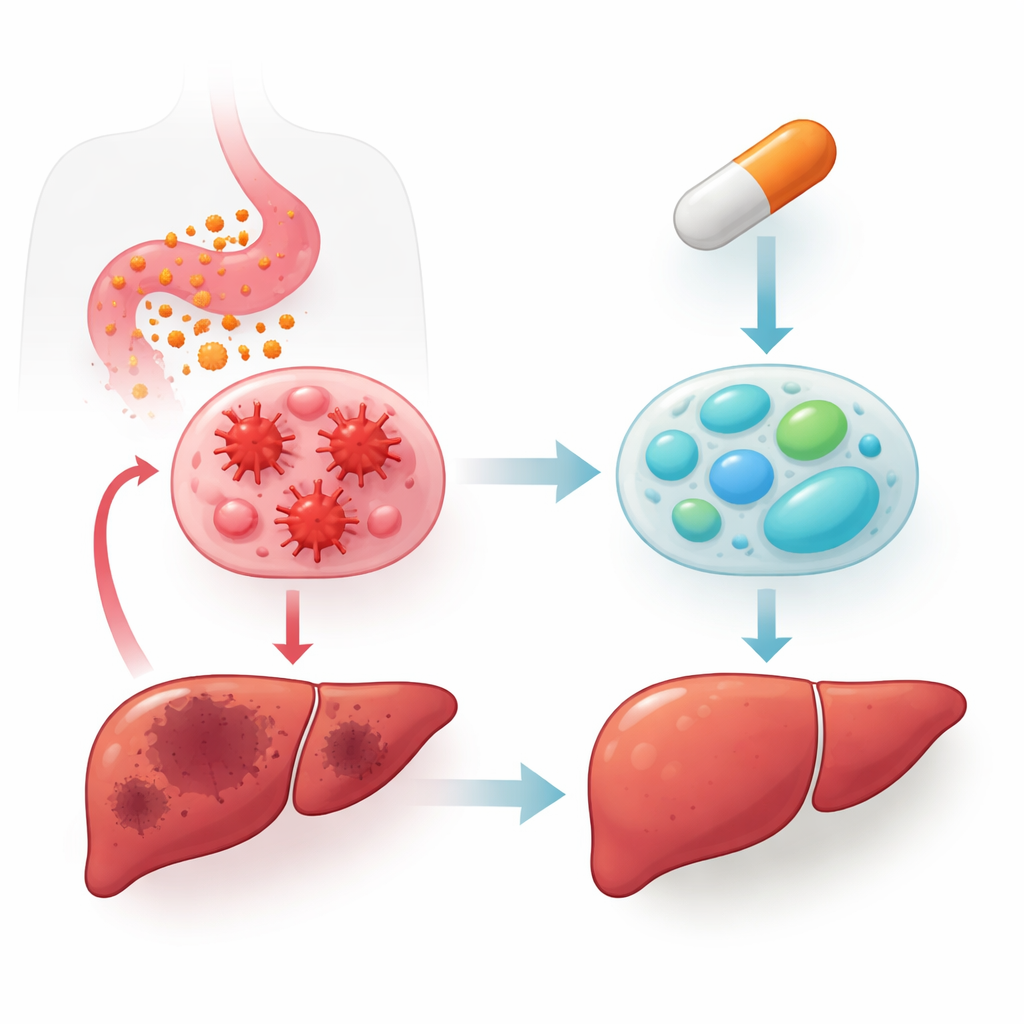
Un interruttore legato alla vitamina A all’interno delle cellule immunitarie
La vitamina A e i suoi derivati, chiamati retinoidi, regolano molti geni legandosi ai recettori dell’acido retinoico (RAR) all’interno delle cellule. L’adapalene è un retinoide sintetico che prende di mira in modo selettivo uno di questi recettori, RARβ. Gli autori si sono chiesti se l’attivazione di RARβ con l’adapalene potesse ricalibrare i macrofagi esposti al lipopolisaccaride (LPS), un componente batterico che scatena una potente risposta infiammatoria. In cellule di macrofagi murini, l’LPS aumentava nettamente messaggeri e enzimi classici dell’infiammazione. L’aggiunta di piccolissime quantità di adapalene ha attenuato questi segnali in modo dipendente dalla concentrazione, aumentando al contempo i marcatori associati allo stato M2, più orientato alla riparazione tissutale. Analisi con citometria a flusso hanno confermato che la popolazione cellulare si è spostata da un profilo di superficie simile all’M1 verso uno simile all’M2.
Spegnere i circuiti infiammatori e attivare la riparazione
Approfondendo, il team ha mappato come l’adapalene riorganizza il circuito molecolare all’interno dei macrofagi. L’LPS normalmente attiva diverse vie chinasi (MAPK e PI3K/Akt) e l’interruttore maestro infiammatorio NF-κB, che poi si sposta nel nucleo per attivare geni infiammatori. L’adapalene ha ridotto sostanzialmente l’attivazione di queste vie e limitato l’ingresso di NF-κB nel nucleo. Allo stesso tempo, ha aumentato la fosforilazione di STAT3, una proteina di segnalazione nota per favorire comportamenti di tipo M2. Quando i ricercatori hanno ridotto i livelli di RARβ con strumenti genetici, o lo hanno bloccato con un antagonista selettivo, l’adapalene ha in gran parte perso questi effetti: i marcatori infiammatori sono aumentati di nuovo, i marcatori calmanti dell’M2 sono diminuiti e le vie di segnalazione si sono riattivate. Questo ha identificato RARβ come l’interruttore interno chiave attraverso cui l’adapalene esercita la sua azione duale — attenuando i circuiti infiammatori e promuovendo i programmi di riparazione.
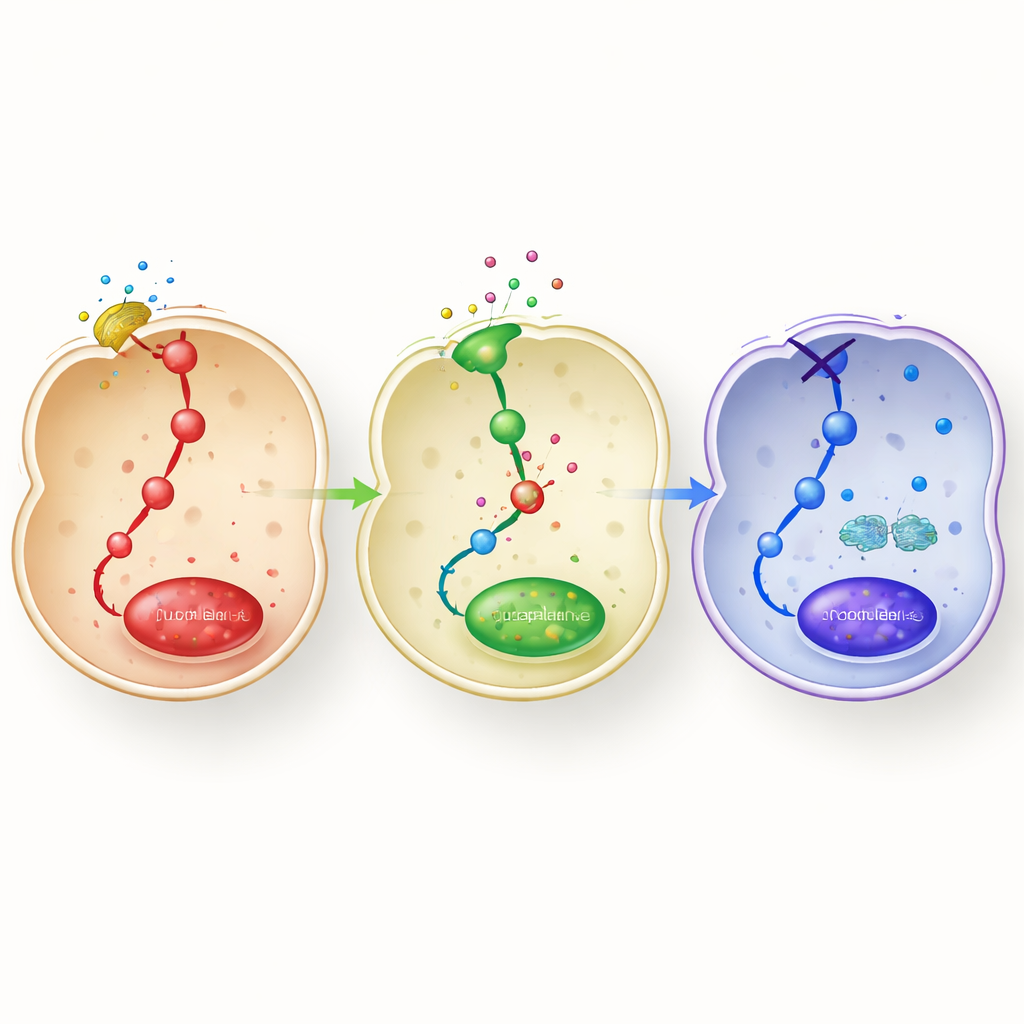
Dalle colture ai fegati malati e agli organismi interi
Per verificare se questi risultati in coltura cellulare avessero rilevanza negli organismi viventi, gli autori si sono rivolti a modelli murini di infiammazione sia acuta sia cronica. In un modello severo di sepsi indotta da LPS, l’adapalene somministrato per via orale ha ridotto le citochine infiammatorie nel sangue e nel fegato, diminuito i marcatori di danno epatico, migliorato la struttura del tessuto epatico all’esame istologico e ha migliorato drasticamente la sopravvivenza, passando da una morte quasi certa a tassi di sopravvivenza elevati. Nei topi resi obesi con una dieta ad alto contenuto di grassi, diverse settimane di adapalene orale hanno ridotto i marcatori infiammatori nel fegato, aumentato i marcatori associati all’M2, diminuito l’attivazione delle stesse vie chinasi e ridotto l’accumulo di grasso e collagene associato a fegato grasso e fibrosi. In tutti questi modelli, i livelli epatici di RARβ sono risultati selettivamente aumentati, rafforzando il ruolo centrale di questo recettore.
Cosa potrebbe significare per i trattamenti futuri
In parole semplici, lo studio suggerisce che l’adapalene può agire come un reostato interno per i macrofagi: abbassa risposte infiammatorie distruttive mentre aumenta risposte di guarigione, in larga parte attivando RARβ e attenuando le cascate di segnalazione a valle. Nei topi, ciò si traduce in protezione dalla sepsi letale, riduzione dell’infiammazione epatica e minore cicatrizzazione nel fegato grasso legato all’obesità. Sebbene l’adapalene sia attualmente approvato solo come trattamento cutaneo, questi risultati sollevano la possibilità che versioni sistemiche, dosate con attenzione e se dimostrate sicure nell’uomo, possano un giorno aiutare a trattare disturbi infiammatori e metabolici ri-educando le cellule immunitarie dell’organismo.
Citazione: Lee, N.H., Choi, M.J., Ji, S.M. et al. Adapalene, an RAR agonist, exerts anti-inflammatory effects by regulating macrophage polarization through RAR\(\upbeta\)-mediated signaling pathways. Sci Rep 16, 11385 (2026). https://doi.org/10.1038/s41598-026-44454-z
Parole chiave: polarizzazione dei macrofagi, adapalene, infiammazione, sepsi, malattia del fegato grasso