Clear Sky Science · zh
离体与计算研究:角膜离子电渗促进大分子渗透——以白蛋白为模型分子
为什么把药物放进眼睛这么难
大多数人认为眼药水是治疗眼病的简单方法,但实际上滴入眼中的药物很少能到达眼球内部。眼睛前方的透明窗口——角膜——的结构就是为了阻挡不受欢迎的物质,这对保护眼睛很重要,但对蛋白药物和其他大分子生物制剂等现代治疗却是主要障碍。本研究考察了一种温和的电学技术,称为离子电渗,旨在在保持眼组织安全的同时,更有效地推动大分子药物穿透角膜。
来自电力的温和推动
离子电渗通过在眼表施加低而受控的电流,促进药物分子穿过角膜。研究者以一种常见的血浆蛋白——白蛋白,作为许多高分子量药物的替代模型。他们将新鲜切下的兔角膜置于专用腔室中,施加不同强度的电流仅十秒钟,并测量有多少白蛋白穿过角膜。同时,他们建立了计算机模型来预测治疗过程中角膜的升温情况,因为过高的温度会损伤脆弱的眼组织。
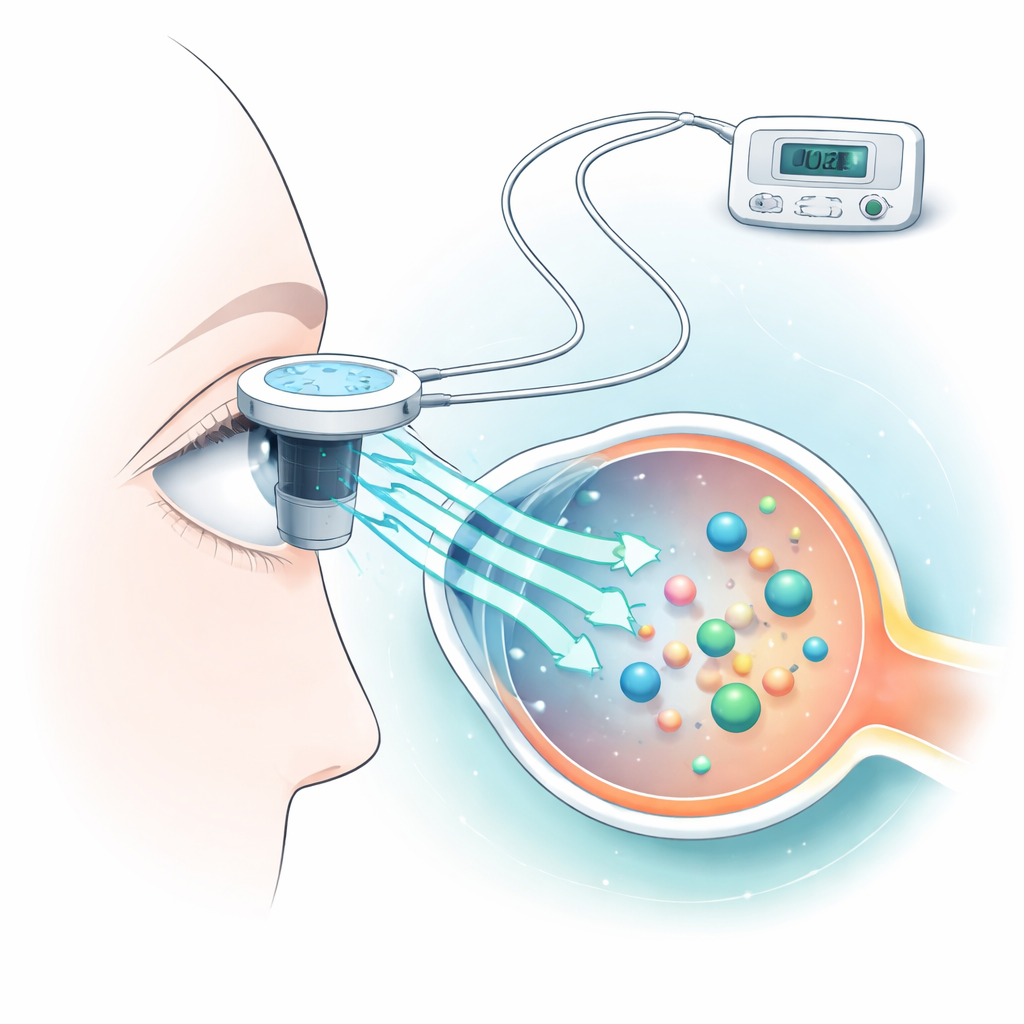
在递送与损伤之间寻找平衡点
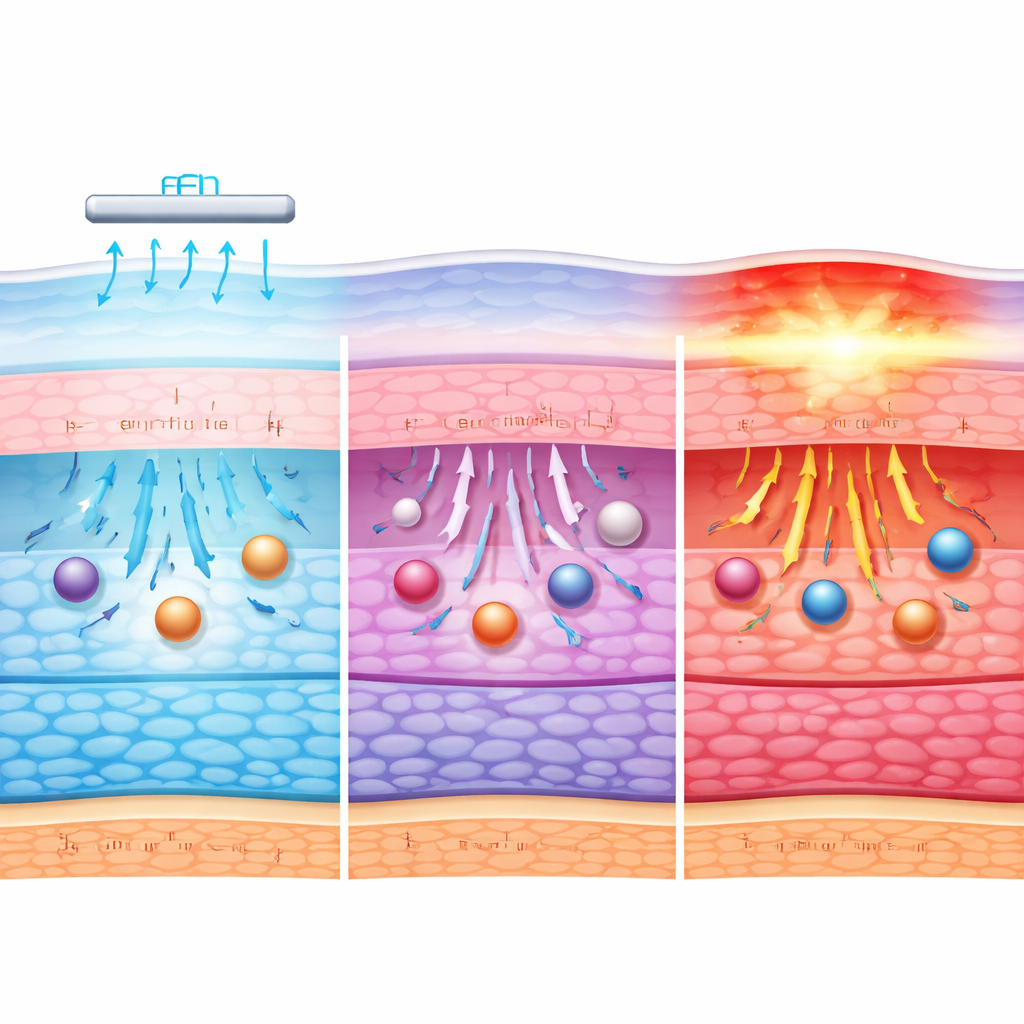
研究团队发现,与单纯浸泡相比,离子电渗明显提高了白蛋白的转运,且总体上电流越高,穿透的蛋白越多。在临床相关范围内(约高达7毫安),白蛋白的通透性有所增加,6–7毫安时效果最显著。他们的计算模拟显示,非常低的电流(约不超过2毫安)可将角膜表面温度维持在大约32–36°C的正常范围内,而3–7毫安的电流会进一步升温,若应用时间过长,有时会接近热应激成为问题的水平。作为损伤模型的极端测试电流500毫安导致强烈升温并出现明显的组织破坏迹象。
窥视角膜的分子结构
为了超越简单的温度和转运测量,研究人员使用红外光谱技术,这种方法能揭示角膜内水分、蛋白质和脂类在分子尺度上的响应。在低至中等电流下,光谱特征显示水结合、蛋白构象和脂类组织的细微变化,表明组织在电热负荷下做出适应但未失去基本结构。这些改变可能使通道稍微放宽,从而让大分子更易通过。然而在最高但非临床使用的电流下,红外谱图发生剧烈变化,提示蛋白质被破坏、水网路改变和膜结构受扰——这些都是不可逆损伤的标志。
该过程如何在流动、热量与结构之间取得平衡
研究表明,在角膜离子电渗过程中,多种因素共同作用。电场本身通过推动液体和带电颗粒帮助白蛋白穿过组织;轻微的升温进一步促进分子运动而不会立即伤害细胞。在低电流下,这种联合效应较小,角膜屏障大体保持完整。随着电流增至中等范围,更多的白蛋白得以渗透,这既受更强电力的推动,也受角膜分子排列发生小且可逆松弛的帮助。只有当电流达到极端时,热量和结构破坏才成为主导,破坏屏障而非温和打开它。
这对未来眼部治疗意味着什么
对普通读者而言,核心信息是:经过精心调整的电流剂量,未来有望让医生在无需注射的情况下将大型、有效的药物分子输送至眼内。这项工作描绘了在离体模型中既能增强药物渗透又能将角膜温度与分子结构保持在安全范围内的实际电流与时间窗口。尽管仍需在活体眼和真实治疗性蛋白上开展更多研究,但这些发现支持将离子电渗作为一种有前景的、非侵入性治疗手段,用于目前需注射的严重眼病,可能使治疗更安全、更舒适。
引用: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
关键词: 眼部药物递送, 角膜离子电渗, 白蛋白运输, 热安全性, 生物制剂治疗