Clear Sky Science · ru
Ex vivo и компьютерное исследование корнеальной ионтопфореза для повышения проникновения соединений с высокой молекулярной массой: исследование с использованием альбумина в качестве модельной молекулы
Почему так трудно доставить лекарство в глаз
Большинство людей считают, что глазные капли — это простое средство от болезней глаз, но на самом деле лишь малая часть препарата из капли попадает внутрь глаза. Прозрачное переднее окно глаза — роговица — устроено так, чтобы не пропускать посторонние вещества, что прекрасно защищает глаз, но создает серьёзное препятствие для современных методов лечения, таких как белковые препараты и другие крупные биомолекулы. В этом исследовании рассматривается щадящая электрическая методика, называемая ионтопфорезом, которая призвана эффективнее проталкивать большие молекулы через роговицу, сохраняя при этом безопасность глаза.
Мягкий толчок от электричества
Ионтопфорез работает за счёт приложения низкого, контролируемого электрического тока на поверхность глаза, что побуждает молекулы лекарства перемещаться через роговицу. Исследователи использовали распространённый белок крови — альбумин — в качестве заменителя многих препаратов с большой молекулярной массой. Они поместили свежевыделенные роговицы кроликов в специальные камеры, применяли разные уровни тока всего по десять секунд и измеряли, сколько альбумина прошло на другую сторону. Одновременно они создали компьютерную модель, чтобы предсказать, насколько прогреется роговица во время процедуры, поскольку избыточное тепло может повредить деликатные ткани глаза.
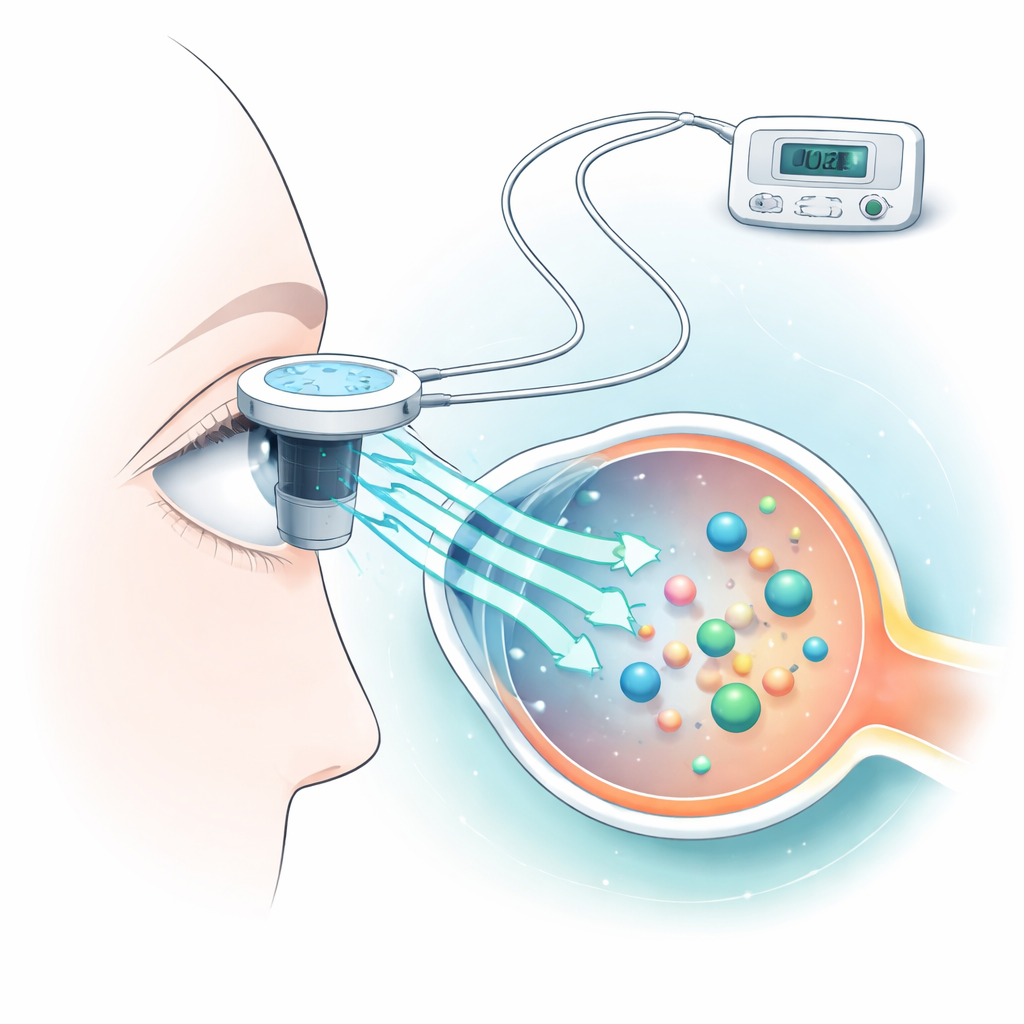
Нахождение оптимума между доставкой и повреждением
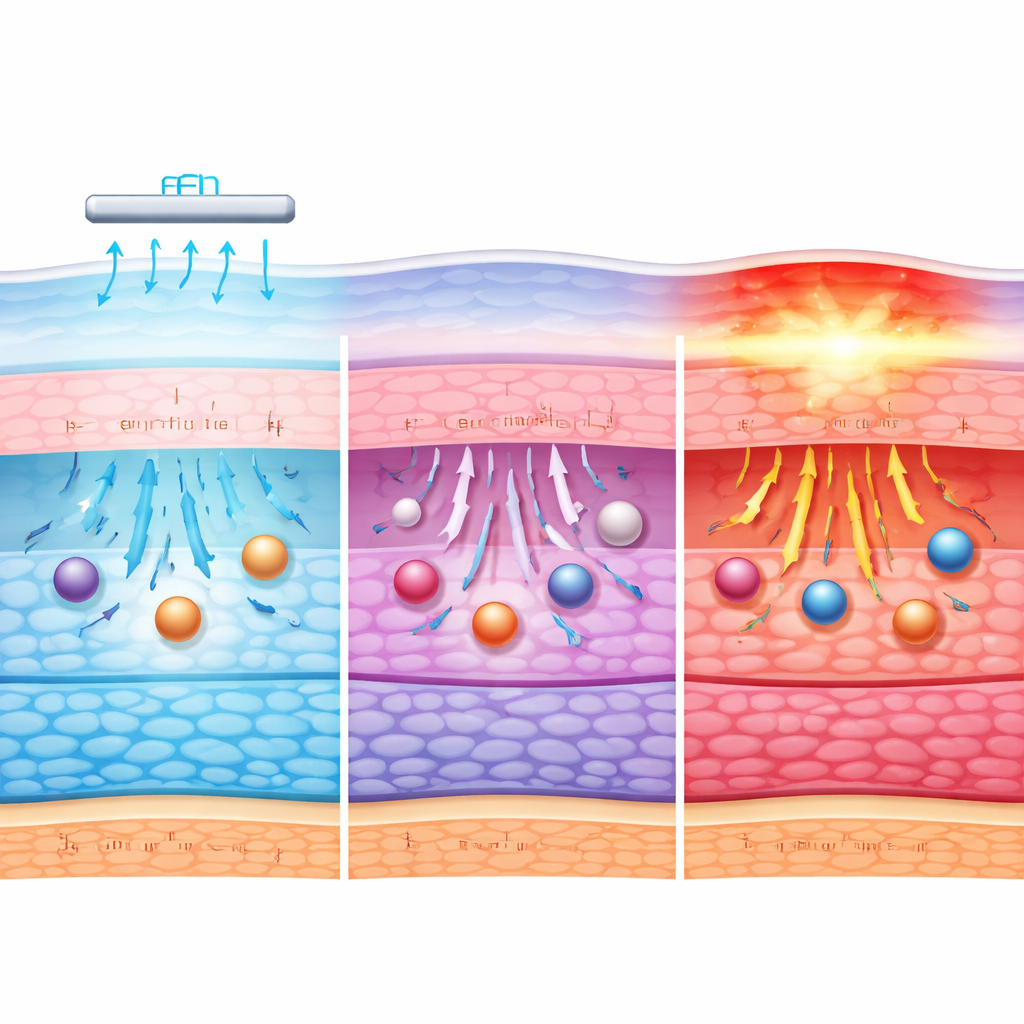
Команда обнаружила, что ионтопфорез явно усиливает транспорт альбумина по сравнению с простым вымачиванием, и что более высокие токи обычно перемещают больше белка через роговицу. Токи в клинически релевантном диапазоне, до примерно 7 миллиампер, увеличивали проницаемость для альбумина, с наибольшим эффектом при 6–7 миллиамперах. Их компьютерные симуляции показали, что очень низкие токи, до примерно 2 миллиампер, сохраняют температуру поверхности роговицы в её обычном диапазоне около 32–36 °C, в то время как токи 3–7 миллиампер дополнительно повышали температуру поверхности, иногда приближаясь к уровням, при которых тепловой стресс становится проблемой при длительном воздействии. Экстремальный тестовый ток в 500 миллиампер, использованный только как модель повреждения, вызвал интенсивный нагрев и явные признаки разрушения ткани.
Взгляд внутрь молекулярной структуры роговицы
Чтобы выйти за рамки простых измерений температуры и транспорта, исследователи обратились к инфракрасной спектроскопии — технике, которая показывает, как вода, белки и липиды внутри роговицы реагируют на молекулярном уровне. При низких и умеренных токах спектральные сигнатуры указывали на тонкие сдвиги в связях воды, форме белков и организации липидов, что согласуется с адаптацией ткани к электрической и тепловой нагрузке без утраты её базовой структуры. Эти изменения, вероятно, несколько ослабляют барьеры, позволяя крупным молекулам легче проходить. Однако при самом высоком, не клиническом токе инфракрасные паттерны заметно изменялись, сигнализируя о разрушении белков, перестройке водных сетей и нарушении мембран — признаках необратимого повреждения.
Как процесс уравновешивает поток, тепло и структуру
Исследование показывает, что при корнеальном ионтопфорезе действует несколько взаимосвязанных факторов. Сам электрическое поле помогает проталкивать альбумин через ткань, стимулируя движение жидкости и заряженных частиц; лёгкий нагрев дополнительно способствует перемещению без немедленного вреда для клеток. При низких токах этот комбинированный эффект умерен, и барьерная функция роговицы в основном сохраняется. По мере увеличения тока в средний диапазон через роговицу проникает больше альбумина благодаря как более сильным электрическим силам, так и небольшим, обратимым расслаблениям в молекулярной упаковке роговицы. Только при экстремальных токах тепло и структурные нарушения начинают доминировать, разрушая барьер вместо его щадящего открытия.
Что это значит для будущих методов лечения глаз
Для непрофессионала главный вывод таков: аккуратно подобранная доза электричества может в будущем позволить врачам доставлять крупные, эффективные молекулы в глаз без инъекций. Эта работа очерчивает практическое окно по величине тока и времени воздействия, которое повышает проникновение препарата, сохраняя при этом температуру роговицы и молекулярную структуру в безопасных пределах в ex vivo модели. Хотя необходимы дальнейшие исследования на живых глазах и с реальными терапевтическими белками, результаты поддерживают ионтопфорез как перспективный неинвазивный способ лечения серьёзных заболеваний глаза, которые в настоящее время требуют инъекций, что потенциально сделает уход более безопасным и комфортным для пациентов.
Цитирование: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
Ключевые слова: доставка лекарств в глаз, корнеальный ионтопфорез, транспорт альбумина, тепловая безопасность, биологические терапевтические препараты