Clear Sky Science · pl
Badania ex vivo i obliczeniowe nad jontoforezą rogówki w celu zwiększenia penetracji związków o dużej masie cząsteczkowej: badanie z użyciem albuminy jako modelowej cząsteczki
Dlaczego podawanie leków do oka jest takie trudne
Większość osób wyobraża sobie krople do oczu jako proste rozwiązanie problemów okulistycznych, tymczasem tylko niewielka część substancji z kropli rzeczywiście dociera do wnętrza oka. Przezroczysta przednia warstwa oka — rogówka — została zaprojektowana, by chronić przed niechcianymi substancjami, co jest korzystne z punktu widzenia ochrony, ale stanowi poważną przeszkodę dla nowoczesnych terapii, takich jak leki białkowe i inne duże cząsteczki biologiczne. W tym badaniu przyjrzano się delikatnej technice elektrycznej, zwanej jontoforezą, mającej na celu skuteczniejsze przepychanie dużych cząsteczek leku przez rogówkę przy jednoczesnym zachowaniu bezpieczeństwa oka.
Delikatne pchnięcie prądem
Jontoforeza polega na zastosowaniu niskiego, kontrolowanego prądu na powierzchni oka, aby zachęcić cząsteczki leku do przemieszczania się przez rogówkę. Badacze użyli powszechnego białka krwi, albuminy, jako substytutu dla wielu leków o dużej masie cząsteczkowej. Umieścili świeżo wyjęte rogówki królicze w specjalnych komorach, przyłożyli różne poziomy prądu na zaledwie dziesięć sekund i zmierzyli, ile albuminy przeszło na drugą stronę. Równocześnie zbudowali model komputerowy, który przewidywał, jak bardzo rogówka nagrzeje się podczas zabiegu, ponieważ nadmiar ciepła może uszkodzić delikatne tkanki oka.
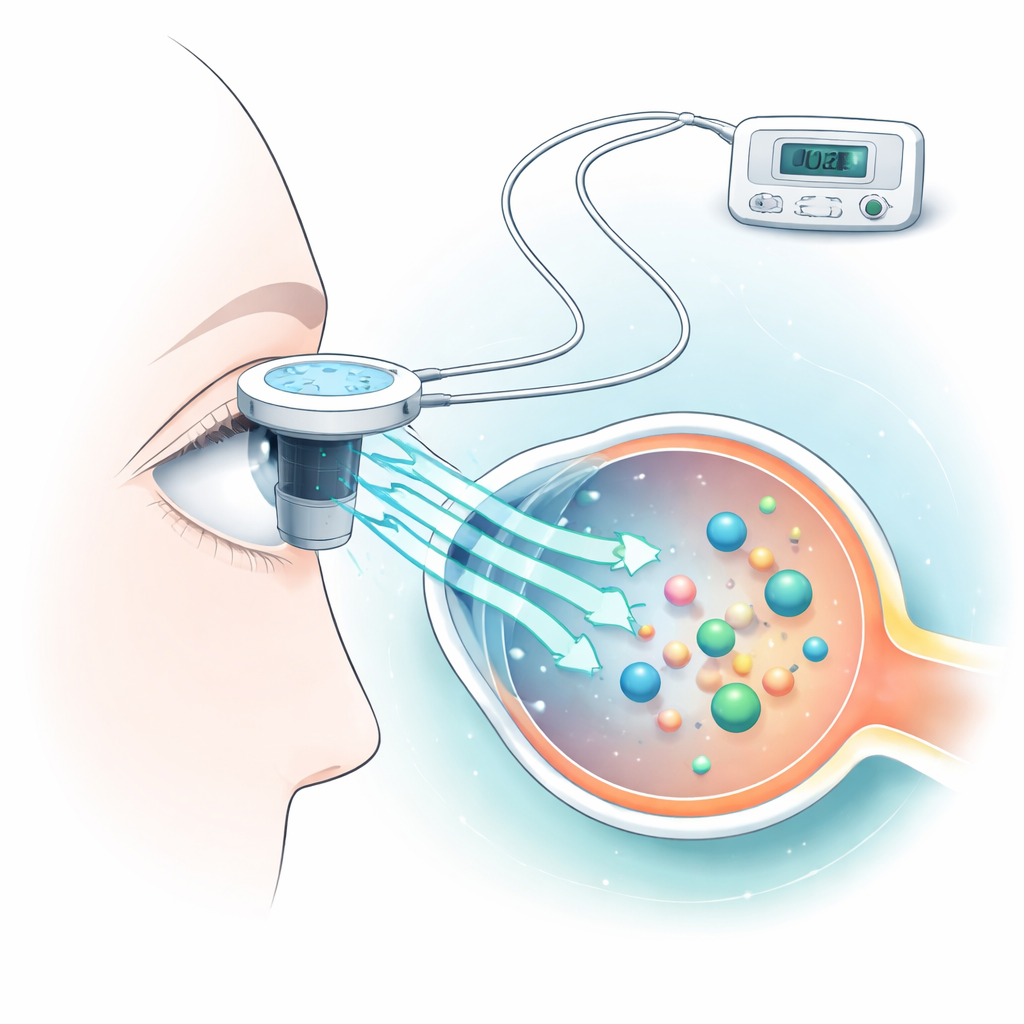
Wyznaczanie złotego środka między dostarczeniem a uszkodzeniem
Zespół wykazał, że jontoforeza wyraźnie zwiększa transport albuminy w porównaniu z prostym namaczaniem, oraz że wyższe natężenia prądu generalnie przesuwają więcej białka przez rogówkę. Prądy w zakresie klinicznie istotnym, do około 7 miliamperów, zwiększały przepuszczalność dla albuminy, z najsilniejszymi efektami przy 6–7 mA. Symulacje komputerowe wykazały, że bardzo niskie prądy, do około 2 mA, utrzymują temperaturę powierzchni rogówki w zwykłym zakresie około 32–36 °C, podczas gdy prądy 3–7 mA dodatkowo ją podgrzewają, czasem osiągając poziomy, przy których stres termiczny staje się problematyczny, jeśli działanie trwa zbyt długo. Ekstremalny prąd testowy 500 mA, użyty tylko jako model uszkodzenia, spowodował intensywne nagrzewanie i wyraźne oznaki rozpadu tkanek.
Wgląd w molekularną strukturę rogówki
Aby wyjść poza proste pomiary temperatury i transportu, badacze sięgnęli po spektroskopię podczerwieni — technikę ukazującą, jak woda, białka i tłuszcze w rogówce reagują na poziomie molekularnym. Przy niskich i umiarkowanych prądach sygnatury spektralne wskazywały subtelne przesunięcia w wiązaniach wody, kształcie białek oraz organizacji lipidów, co zgadza się z adaptacją tkanki do obciążenia elektrycznego i termicznego bez utraty jej podstawowej struktury. Zmiany te prawdopodobnie nieco rozluźniają drogi przepływu, umożliwiając łatwiejsze przenikanie dużych cząsteczek. Przy najwyższym, pozaklinicznym natężeniu prądu wzory w podczerwieni zmieniły się drastycznie, sygnalizując zaburzenie białek, zmienione sieci wody i naruszone błony — cechy nieodwracalnego uszkodzenia.
Jak proces równoważy przepływ, ciepło i strukturę
Badanie pokazuje, że podczas jontoforezy rogówki działa wiele współzależnych czynników. Pole elektryczne samo w sobie pomaga napędzać albuminę przez tkankę, popychając płyny i naładowane cząstki; łagodne ogrzanie dodatkowo sprzyja ruchowi bez natychmiastowego uszkadzania komórek. Przy niskich prądach efekt ten jest skromny, a bariera rogówki w dużej mierze pozostaje nienaruszona. W miarę wzrostu natężenia do zakresu średniego więcej albuminy przenika, wspomagane zarówno silniejszymi siłami elektrycznymi, jak i drobnymi, odwracalnymi rozluźnieniami w molekularnym upakowaniu rogówki. Dopiero przy ekstremalnych natężeniach dominują ciepło i zaburzenia strukturalne, niszcząc barierę zamiast jej łagodnego otwarcia.
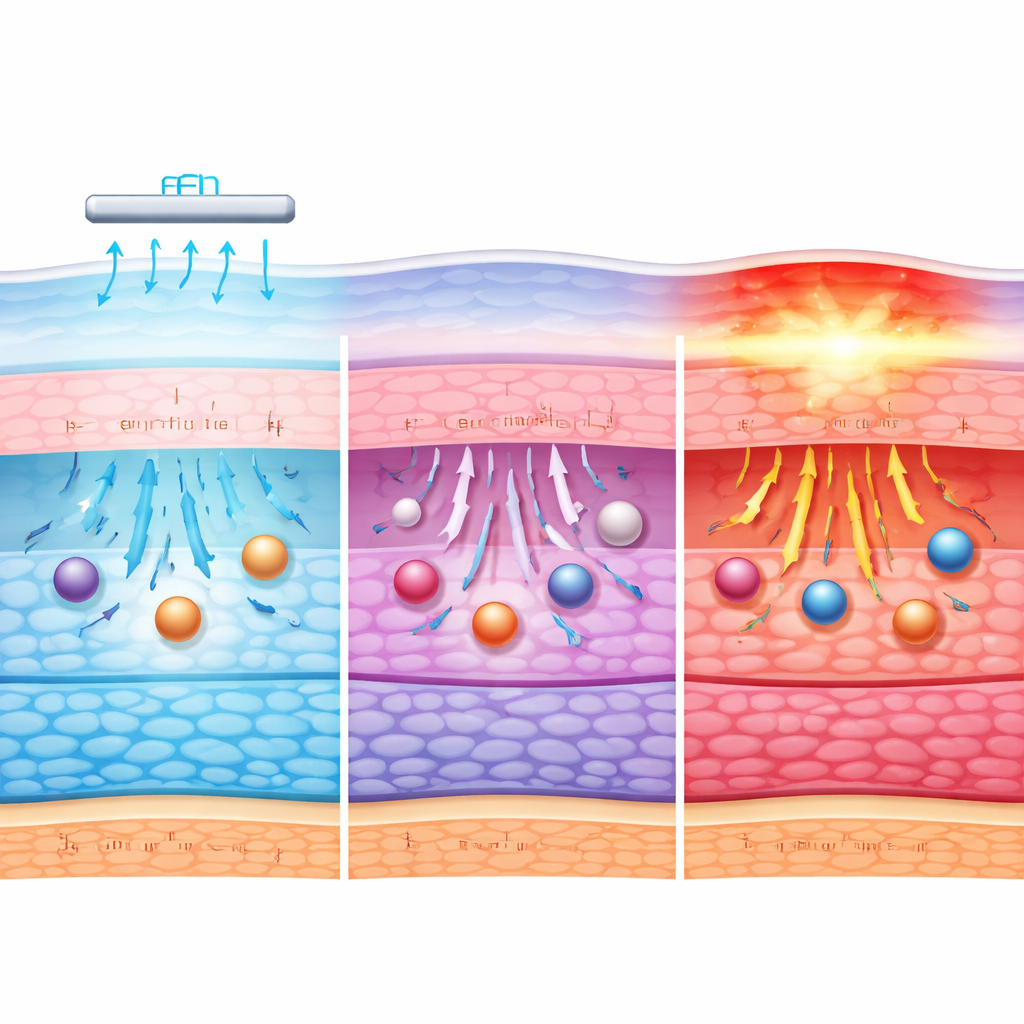
Co to oznacza dla przyszłych terapii okulistycznych
Dla laików kluczowy wniosek jest taki, że ostro wyregulowana dawka prądu może w przyszłości pozwolić lekarzom dostarczać duże, silne cząsteczki leków do oka bez użycia igieł. Praca ta wyznacza praktyczne okno natężenia i czasu, które zwiększa penetrację leku przy utrzymaniu temperatury rogówki i struktury molekularnej w bezpiecznych granicach w modelu ex vivo. Choć potrzebne są dalsze badania na żywych oczach i z rzeczywistymi białkami terapeutycznymi, wyniki wspierają jontoforezę jako obiecującą, nieinwazyjną metodę leczenia poważnych chorób oczu, które dziś wymagają wstrzyknięć — potencjalnie czyniąc opiekę bezpieczniejszą i bardziej komfortową dla pacjentów.
Cytowanie: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
Słowa kluczowe: dostarczanie leków do oka, jontoforeza rogówki, transport albuminy, bezpieczeństwo termiczne, leki biologiczne