Clear Sky Science · es
Investigación ex vivo y computacional de la iontoforesis corneal para mejorar la penetración de compuestos de alto peso molecular: un estudio usando albúmina como molécula modelo
Por qué es tan difícil introducir medicamentos en el ojo
La mayoría de la gente piensa que las gotas oftálmicas son una solución sencilla para las enfermedades oculares, pero en realidad muy poco del fármaco de una gota llega al interior del ojo. La ventana frontal transparente del ojo —la córnea— está diseñada para mantener fuera las sustancias no deseadas, lo cual es excelente para la protección pero un gran obstáculo para tratamientos modernos como los fármacos proteicos y otras moléculas biológicas de gran tamaño. Este estudio explora una técnica eléctrica suave, llamada iontoforesis, diseñada para impulsar moléculas grandes a través de la córnea de manera más eficaz sin comprometer la seguridad del ojo.
Un empujón suave mediante electricidad
La iontoforesis funciona aplicando una corriente eléctrica baja y controlada en la superficie del ojo para fomentar el movimiento de las moléculas del fármaco a través de la córnea. Los investigadores usaron una proteína sanguínea común, la albúmina, como sustituto de muchos medicamentos de alto peso molecular. Colocaron córneas de conejo recién extraídas en cámaras especiales, aplicaron distintos niveles de corriente durante solo diez segundos y midieron cuánto de albúmina atravesó hasta el otro lado. Al mismo tiempo, construyeron un modelo computacional para predecir cuánto se calentaría la córnea durante el tratamiento, porque el calor excesivo puede dañar los tejidos delicados del ojo.
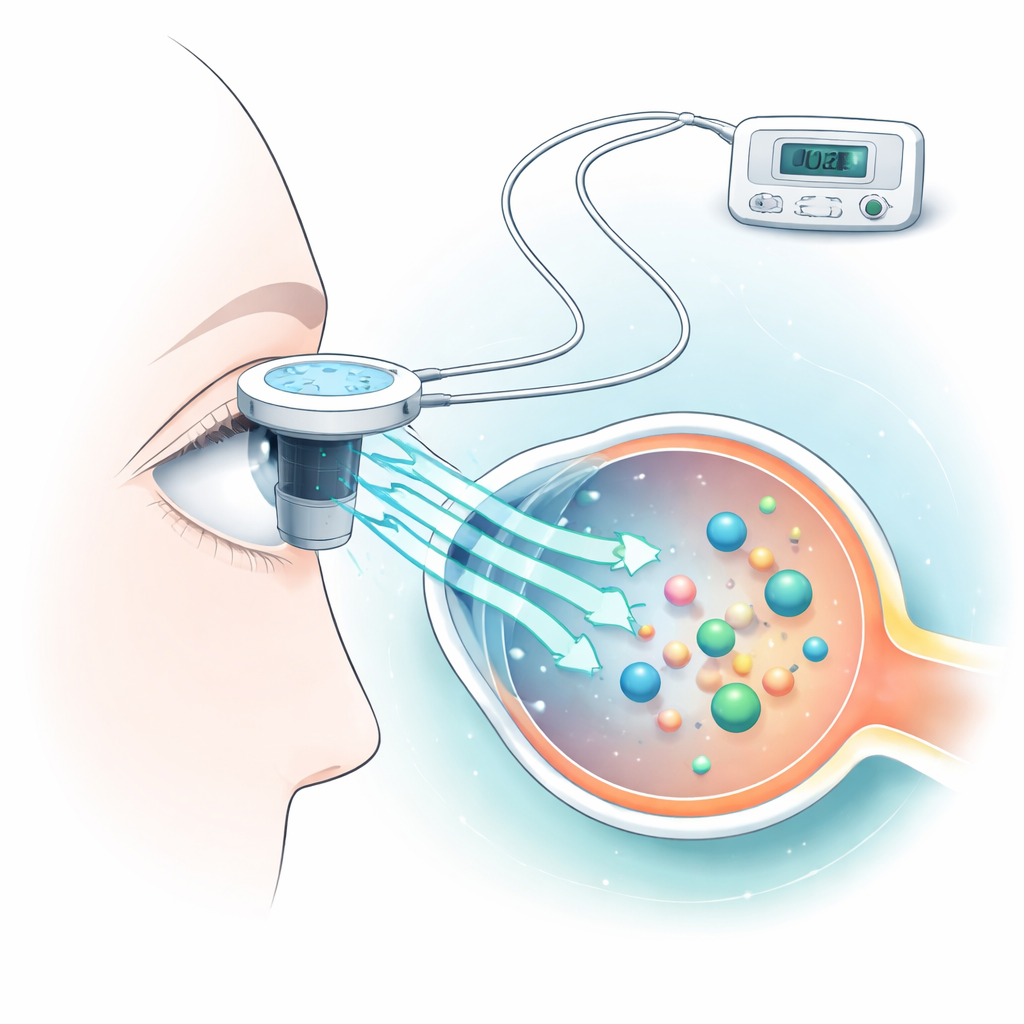
Encontrar el punto óptimo entre entrega y daño
El equipo halló que la iontoforesis aumentó claramente el transporte de albúmina en comparación con la simple inmersión, y que corrientes más altas generalmente movían más proteína a través de la córnea. Corrientes en el rango clínicamente relevante, hasta aproximadamente 7 miliamperios, aumentaron la permeación de albúmina, con las mayores ganancias alrededor de 6–7 miliamperios. Sus simulaciones por ordenador mostraron que corrientes muy bajas, hasta aproximadamente 2 miliamperios, mantenían la temperatura superficial corneal dentro de su rango habitual de unos 32–36 °C, mientras que corrientes de 3–7 miliamperios calentaban más la superficie, a veces acercándose a niveles donde el estrés térmico se convierte en un riesgo si se aplican durante demasiado tiempo. Una corriente extrema de prueba de 500 miliamperios, usada solo como modelo de daño, produjo un calentamiento intenso y claros signos de degradación tisular.
Mirando dentro del tejido molecular de la córnea
Para ir más allá de las simples mediciones de temperatura y transporte, los investigadores recurrieron a la espectroscopía infrarroja, una técnica que revela cómo responden a escala molecular el agua, las proteínas y las grasas dentro de la córnea. A corrientes bajas a moderadas, las firmas espectrales indicaron cambios sutiles en la unión del agua, la conformación de las proteínas y la organización de los lípidos, coherentes con un tejido que se adapta a la carga eléctrica y térmica sin perder su estructura básica. Estos cambios probablemente aflojan lo suficiente las vías como para que las moléculas grandes puedan deslizarse con mayor facilidad. Sin embargo, en la corriente más alta, no clínica, los patrones infrarrojos cambiaron de forma drástica, señalando proteínas alteradas, redes de agua modificadas y membranas perturbadas, rasgos característicos de daño irreversible.
Cómo el proceso equilibra flujo, calor y estructura
El estudio muestra que múltiples factores actúan conjuntamente durante la iontoforesis corneal. El campo eléctrico en sí ayuda a impulsar la albúmina a través del tejido al mover fluidos y partículas cargadas; un calentamiento moderado facilita aún más el movimiento sin dañar inmediatamente las células. A corrientes bajas, este efecto combinado es modesto y la barrera corneal permanece en gran medida intacta. A medida que la corriente aumenta hacia el rango medio, más albúmina penetra, favorecida tanto por fuerzas eléctricas más fuertes como por pequeñas y reversibles relajaciones en el empaquetamiento molecular de la córnea. Solo cuando la corriente se vuelve extrema predominan el calor y la disrupción estructural, destruyendo la barrera en lugar de abrirla suavemente.
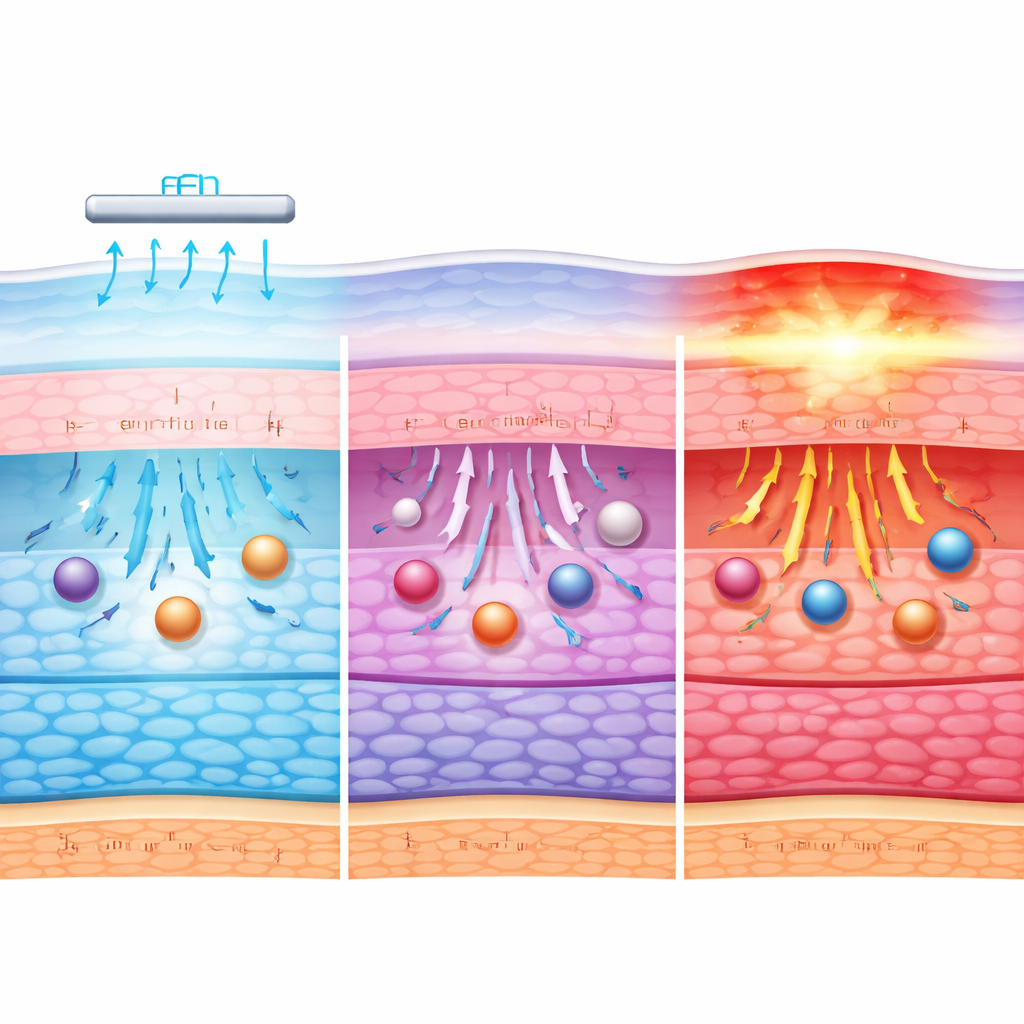
Qué implica esto para futuros tratamientos oculares
Para un público general, el mensaje clave es que una dosis cuidadosamente ajustada de electricidad podría algún día permitir a los médicos administrar moléculas grandes y potentes en el ojo sin agujas. Este trabajo traza una ventana práctica de corriente y tiempo que aumenta la penetración del fármaco manteniendo la temperatura corneal y la estructura molecular dentro de límites seguros en un modelo ex vivo. Aunque se necesitan más estudios en ojos vivos y con proteínas terapéuticas reales, los hallazgos respaldan la iontoforesis como una vía prometedora y no invasiva para tratar enfermedades oculares graves que actualmente requieren inyecciones, lo que podría hacer la atención más segura y cómoda para los pacientes.
Cita: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
Palabras clave: administración de fármacos oculares, iontoforesis corneal, transporte de albúmina, seguridad térmica, terapéuticos biológicos