Clear Sky Science · he
חקירה חוץ-גופית וחישובית של יונטופורזה לקרנית לשיפור חדירת תרכובות בעלות משקל מולקולרי גבוה: מחקר המשתמש באלבומין כמולקולת מודל
מדוע קשה להחדיר תרופות לתוך העין
רוב האנשים חושבים שטיפות עין הן פתרון פשוט למחלות עין, אך במציאות מעט מאוד מהתרופה בטיפה מגיע בפועל אל פנים העין. החלון הקדמי השקוף של העין — הקרנית — בנוי כדי למנוע כניסת חומרים לא רצויים, וזה מצוין להגנה אך מהווה מכשול משמעותי לטיפולים מודרניים כגון תרופות חלבוניות ומולקולות ביולוגיות גדולות אחרות. מחקר זה חוקר שיטה חשמלית עדינה, הקרויה יונטופורזה, שנועדה לדחוף מולקולות תרופה גדולות דרך הקרנית ביעילות רבה יותר תוך שמירה על בטיחות העין.
דחיפה עדינה על ידי חשמל
יונטופורזה פועלת על‑ידי יישום זרם חשמלי נמוך ומבוקר על פני שטח העין כדי לעודד את תנועת מולקולות התרופה דרך הקרנית. החוקרים השתמשו בחלבון דם נפוץ, אלבומין, כתחליף לרבות מהתרופות בעלות המשקל המולקולרי הגבוה. הם הניחו קרניות ארנב שהתנקרו טרי בתאים מיוחדים, יישמו רמות שונות של זרם למשך עשר שניות בלבד, ומדדו כמה אלבומין עבר לצד השני. במקביל הם בנו מודל ממוחשב כדי לחזות עד כמה הקרנית תתחמם במהלך הטיפול, משום שחימום מופרז עלול לפגוע ברקמות העדינות של העין.
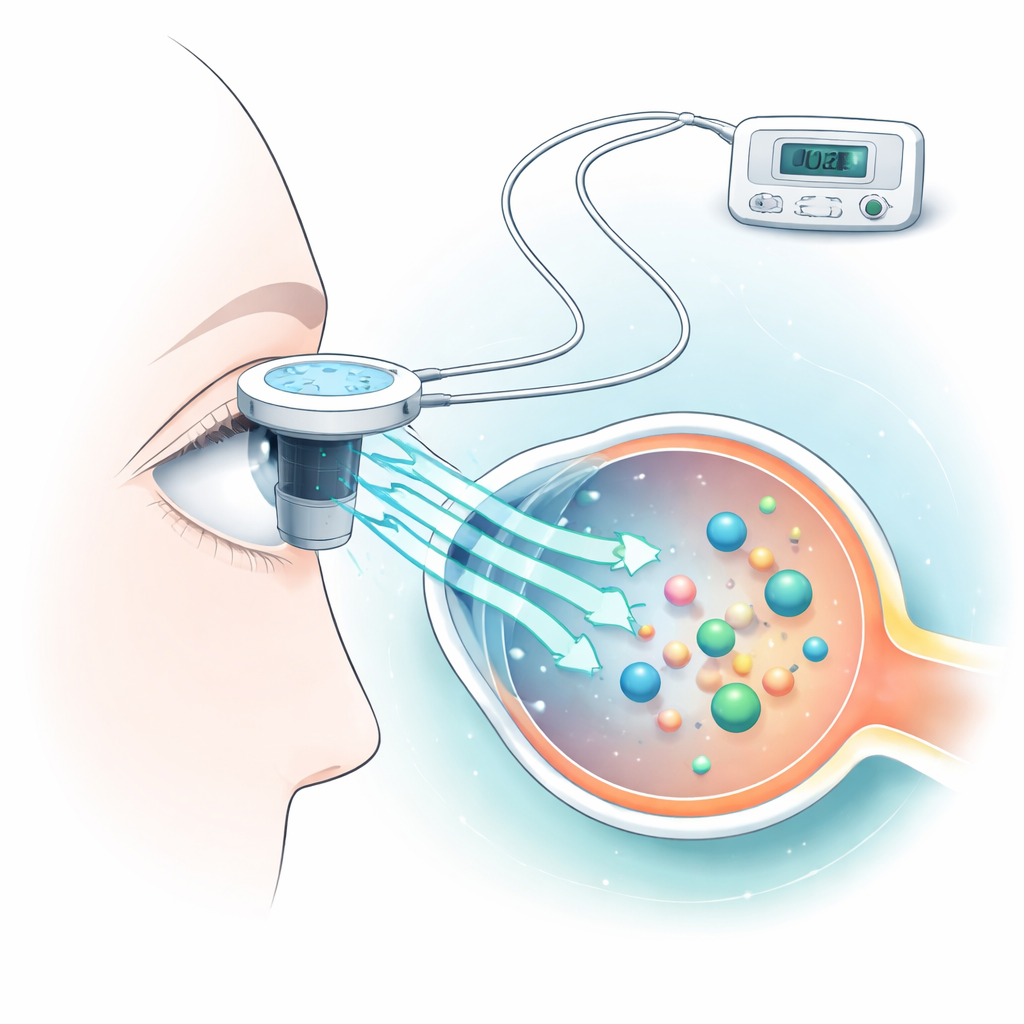
מציאת הנקודה המתאימה בין העברה לנזק
הצוות מצא שיונטופורזה שיפרה באופן ברור את העברת האלבומין בהשוואה להשריה פשוטה, וכי זרמים גבוהים יותר בדרך כלל נדחפו יותר חלבון דרך הקרנית. זרמים בתחום הקליני הרלוונטי, עד כ‑7 מיליאמפר, הגדילו את חדירות האלבומין, עם התועלות החזקות ביותר ב‑6–7 מיליאמפר. המדידות והסימולציות הממוחשבות הראו שזרמים נמוכים מאוד, בערך עד 2 מיליאמפר, הקפידו על טמפרטורת פני הקרנית בטווח הרגיל שלה כ‑32–36 °C, בעוד שזרמים של 3–7 מיליאמפר חיממו את המשטח עוד יותר, לעתים מתקרבים לרמות שבהן מתח חום עלול להיות חשש אם מוחל למשך זמן רב מדי. זרם מבחן קיצוני של 500 מיליאמפר, ששימש רק כמודל לנזק, יצר חימום אינטנסיבי וסימני פירוק רקמה ברורים.
מסתכלים בתוך הסיבוב המולקולרי של הקרנית
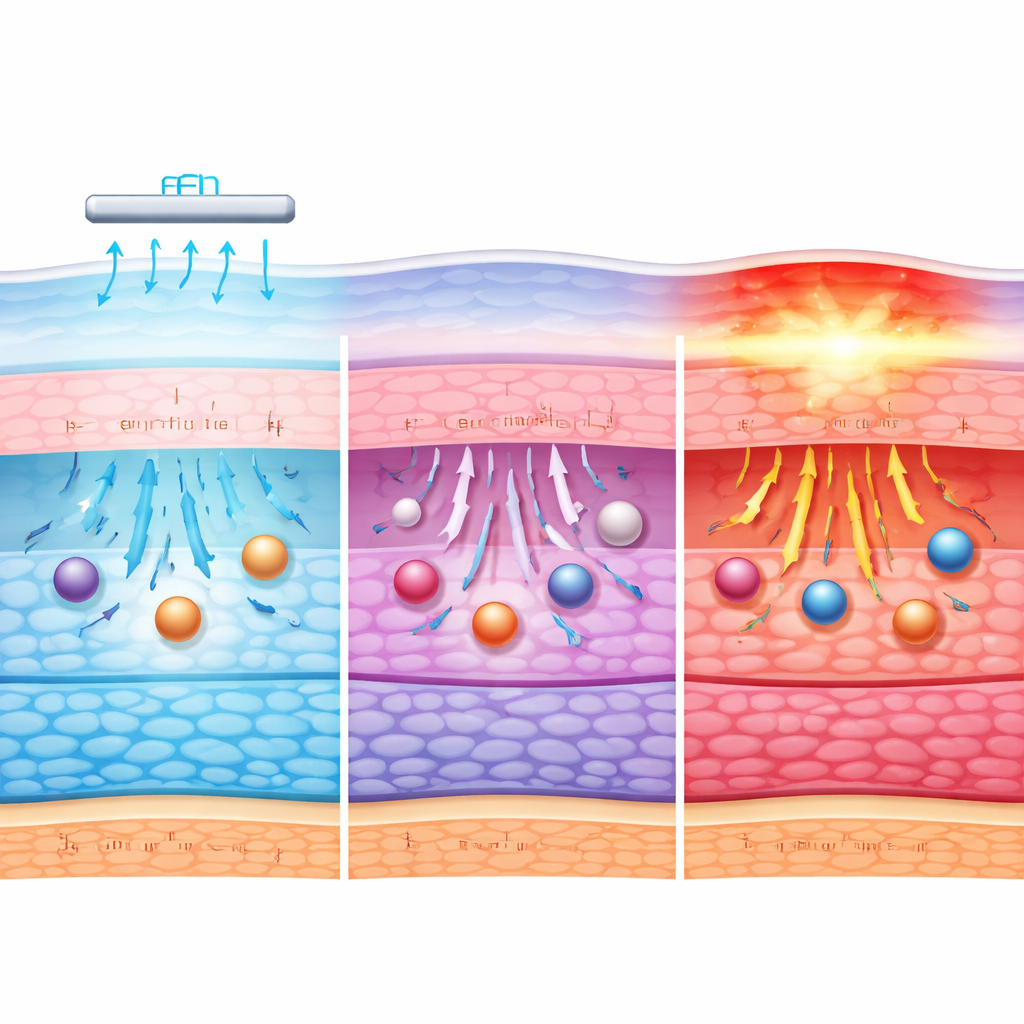
כדי להתקדם מעבר למדידות פשוטות של טמפרטורה והעברה, החוקרים פנו לספקטרוסקופיה תת‑אדומה, שיטה החושפת כיצד המים, החלבונים והשומנים בתוך הקרנית מגיבים בקנה מידה מולקולרי. בזרמים נמוכים עד בינוניים, החתימות ספקטרליות הצביעו על שינויים עדינים בקשירת המים, בצורת החלבונים ובארגון הליפידים (שומנים), תואם להתאמת הרקמה לעומס החשמלי והתרמי מבלי לאבד את המבנה הבסיסי שלה. שינויים אלה סביר שמרחיבים נתיבים מספיק כדי שמולקולות גדולות יעברו בקלות רבה יותר. אולם בזרם הגבוה ביותר שאינו קליני, דפוסי התת‑אדום השתנו בצורה ניכרת, מה שמעיד על חלבונים מופרעים, רשתות מים משובשות וממברנות שנפגעו — מאפיינים של נזק בלתי הפיך.
כיצד התהליך מאזן בין זרימה, חום ומבנה
המחקר מראה שמספר גורמים פועלים יחד במהלך יונטופורזה לקרנית. השדה החשמלי עצמו מסייע בדריבתו של האלבומין דרך הרקמה על‑ידי דחיפת נוזל וחלקיקים טעונים; חימום מתון עוד מעודד תנועה מבלי לפגוע בתאים באופן מיידי. בזרמים נמוכים ההשפעה המשולבת צנועה, ומחסום הקרנית נשאר ברובו שלם. ככל שהזרם עולה לטווח הביניים, יותר אלבומין חודר, בסיוע גם לכוחות חשמליים חזקים יותר וגם לשחרורים מולקולריים הפיכים במארג הקרנית. רק כאשר הזרם נעשה קיצוני שולט החום והשיבוש המבני, והם הורסים את המחסום במקום לפתוח אותו בעדינות.
מה משמעות הדבר עבור טיפולי עין עתידיים
לציבור הרחב, המסר המרכזי הוא שמינון חשמלי מכויל היטב עשוי יום אחד לאפשר לרופאים להסיע מולקולות תרופה גדולות ועוצמתיות לתוך העין ללא מזרקים. עבודה זו ממפה חלון מעשי של זרם וזמן שמגביר חדירת תרופות תוך שמירה על טמפרטורת הקרנית ומבנה המולקולות במסגרת גבולות בטוחים במודל חוץ‑גופי. למרות שיש צורך במחקרים נוספים בעיניים חיות ובשימוש בחלבונים תרופתיים אמיתיים, הממצאים תומכים ביונטופורזה כגישה מבטיחה, לא חודרנית, לטיפול במחלות עין קשות שכרגע דורשות הזרקות — מה שיכול להפוך את הטיפול לבטוח ונוח יותר עבור המטופלים.
ציטוט: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
מילות מפתח: מתן תרופות עיני, יונטופורזה לקרנית, העברת אלבומין, בטיחות תרמית, תרפויטיקה ביולוגית