Clear Sky Science · fr
Étude ex vivo et computationnelle de l’iontophorèse cornéenne pour améliorer la pénétration de composés de haut poids moléculaire : une étude utilisant l’albumine comme molécule modèle
Pourquoi il est si difficile d’administrer des médicaments dans l’œil
La plupart des gens considèrent les gouttes oculaires comme une solution simple aux maladies de l’œil, mais en réalité très peu du médicament contenu dans une goutte atteint l’intérieur de l’œil. La fenêtre antérieure transparente de l’œil — la cornée — est conçue pour empêcher les substances indésirables de pénétrer, ce qui protège bien mais constitue un obstacle majeur pour les traitements modernes tels que les protéines thérapeutiques et autres grosses molécules biologiques. Cette étude explore une technique électrique douce, appelée iontophorèse, destinée à faire traverser la cornée par de grosses molécules médicamenteuses de manière plus efficace tout en préservant la sécurité oculaire.
Une poussée douce fournie par l’électricité
L’iontophorèse fonctionne en appliquant un courant électrique faible et contrôlé à la surface de l’œil pour encourager les molécules de médicament à traverser la cornée. Les chercheurs ont utilisé une protéine sanguine commune, l’albumine, comme substitut de nombreux médicaments à haut poids moléculaire. Ils ont placé des cornées de lapin fraîchement prélevées dans des chambres spéciales, appliqué différents niveaux de courant pendant seulement dix secondes, et mesuré la quantité d’albumine ayant traversé jusqu’à l’autre côté. Parallèlement, ils ont construit un modèle informatique pour prédire le réchauffement de la cornée pendant le traitement, car un excès de chaleur peut endommager les tissus oculaires délicats.
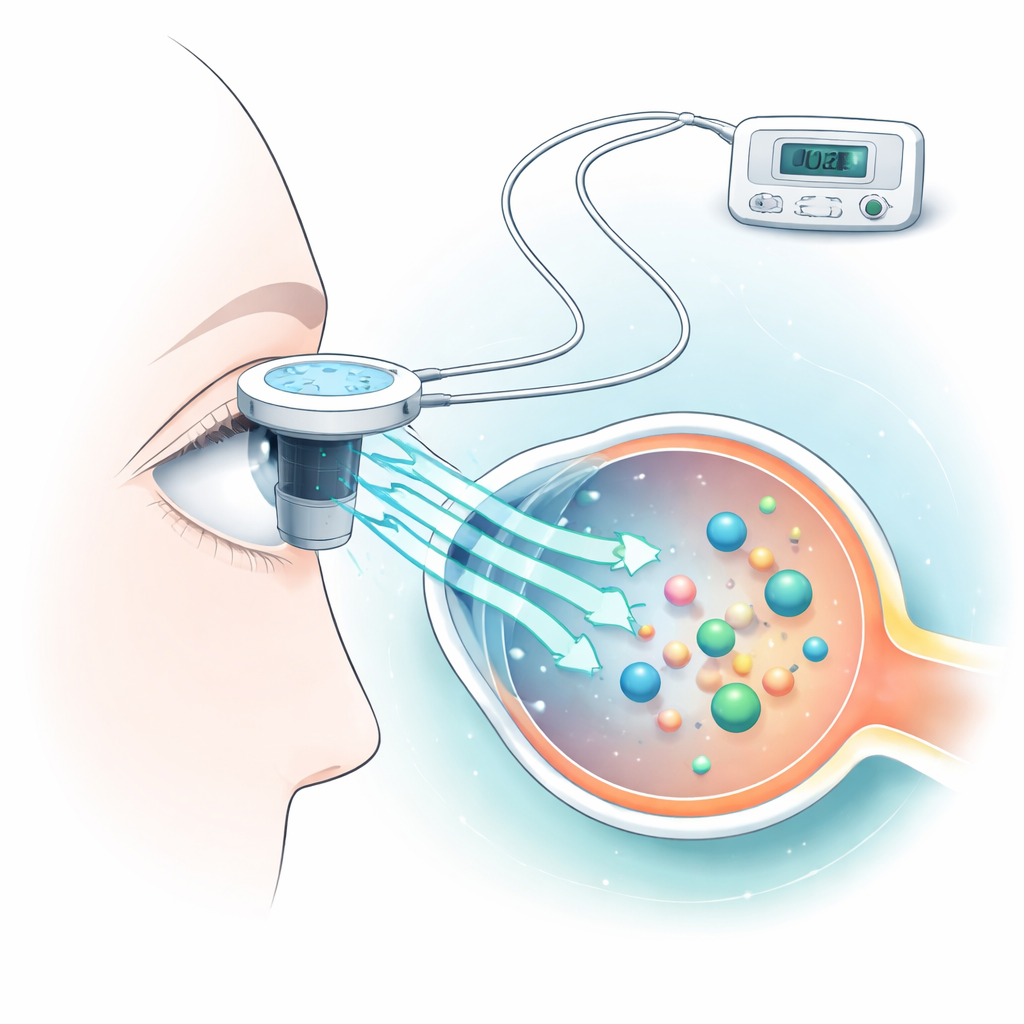
Trouver l’équilibre entre délivrance et dommage
L’équipe a constaté que l’iontophorèse augmentait clairement le transport d’albumine par rapport à une simple imprégnation, et que des courants plus élevés faisaient généralement traverser davantage de protéine à travers la cornée. Des courants dans la plage cliniquement pertinente, jusqu’à environ 7 milliampères, ont augmenté la perméation de l’albumine, avec les plus forts gains autour de 6–7 milliampères. Leurs simulations informatiques ont montré que des courants très faibles, jusqu’à environ 2 milliampères, maintenaient la température de surface cornéenne dans sa fourchette habituelle d’environ 32–36 °C, tandis que des courants de 3–7 milliampères réchauffaient davantage la surface, parfois en approchant des niveaux où le stress thermique devient préoccupant si appliqué trop longtemps. Un courant extrême de 500 milliampères, utilisé uniquement comme modèle de dommage, a produit un réchauffement intense et des signes évidents de détérioration tissulaire.
Regarder à l’intérieur du tissu moléculaire de la cornée
Pour aller au‑delà des simples mesures de température et de transport, les chercheurs ont eu recours à la spectroscopie infrarouge, une technique qui révèle comment l’eau, les protéines et les lipides à l’intérieur de la cornée réagissent à l’échelle moléculaire. À des courants faibles à modérés, les signatures spectrales indiquaient des modifications subtiles de la liaison de l’eau, de la conformation des protéines et de l’organisation des lipides, compatibles avec une adaptation du tissu à la charge électrique et thermique sans perte de sa structure de base. Ces changements semblent probablement assouplir suffisamment les voies pour que de grosses molécules puissent se faufiler plus facilement. En revanche, au courant le plus élevé mais non clinique, les profils infrarouges ont basculé de façon spectaculaire, signalant des protéines perturbées, des réseaux d’eau altérés et des membranes désorganisées — caractéristiques d’un dommage irrémédiable.
Comment le processus équilibre flux, chaleur et structure
L’étude montre que plusieurs facteurs agissent de concert lors de l’iontophorèse cornéenne. Le champ électrique lui‑même favorise le passage de l’albumine à travers le tissu en entraînant des flux de fluide et des particules chargées ; un léger réchauffement encourage en outre le mouvement sans endommager immédiatement les cellules. À faibles courants, cet effet combiné est modeste et la barrière cornéenne reste en grande partie intacte. À mesure que le courant augmente dans la plage intermédiaire, plus d’albumine pénètre, aidée à la fois par des forces électriques plus fortes et par de petites relaxations réversibles dans le compactage moléculaire de la cornée. Ce n’est que lorsque le courant devient extrême que la chaleur et la disruption structurelle prédominent, détruisant la barrière plutôt que de l’ouvrir doucement.
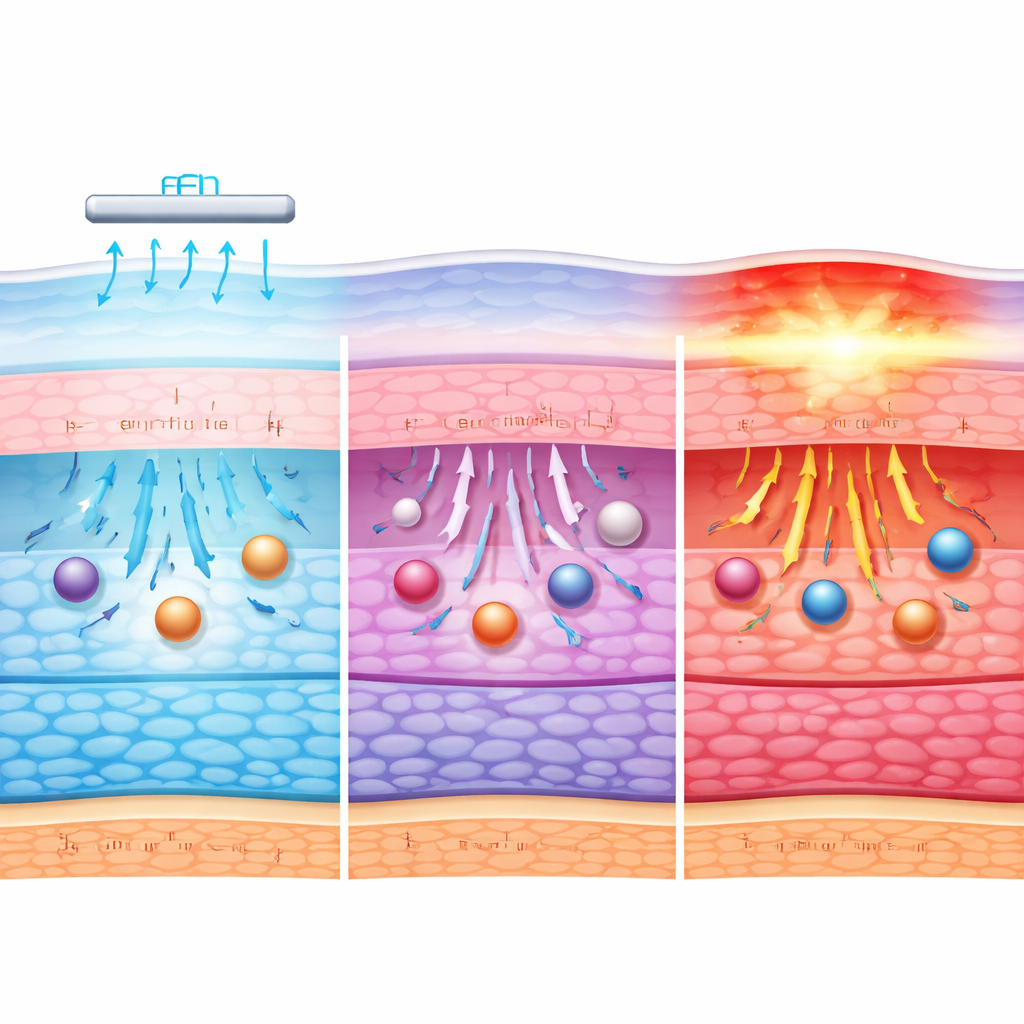
Ce que cela signifie pour les traitements oculaires futurs
Pour le grand public, le message clé est qu’une dose d’électricité soigneusement réglée pourrait un jour permettre aux médecins d’administrer de grosses molécules médicamenteuses dans l’œil sans aiguilles. Ce travail cartographie une fenêtre pratique de courant et de durée qui augmente la pénétration des médicaments tout en maintenant la température et la structure moléculaires de la cornée dans des limites sûres dans un modèle ex vivo. Bien que des études supplémentaires sur des yeux vivants et avec de véritables protéines thérapeutiques soient nécessaires, les résultats soutiennent l’iontophorèse comme une méthode non invasive prometteuse pour traiter des maladies oculaires graves actuellement traitées par injections, rendant potentiellement les soins à la fois plus sûrs et plus confortables pour les patients.
Citation: Mohamed, A.K., Mahmoud, S.S., Elshibly, S.M. et al. Ex vivo and computational investigation of corneal iontophoresis to enhance penetration of high-molecular-weight compounds: a study using albumin as a model molecule. Sci Rep 16, 10990 (2026). https://doi.org/10.1038/s41598-026-43580-y
Mots-clés: administration oculaire de médicaments, iontophorèse cornéenne, transport de l’albumine, sécurité thermique, thérapeutiques biologiques