Clear Sky Science · zh
集成密度泛函理论、分子对接与分子动力学研究若干新型2-硫代水杨酰脲类似物作为有效CDK2抑制剂用于抗癌治疗
这项研究对未来癌症治疗的重要性
许多抗癌药物像钝器一样作用,在攻击肿瘤的同时也损伤健康细胞。本文探讨一种更精确的策略:设计能够选择性关闭细胞分裂关键引擎——名为CDK2的蛋白质的小分子。研究人员通过先进的计算模拟替代反复试错的合成化学,筛选出若干有前景的候选分子,这些分子未来有望成为更安全、更具靶向性的抗癌药物。
从源头阻止失控的细胞分裂
许多癌症的增长归因于细胞周期(控制细胞何时分裂的内部时钟)失控。CDK2是推动细胞进入该周期的主要开关之一。早期试图抑制CDK2的药物虽显示出潜力,但常常也作用于与之高度相似且对正常细胞必不可少的蛋白,导致副作用。作者专注于一种较少被研究的化学家族——2‑硫代水杨酰脲,这类环状分子在电子和构型上可调。研究目标是评估该家族的某些成员是否能比细胞自身的能量分子ATP更强且更具选择性地结合CDK2,同时避免影响其他激酶。
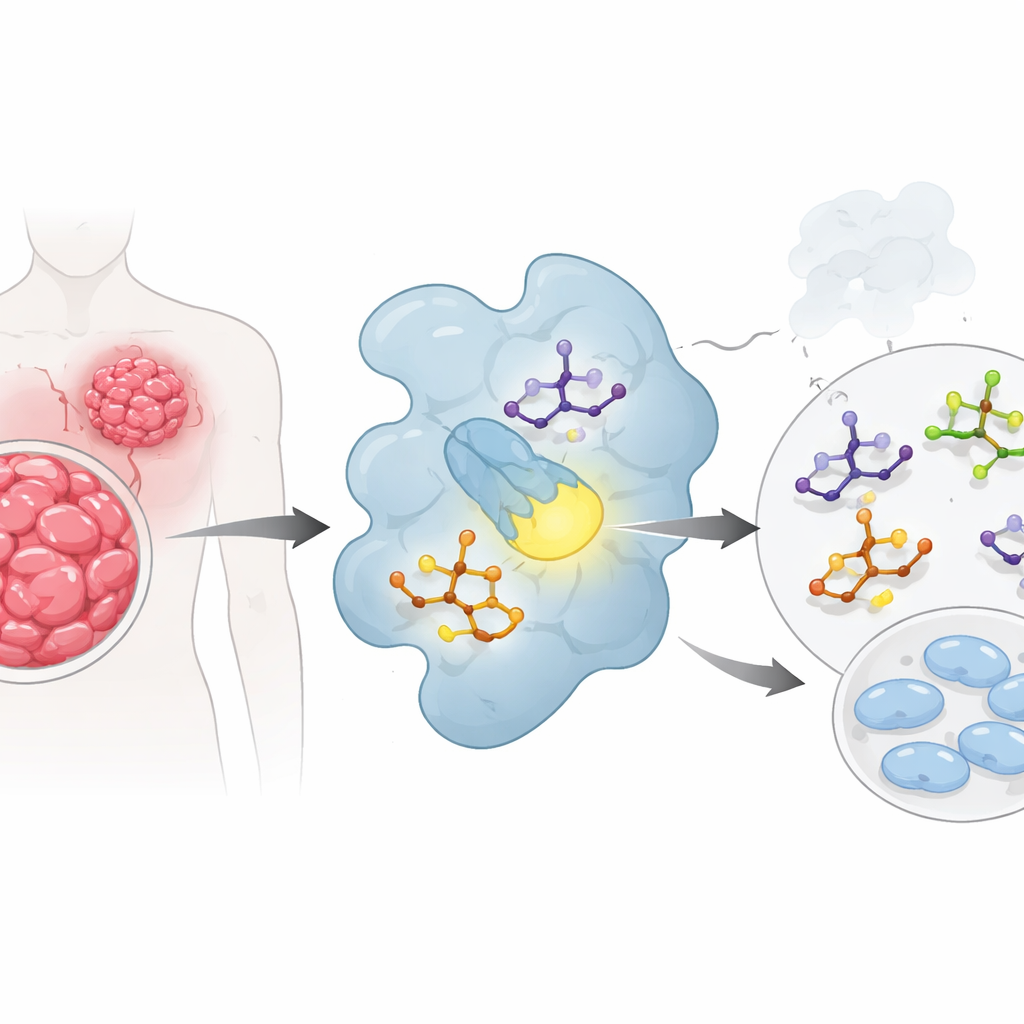
用计算方法“预先测试”药物候选物
研究团队没有直接进入实验室合成,而是首先采用多层次的量子化学与分子建模来了解这些分子的行为。他们计算了每个化合物中电子迁移的难易程度、极性以及分子中哪些部分最可能与蛋白质形成有利接触。标记为2b到2e的化合物脱颖而出:它们在关键电子态之间的能隙较小且具有高“亲电性”,表明应当更易与生物配体相互作用。每个分子的电荷表面图显示氧和硫原子周围存在明显的负电区域,而某些氢原子周围呈现正电区域——这些是当药物嵌入蛋白口袋时形成氢键的天然热点。
测试在CDK2口袋内的契合度
下一步是虚拟对接:将每个候选分子放入CDK2的三维结构中,让计算机搜索最佳契合,就像在锁中试钥匙一样。在这些模拟中,若干分子,尤其是2b、2c和2d,比ATP本身与CDK2的结合更紧密。它们与位于ATP结合口袋核心的两个残基Lys33和Thr14形成关键的氢键,并且紧密填充了衬在空腔内的疏水氨基酸。相比之下,未经过精细取代的母体骨架结合力较弱,这强调了环上化学修饰的细微变化如何显著改变性能。
观察蛋白—药物复合体的动态行为
由于蛋白和药物并非刚性不变,作者进行了分子动力学模拟,实际上是在原子尺度上以慢动作观察十纳秒级的演化。这些模拟显示CDK2的整体构象保持稳定,同时某些药物—蛋白对会晃动甚至逐渐脱离。有一分子2f表现出极高的稳定性,几乎不在口袋内移动,平均维持近三个氢键与蛋白相互作用。其他如2c和2d则在强结合与适度柔性之间取得平衡。为了将这些运动转化为整体“黏附力”,团队使用MM‑PBSA技术估算结合自由能。在这项分析中,化合物2d表现为最均衡的优选者,在口袋内的吸引力与离开溶剂所需的能量成本之间具备特别有利的平衡。
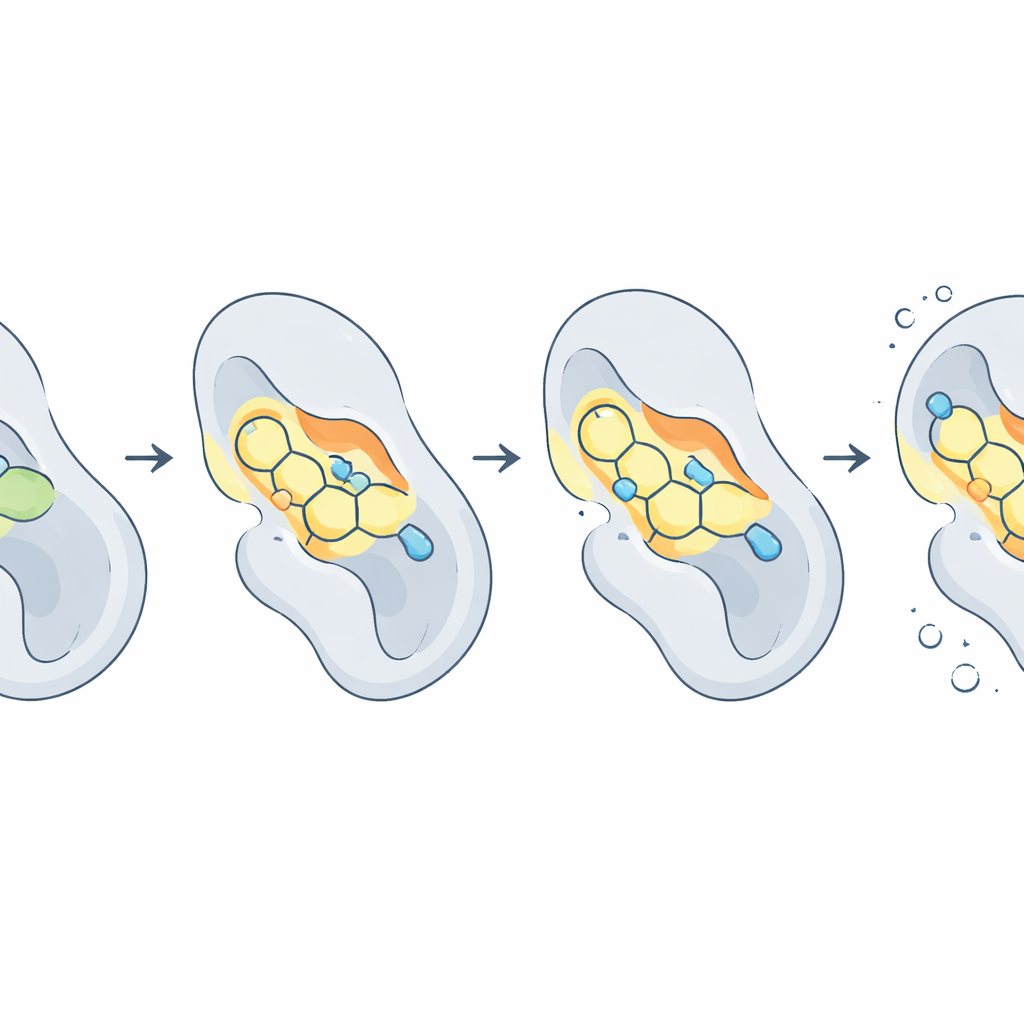
这对患者可能意味着什么
综上模拟结果表明,四种2‑硫代水杨酰脲化合物——2b、2c、2d和2f——是作为抗癌药物开发的特别有希望的起点。它们兼具有利的电子特性、对CDK2的强且定向的结合,以及在2d的情况下尤其有利的整体结合能。虽然这些发现纯属计算预测,仍需实验验证,但为化学家提供了详细的蓝图:在核心环上应如何放置卤素、酸或酯基以增强结合力与选择性。如果未来的实验测试证实这些预测,这项工作可能加速更精确的CDK2靶向疗法的开发,从而在抑制肿瘤生长的同时尽量保护健康细胞。
引用: Khaled, N.A., Ahmed, S.A., Ibrahim, M.A. et al. Integrated DFT, molecular docking, and molecular dynamics investigation of some novel 2-thiohydantoin analogues as potent CDK2 inhibitors for anticancer therapy. Sci Rep 16, 10985 (2026). https://doi.org/10.1038/s41598-026-42330-4
关键词: CDK2抑制剂, 靶向癌症治疗, 分子对接, 2-硫代水杨酰脲, 计算药物设计