Clear Sky Science · ru
Интегрированное исследование методом теории функционала плотности, молекулярного докинга и молекулярной динамики некоторых новых аналогов 2-тиогидантоина как потенциальных ингибиторов CDK2 для противораковой терапии
Почему это исследование важно для будущего лечения рака
Препараты против рака часто действуют как грубые инструменты, повреждая здоровые клетки наряду с опухолевыми. В этой статье рассматривается более точная стратегия: разработка малых молекул, которые селективно выключают ключевой механизм деления клеток — белок CDK2. Используя продвинутые компьютерные симуляции вместо метода проб и ошибок в химии, исследователи выявляют несколько перспективных кандидатных молекул, которые в будущем могут стать более безопасными и целенаправленными противораковыми средствами.
Остановка неконтролируемого деления клеток у истока
Многие виды рака развиваются потому, что клеточный цикл — внутренняя «машина времени», контролирующая, когда клетки делятся, — вышел из-под контроля. CDK2 является одним из главных переключателей, продвигающих клетки через этот цикл. Ранние препараты, нацеленные на CDK2, показывали обещающие результаты, но часто также поражали близкородственные белки, важные для нормальных клеток, что приводило к побочным эффектам. Авторы сосредоточились на малоизученной химической семье 2‑тиогидантоинов — кольцевых молекулах, которые можно электроночно и структурно настроить. Их цель — выяснить, смогут ли выбранные представители этой семейства связываться с CDK2 сильнее и более селективно, чем собственная «топливная» молекула клетки, ATP, при минимальном взаимодействии с другими киназами.
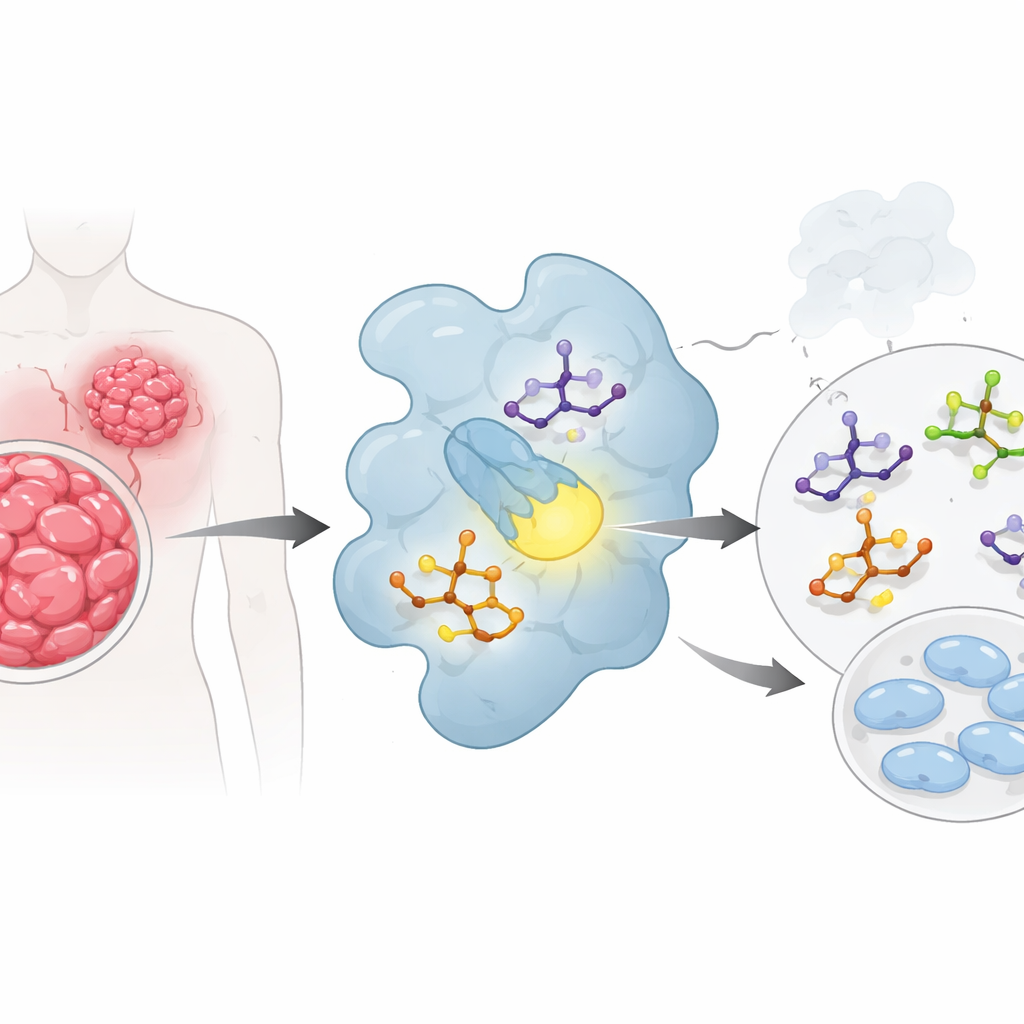
Использование компьютеров для «предварительной проверки» кандидатов в лекарства
Вместо того чтобы сразу идти к лабораторному столу, команда сначала применила несколько уровней квантовой химии и молекулярного моделирования, чтобы понять поведение своих молекул. Они вычисляли, насколько легко каждый соединение перераспределяет электроны в своей структуре, насколько оно полярно и какие участки молекулы наиболее склонны к образованию привлекательных контактов с белком. Соединения, обозначенные как 2b–2e, выделялись: у них были небольшие энергетические разрывы между ключевыми электронными состояниями и высокая «электрофильность», то есть они должны активно взаимодействовать с биологическими партнерами. Карты электрического потенциала поверхности каждой молекулы выявляли сильно отрицательные области вокруг атомов кислорода и серы и положительные области вокруг отдельных водородов — естественные «горячие точки» для водородных связей, когда препарат встраивается в белковый карман.
Проверка вхождения в карман CDK2
Следующим шагом стал виртуальный докинг: размещение каждого кандидата в трехмерной структуре CDK2 с поиском оптимального соответствия, как подбор ключа к замку. В этих симуляциях несколько молекул, особенно 2b, 2c и 2d, сцеплялись с CDK2 крепче, чем сам ATP. Они формировали критические водородные связи с двумя остатками — Lys33 и Thr14, расположенными в центре ATP-связывающего кармана, и также плотно упирались в гидрофобные аминокислоты, выстилающие полость. В отличие от этого, исходный скелет без целевых заместителей связывался слабо, что подчёркивает, насколько тонкие химические модификации кольца могут радикально изменить эффективность.
Наблюдение за движением комплекса белок–препарат
Поскольку белки и лекарства не являются жесткими объектами, авторы провели молекулярно-динамические симуляции — фактически замедленные «фильмы» на атомном уровне — на интервале в десять миллиардных долей секунды. Они показали, что общая форма CDK2 оставалась стабильной, в то время как некоторые пары «лекарство–белок» качались или даже удалялись. Одна молекула, 2f, оказалась исключительно устойчивой: она почти не смещалась в кармане и в среднем сохраняла почти три водородные связи с белком. Другие, такие как 2c и 2d, сочетали сильное связывание с умеренной гибкостью. Чтобы свести эти движения к общей «липкости» связывания, команда использовала метод MM‑PBSA для оценки свободной энергии связывания. Здесь соединение 2d показало себя как лучший универсальный кандидат, с особенно благоприятным балансом между притягивающими силами внутри кармана и энергетическими затратами при выходе из окружающего растворителя.
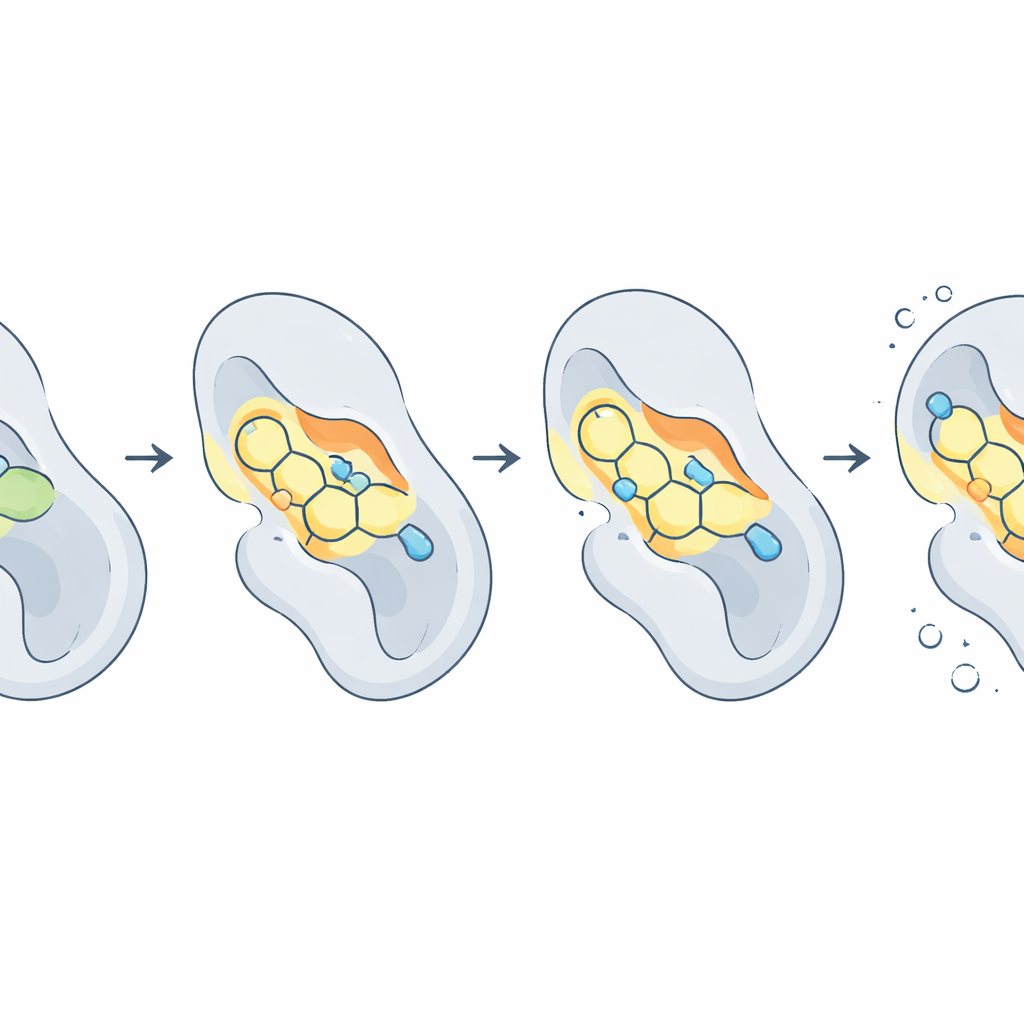
Что это может значить для пациентов
В сумме симуляции выделяют четыре соединения 2‑тиогидантоина — 2b, 2c, 2d и 2f — как особенно перспективные отправные точки для разработки противораковых препаратов. Они сочетают благоприятные электронные свойства, прочное и правильно ориентированное удержание CDK2 и, в случае 2d, особенно выгодную суммарную энергию связывания. Хотя эти выводы чисто вычислительные и требуют экспериментального подтверждения, они дают химикам подробный план: куда поместить галоген, карбоновую группу или эфир на основном кольце, чтобы усилить связывание и селективность. Если последующие лабораторные тесты подтвердят эти предсказания, работа может ускорить создание более точечных терапий против CDK2, замедляющих рост опухолей и при этом щадящих здоровые клетки.
Цитирование: Khaled, N.A., Ahmed, S.A., Ibrahim, M.A. et al. Integrated DFT, molecular docking, and molecular dynamics investigation of some novel 2-thiohydantoin analogues as potent CDK2 inhibitors for anticancer therapy. Sci Rep 16, 10985 (2026). https://doi.org/10.1038/s41598-026-42330-4
Ключевые слова: ингибиторы CDK2, таргетная противораковая терапия, молекулярный докинг, 2-тиогидантоин, компьютерное проектирование лекарств