Clear Sky Science · he
מחקר משולב DFT, העיגון המולקולרי ודינמיקה מולקולרית של אנלוגים חדשים של 2‑תיאוהידנטואין כמעכבים חזקים של CDK2 לטיפול אנטי‑סרטן
מדוע מחקר זה חשוב לטיפול בסרטן בעתיד
תרופות נגד סרטן לעיתים פועלות ככלים גסים שפוגעים בתאים בריאים בזמן שהן תוקפות גידולים. מאמר זה בוחן אסטרטגיה מדויקת יותר: תכנון מולקולות קטנות שיכבות באופן סלקטיבי מנוע מרכזי של חלוקת התאים — חלבון בשם CDK2. באמצעות סימולציות ממוחשבות מתקדמות במקום כימיה של ניסוי‑ושגיאה, החוקרים מזהים מספר מולקולות מועמדות מבטיחות שעשויות יום אחד להפוך לתרופות אנטי‑סרטן בטוחות וממוקדות יותר.
עוצרים את חלוקת התאים המתמשכת בבסיסה
ממאירות רבות גדלות כיוון שמחזור התא — השעון הפנימי שמווסת מתי תאים מתחלקים — יצא משליטה. CDK2 הוא אחד המתגים המרכזיים שמניעים את התאים דרך מחזור זה. תרופות קודמות שניסו לחסום את CDK2 הראו הבטחה, אך לעיתים קרובות פגעו גם בחלבונים קרובים החיוניים לתאי בריא, וגרמו לתופעות לוואי. המחברים מתמקדים במשפחת־חומרים שרק מעט נחקרה, 2‑תיאוהידנטואינים, מולקולות טבעתיות שניתן לכוונן אותן מבחינה אלקטרונית ומבנית. מטרתם היא לבדוק האם חברים נבחרים במשפחה זו יכולים להיקשר ל‑CDK2 בעוצמה ובסלקטיביות גבוהה יותר ממולקולת הדלק של התא, ATP, ובו־זמנית להמנע מקינאזות אחרות.
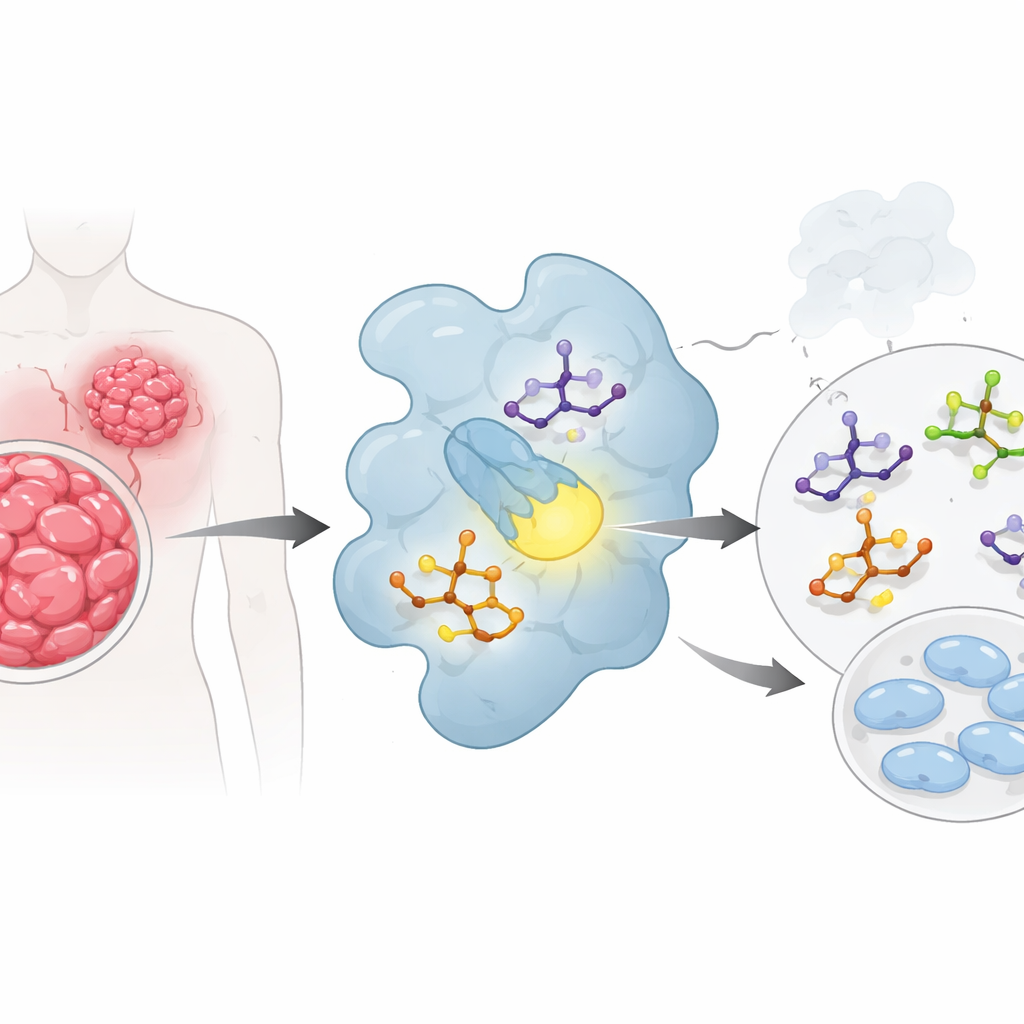
שימוש במחשבים כדי "לבדוק מראש" מועמדים לתרופה
במקום לעבור ישירות לספסל המעבדה, הצוות השתמש תחילה במספר שכבות של כימיה קוונטית ודוגמנות מולקולרית כדי להבין כיצד המולקולות שלהם מתנהגות. הם חישבו כמה בקלות כל תרכובת יכולה להזיז אלקטרונים במבנה שלה, כמה היא פולרית ואילו חלקים במולקולה סביר שייצרו אינטראקציות אטרקטיביות עם חלבון. תרכובות המסומנות 2b עד 2e בלטו: להן היו פערי אנרגיה קטנים בין המצבים האלקטרוניים המרכזיים ו"אלקטרופיליות" גבוהה, כלומר הן צפויות להגיב בקלות עם שותפים ביולוגיים. מפות של משטח החשמל של כל מולקולה הדגישו אזורים שליליים חזקים סביב אטומי חמצן וגופרית ואזורים חיוביים סביב מימנים מסוימים — נקודות חמות טבעיות ליצירת קשרי מימן כאשר תרופה שוקעת בכיס חלבוני.
בדיקת ההתאמה בתוך כיס ה‑CDK2
השלב הבא היה עיגון וירטואלי: הצבת כל מועמד במבנה התלת‑ממדי של CDK2 ומתן למחשב לחפש את ההתאמה הטובה ביותר, בדומה לנסיון מפתחות במנעול. מספר מולקולות, ובמיוחד 2b, 2c ו‑2d, התקשרו ל‑CDK2 בחוזקה יותר מאשר ATP עצמו בסימולציות אלה. הן יצרו קשרי מימן מכריעים עם שתי שיירות, Lys33 ו‑Thr14, שנמצאות בלב כיס קשירת ה‑ATP, והן גם התקבצו בנוחות לצד חומצות אמינו הידרופוביות שמרפדות את המתא. לעומת זאת, השלד המקורי ללא תחליפים מותאמים התקשר בחולשה, מה שמדגיש כיצד שינויים עדינים בקישוט הכימי של הטבעת יכולים לשנות את הביצועים באופן דרמטי.
צפייה במורכבות חלבון־תרופה בתנועה
מאחר שחלבונים ותרופות אינם נוקשים, המחברים הריצו סימולציות דינמיקה מולקולרית — מעין סרטים באיטיות בקנה‑מידת אטומים — לאורך עשר מיליארדי השניות (ננוסקונד). אלה הראו שהצורה הכוללת של CDK2 נשארה יציבה בעוד שחלק מזוגות תרופה‑חלבון רעדו או אפילו סטו החוצה. מולקולה אחת, 2f, התגלתה כיציבה במיוחד, כמעט ולא הזיזה את מיקומה בתוך הכיס ושמרה בממוצע על כמעט שלושה קשרי מימן עם החלבון. אחרות, כמו 2c ו‑2d, שילבו קשירה חזקה עם גמישות מתונה. כדי לתרגם תנועות אלה ל"דביקות" כוללת, הצוות השתמש בטכניקת MM‑PBSA להערכת אנרגיות חיבור חופשיות. כאן, תרכובת 2d בלטה כביצועית הטובה מכל, עם איזון פרופורציונלי במיוחד בין כוחות אטרקטיביים בתוך הכיס והעלות האנרגטית של יציאה מסביבה הממס.
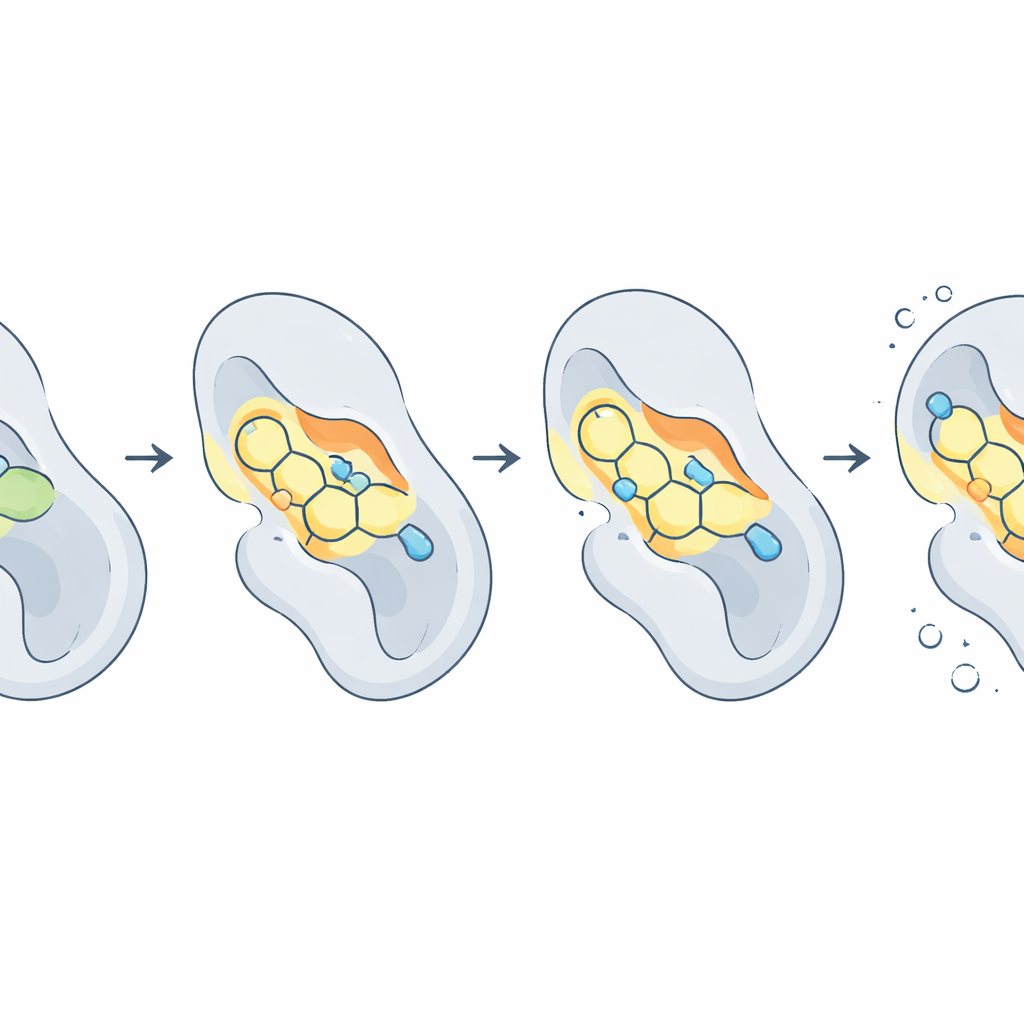
מה זה יכול להסביר עבור מטופלים
ביחד, הסימולציות מדגישות ארבע תרכובות 2‑תיאוהידנטואין — 2b, 2c, 2d ו‑2f — כנקודות התחלה מבטיחות במיוחד לפיתוח תרופות אנטי‑סרטן. הן משלבות תכונות אלקטרוניות נוחות, אחיזה חזקה ומכוונת היטב על CDK2, ובמקרה של 2d, אנרגיית קשירה כוללת מיוחדת לטובה. ממצאיהן הן חישוביות טהורות וחייבות עוד אימות ניסיוני, אך הן מספקות מפת דרכים מפורטת לכימאים: היכן להניח קבוצות הלוגן, חומצה או אתר על טבעת הליבה כדי לחזק את הקשירה והסלקטיביות. אם ניסויי מעבדה עתידיים יאמתו תחזיות אלו, העבודה יכולה להאיץ יצירת טיפולים ממוקדי CDK2 מדויקים יותר שעוצרים גדילת גידול תוך שמירה על תאים בריאים.
ציטוט: Khaled, N.A., Ahmed, S.A., Ibrahim, M.A. et al. Integrated DFT, molecular docking, and molecular dynamics investigation of some novel 2-thiohydantoin analogues as potent CDK2 inhibitors for anticancer therapy. Sci Rep 16, 10985 (2026). https://doi.org/10.1038/s41598-026-42330-4
מילות מפתח: מעכבי CDK2, טיפול ממוקד בסרטן, עיגון מולקולרי, 2‑תיאוהידנטואין, עיצוב תרופות חישובי