Clear Sky Science · nl
Geïntegreerd DFT-, moleculair-docking- en moleculaire-dynamicaonderzoek van enkele nieuwe 2-thiohydantoin-analogen als krachtige CDK2-remmers voor kankertherapie
Waarom dit onderzoek belangrijk is voor toekomstige kankerbehandelingen
Kankergeneesmiddelen werken vaak als botte instrumenten: ze beschadigen gezonde cellen terwijl ze tumoren aanvallen. Dit artikel onderzoekt een preciezere strategie: het ontwerpen van kleine moleculen die selectief één belangrijke schakelaar van celdeling uitschakelen, een eiwit genaamd CDK2. Door geavanceerde computersimulaties te gebruiken in plaats van toevalsexperimenten in het laboratorium, identificeren de onderzoekers meerdere veelbelovende kandidaat-moleculen die op termijn veiliger en gerichter als antikankergeneesmiddelen gebruikt zouden kunnen worden.
De ongecontroleerde celdeling bij de bron stoppen
Veel kankers groeien omdat de celcyclus — de interne klok die bepaalt wanneer cellen delen — uit balans is geraakt. CDK2 is een van de belangrijkste schakelaars die cellen door deze cyclus drijft. Vroege geneesmiddelen die CDK2 probeerden te blokkeren lieten veelbelovende resultaten zien, maar vielen vaak ook nauw verwante eiwitten aan die essentieel zijn voor normale cellen, wat tot bijwerkingen leidde. De auteurs richten zich op een weinig onderzochte chemische familie, de 2‑thiohydantoinen: ringvormige moleculen die elektronisch en structureel af te stemmen zijn. Hun doel is na te gaan of geselecteerde leden van deze familie zich sterker en selectiever aan CDK2 kunnen binden dan het cellulaire brandstofmolecuul ATP, en daarbij andere kinasen vermijden.
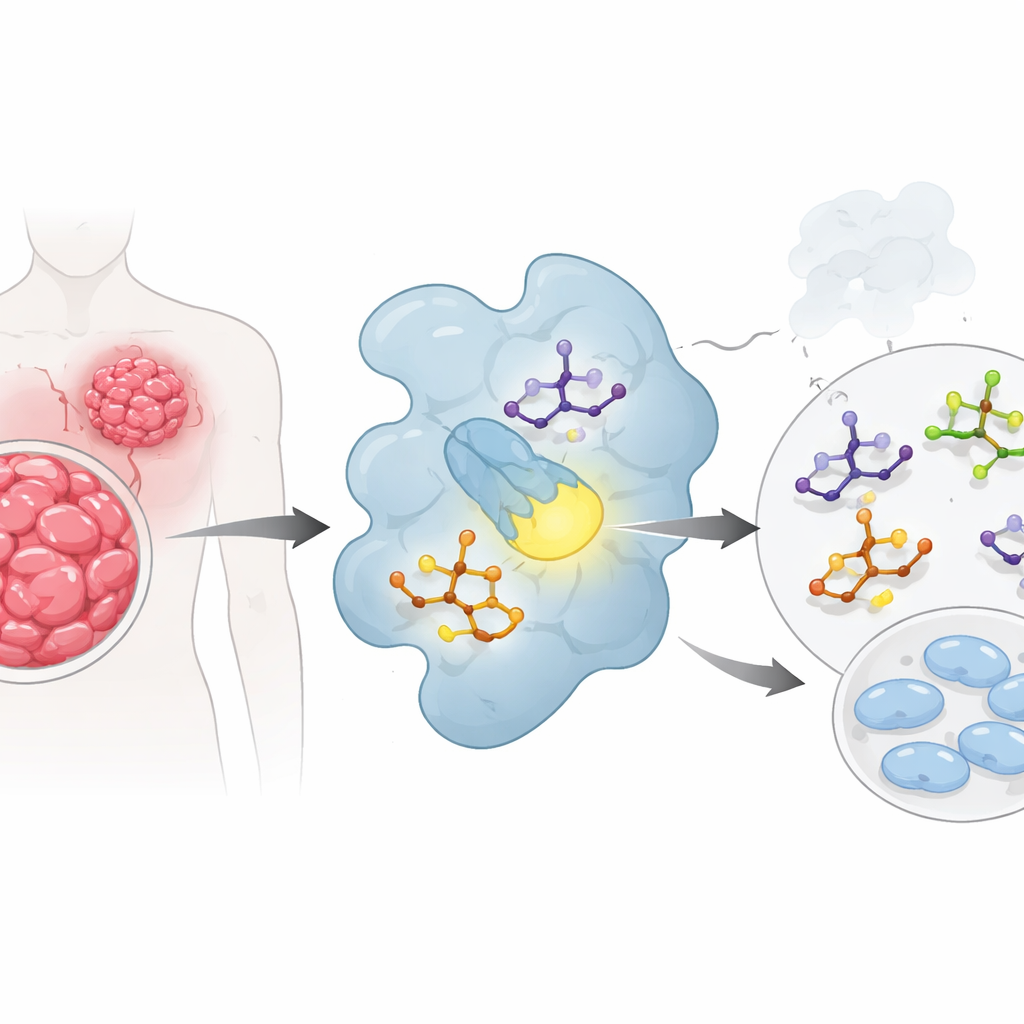
Computers gebruiken om geneesmiddelkandidaten ‘voor te testen’
In plaats van direct naar het lab te gaan, gebruikte het team eerst meerdere lagen van quantumchemie en moleculair modelleren om te begrijpen hoe hun moleculen zich gedragen. Ze berekenden hoe gemakkelijk elk verband elektronen binnen zijn structuur kan verplaatsen, hoe polair het is, en welke delen van het molecuul het meest waarschijnlijk aantrekkelijke contacten met een eiwit vormen. Verbindingen aangeduid als 2b tot en met 2e vielen op: ze hadden kleine energiekloften tussen hun belangrijkste elektronische toestanden en hoge “electrofielheid”, wat betekent dat ze waarschijnlijk gemakkelijk met biologische partners zullen interageren. Kaarten van het elektrische oppervlak van elk molecuul toonden sterk negatieve regio’s rond zuurstof- en zwavelatomen en positieve regio’s rond bepaalde waterstoffen — natuurlijke hotspots voor waterstofbruggen wanneer een geneesmiddel zich in een eiwitbinding nestelt.
Controleren of ze in de CDK2‑pocket passen
De volgende stap was virtueel docken: elk kandidaatmolecuul in de driedimensionale structuur van CDK2 plaatsen en de computer laten zoeken naar de beste passing, vergelijkbaar met sleutels in een slot proberen. Meerdere moleculen, vooral 2b, 2c en 2d, bonden in deze simulaties sterker aan CDK2 dan ATP zelf. Ze vormden cruciale waterstofbruggen met twee residuen, Lys33 en Thr14, die zich in het hart van het ATP-bindingsvak bevinden, en ze lagen ook stevig tegen hydrofobe aminozuren die de holte bekleden. Ter vergelijking: het basale skelet zonder specifieke substituties bond zwak, wat benadrukt hoe subtiele veranderingen in de chemische decoratie van de ring de prestaties sterk kunnen beïnvloeden.
Het eiwit‑geneesmiddeldeel in beweging volgen
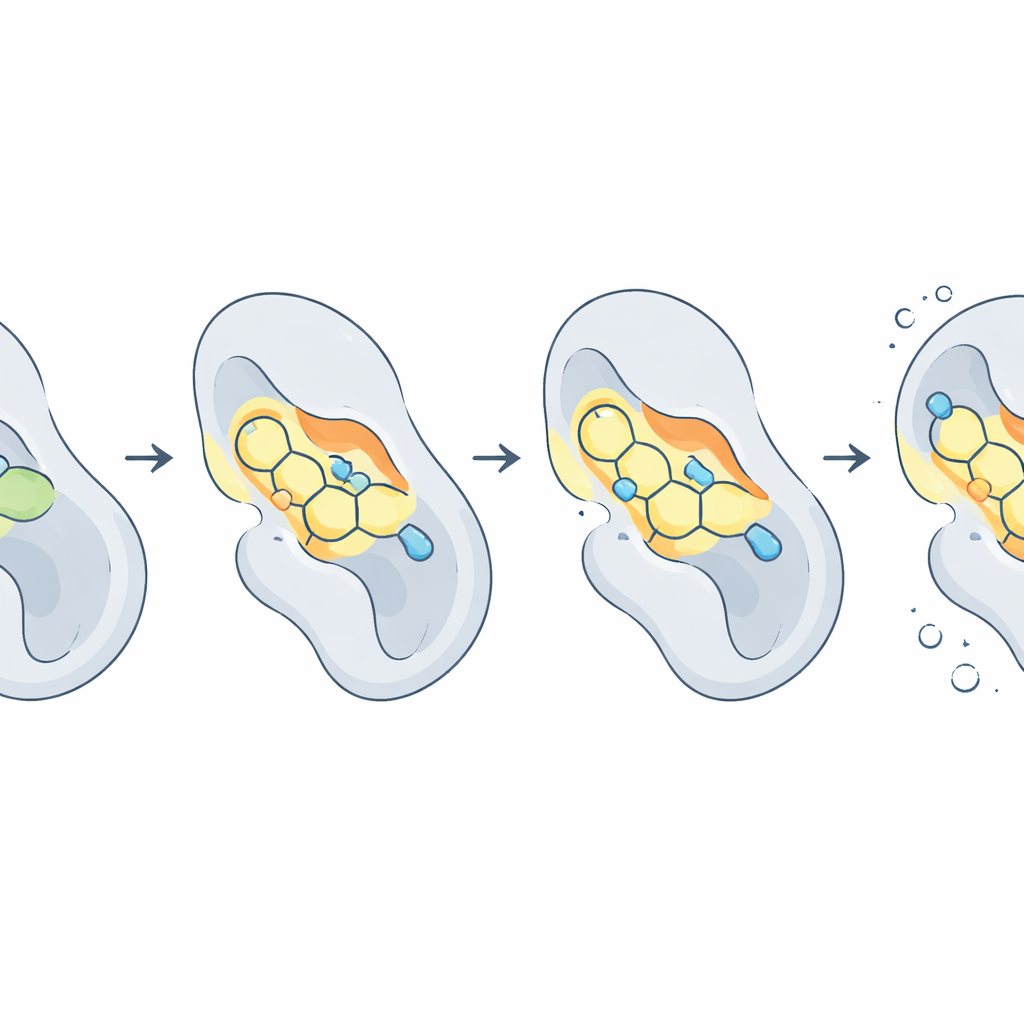
Aangezien eiwitten en geneesmiddelen niet star zijn, voerden de auteurs moleculaire dynamicasimulaties uit — in wezen slowmotionfilms op atomaire schaal — over tien miljardsten van een seconde. Deze toonden dat de algemene vorm van CDK2 stabiel bleef, terwijl sommige eiwit–geneesmiddelparen wiebelden of zelfs wegdreven. Eén molecuul, 2f, bleek uitzonderlijk stabiel: het verschoof nauwelijks binnen de pocket en hield gemiddeld bijna drie waterstofbruggen met het eiwit in stand. Andere, zoals 2c en 2d, combineerden sterke binding met matige flexibiliteit. Om deze bewegingen te vertalen naar een algemene “plakkerigheid” gebruikte het team een techniek genaamd MM‑PBSA om bindingsvrije energieën te schatten. Hierbij kwam verbinding 2d naar voren als de beste allrounder, met een bijzonder gunstige balans tussen aantrekkingskrachten in de pocket en de energiekost van het verlaten van het omringende oplosmiddel.
Wat dit voor patiënten zou kunnen betekenen
Gecombineerd benadrukken de simulaties vier 2‑thiohydantoinverbindingen — 2b, 2c, 2d en 2f — als bijzonder veelbelovende uitgangspunten voor de ontwikkeling van antikankergeneesmiddelen. Ze combineren gunstige elektronische eigenschappen, een sterke en goed georiënteerde greep op CDK2 en, in het geval van 2d, een bijzonder voordelige totale bindingsenergie. Hoewel deze bevindingen puur computationeel zijn en nog experimenteel bevestigd moeten worden, bieden ze chemici een gedetailleerd stappenplan: waar halogeen-, zure of estergroepen op de kerkring geplaatst kunnen worden om binding en selectiviteit te versterken. Als toekomstige laboratoriumtesten deze voorspellingen ondersteunen, kan dit werk de ontwikkeling versnellen van preciezere CDK2‑gerichte therapieën die tumorgroei vertragen en tegelijkertijd gezonde cellen sparen.
Bronvermelding: Khaled, N.A., Ahmed, S.A., Ibrahim, M.A. et al. Integrated DFT, molecular docking, and molecular dynamics investigation of some novel 2-thiohydantoin analogues as potent CDK2 inhibitors for anticancer therapy. Sci Rep 16, 10985 (2026). https://doi.org/10.1038/s41598-026-42330-4
Trefwoorden: CDK2-remmers, gerichte kankertherapie, moleculair docken, 2-thiohydantoin, computationeel geneesmiddelontwerp