Clear Sky Science · zh
来自脑脊液的临床分离株 Streptococcus suis ST1 的基因组分析揭示了抗菌耐药性、毒力特征及其与 ST7 的进化联系
为何一种猪源细菌会牵动人类健康
大多数人认为畜牧场的感染主要影响动物,而非人类。但某些病原体能够从猪传播到人,并引发危及生命的疾病。本研究聚焦于这样一种细菌——猪链球菌(Streptococcus suis),它可导致严重的脑膜炎并造成长期听力损失。通过解析来自患者脑脊液的菌株完整基因组,研究者展示了该病原如何抗衡关键抗生素、有哪些使其特别致病的因素,以及它如何与导致致命暴发的相关菌株共同进化。

一位患者、一次腰椎穿刺与潜伏的威胁
故事始于一名因化脓性脑膜炎入重症监护的患者,这是一种严重的脑部感染。医生在患者的脑脊液中分离出 S. suis,证实一种与猪相关的病原已侵入中枢神经系统。治疗后,患者的意识有所好转,但留下了严重的听力损失,这是一种该感染的常见并发症。这个真实病例为科学家提供了难得的机会:研究来自人源的菌株(命名为 366)的 DNA,探究其基因组中哪些特征可以解释其在体内的行为及对治疗的反应。
哪些药物仍有效——哪些已失效
在实验室中,团队测试了该菌株对常用抗生素的敏感性。结果显示,366 型对若干一线药物仍然敏感,包括青霉素、头孢菌素,以及作为最后防线的碳青霉烯类和万古霉素。然而,它对红霉素、克林霉素和四环素类表现出强烈耐药——这些药物在人用和兽用领域都被广泛使用。基因组扫描发现了两个耐药基因 ermB 和 tet(O),它们改变细菌的蛋白合成机制,使这些药物难以有效结合。有趣的是,这些耐药基因位于染色体主干上,而非位于易于传播的可移动 DNA 元件,提示该菌株的耐药性更可能通过成功菌株谱系的扩张传播,而非快速的基因交换。
关于致病机制的遗传线索
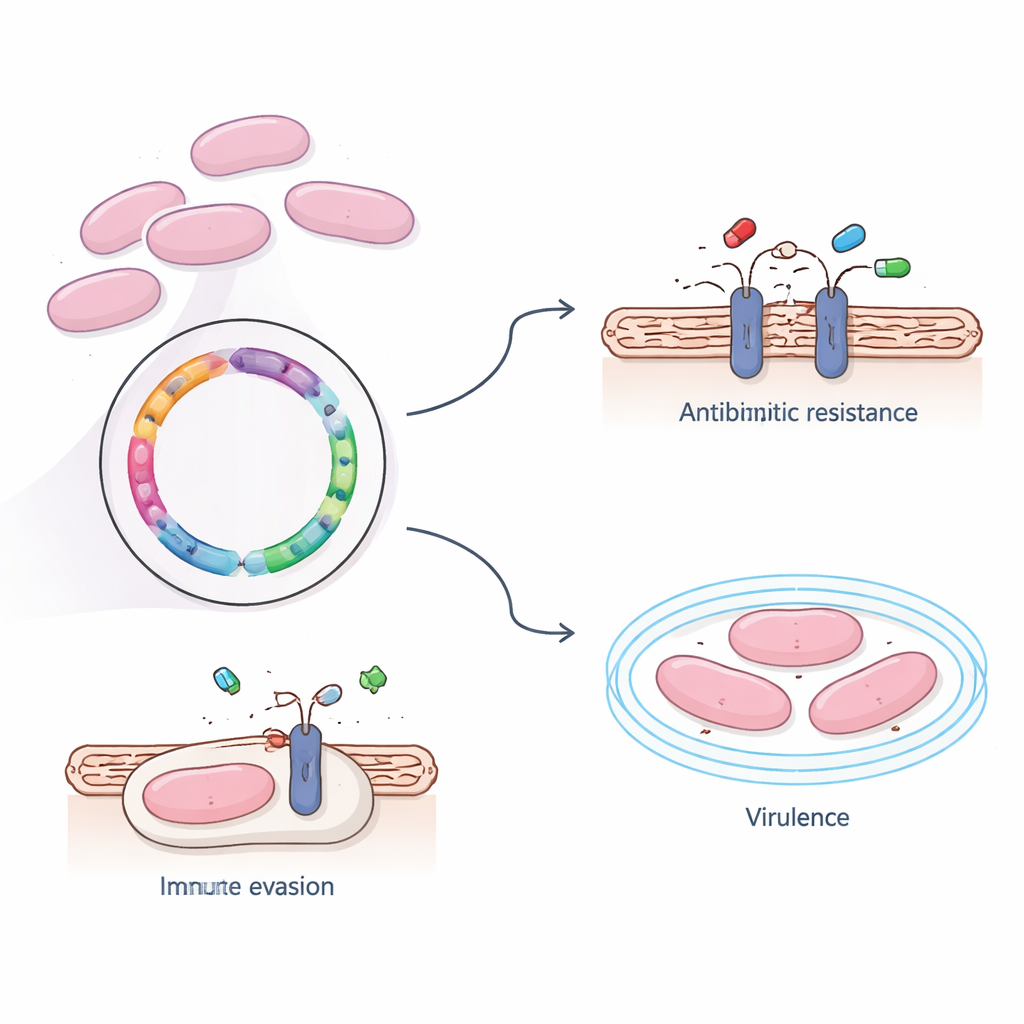
除了耐药性,研究人员还探寻使该菌株能够在血液中存活并侵入脑部的因素。借助多个大型参考数据库,他们鉴定出四个与毒力相关的关键基因。其中三个参与构建包裹细菌的糖衣荚膜,能保护细菌免于被免疫细胞识别与吞噬;第四个基因帮助病原黏附宿主组织。对全基因组的宏观分析表明,许多基因支持基础生命功能,如代谢和蛋白质合成,但也凸显了若干转运系统,这些系统负责将养分、毒素以及可能的药物穿膜运输。其中一个主要通路——被称为 ABC 转运系统——突出为导入有用分子与排出有害物质(可能包括抗生素)的中心枢纽。
危险菌株之间的家族关系
为将该患者的菌株置于更广泛的背景中,研究团队将其基因组与来自不同地区猪和人分离的相关 S. suis 菌株进行了比较。他们发现 366 属于序列类型 ST1,这一遗传谱系已知在人体感染中占主导地位。通过使用成千上万个微小的 DNA 差异构建进化树,研究表明 ST1 与另一个被称为 ST7 的谱系关系密切,后者曾与大规模暴发相关。泛基因组分析——考察多个菌株间哪些基因是共享或独有的——显示 ST1 与 ST7 之间存在大量共同核心基因,支持一种观点:流行性 ST7 菌株是在 ST1 背景上通过获得额外遗传物质直接演化而来。
对公共卫生的意义
综合来看,研究结果描绘出一种高度适应的猪源病原,它携带一整套既能抵抗治疗又能致使严重疾病的工具箱,并已跨入人类群体。该患者菌株在染色体上编码了对若干广泛使用抗生素的稳定耐药性,同时具备帮助其逃避免疫攻击并黏附人组织的关键基因。与此同时,与暴发相关谱系的密切亲缘关系表明,危险变体可能从同一族谱中出现。通过剖析来自单一、记录完备的临床分离株的基因组,本研究深化了我们对 S. suis ST1 如何运作与进化的理解,为更有效的监测、更合理的抗生素使用以及更有针对性的防控策略提供了基础,以保护农场工人和更广泛的公众健康。
引用: Jiang, J., Duan, W. & Liang, L. Genomic analysis of a clinical Streptococcus suis ST1 isolate from CSF reveals antimicrobial resistance, virulence, and an evolutionary link to ST7. Sci Rep 16, 11271 (2026). https://doi.org/10.1038/s41598-026-41475-6
关键词: 猪链球菌, 人畜共患性脑膜炎, 抗生素耐药性, 细菌基因组学, 猪到人传播感染