Clear Sky Science · zh
SMC-LUD:用于肝细胞癌与血管瘤分类的大规模 B 超肝脏影像数据集
这对日常健康为何重要
肝癌是全球最致命的癌症之一,部分原因在于很难在能获得有效治疗的早期被发现和准确分型。医生常依赖超声检查——一种快速且经济的扫描方式——来寻找肝脏中的可疑病灶。但在这些颗粒状的黑白影像上,危险的肿瘤与无害的增生常常在外观上极为相似,即便是专家也会感到困惑。本文介绍了一个新的大型图像集合,旨在帮助计算机学会区分两类病变,从而有望提升肝脏筛查的准确性并扩大可及性。
更细看肝脏上的发现
肝脏影像上常见的两类病灶在风险上处于截然不同的两端。肝细胞癌是原发性肝癌,如果漏诊或发现较晚,可能危及生命。相比之下,血管瘤通常是由血管聚集形成的良性病变,极少需要治疗。然而在基础超声图像上,这两者常难以区分,尤其是在肝组织已受损或病灶较小时。今天,医生往往需要安排额外检查,如 CT 或 MRI,以获得确诊置信度,但这会增加费用、耗时,并带来放射或造影剂暴露。
构建大规模肝脏影像库
为了解决这一问题,首尔三星医疗中心的研究人员整理了 SMC-LUD,这是一个新的公开数据集,包含 2015 至 2024 年间 1,021 名真实患者的 5,385 张肝脏超声图像。每张图像均显示一个肝脏病灶,并被细致地归类为两类之一:癌症(肝细胞癌,2,716 张)或良性血管瘤(2,669 张)。癌症病例通过术中或活检获得的组织学检查确诊,血管瘤则由经验丰富的放射科医师根据典型影像学特征作出诊断。所有图像均已匿名化、按患者分组,并由专家复核以确保标签可靠。 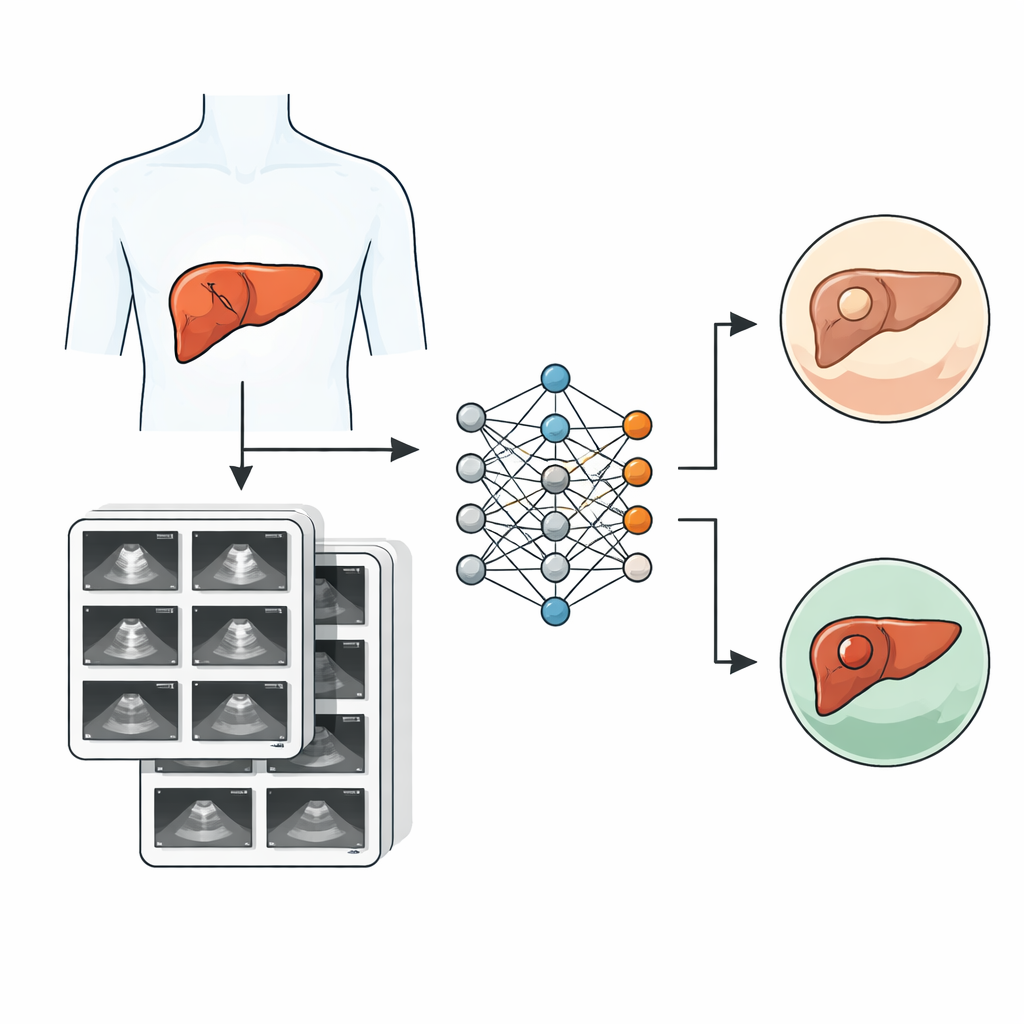
为智能算法准备数据
研究团队按便于人工智能研究者使用的方式组织了数据集。图像被统一调整大小和标准化,使计算模型以一致格式读取,且数据被划分为训练、微调和最终测试的独立组,确保同一患者的图像不会出现在多个组中。数据集提供两种版本:“Clean” 版本不含测量标记,“Caliper” 版本包含这些标记。为保证公平测试,研究者仅在 Clean 图像上训练模型,以避免算法通过学习标记模式来作弊、而非专注于病灶本身。附带的患者信息表(例如癌症病例的肿瘤大小和分期)支持更深入的临床分析。
计算机如何学会“看见”
为展示该资源的潜力,作者构建了一个基于知名图像识别框架的深度学习模型,并用特殊的“注意力”模块对其进行增强。这些组件帮助网络聚焦于图像中最有信息的部分以及亮度与纹理的关键模式。模型设计采用两条并行分支,对相同特征以略有不同的方式处理后再合并,随后应用空间滤波以突显重要区域,类似放射科医师在脑海中放大可疑区域的过程。在 SMC-LUD Clean 子集上训练后,该模型与多种常见的医学影像神经网络结构进行了比较。 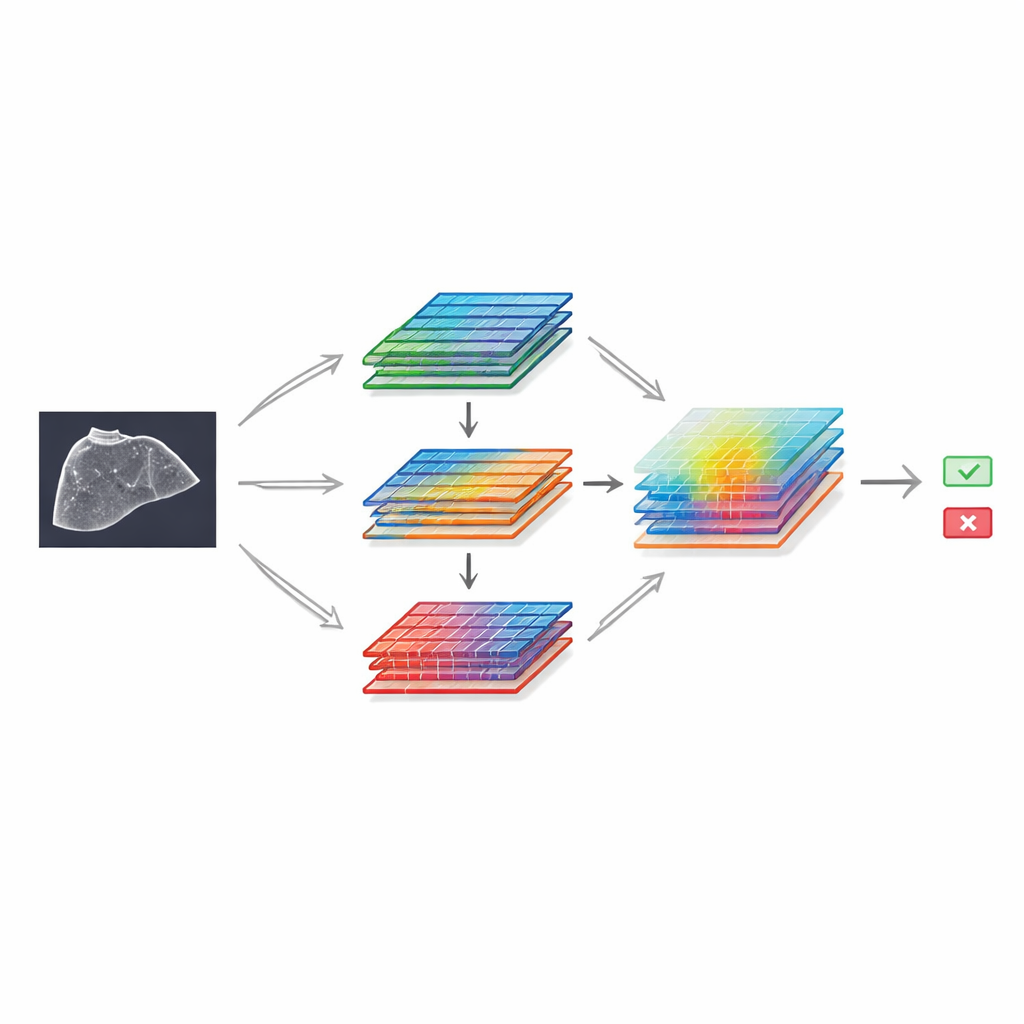
结果说明了什么
在保留的测试图像上,这一增强注意力模型在区分肝癌与血管瘤方面的准确率接近 99%,优于比较模型。从网络内部计算得到的热图显示,模型倾向于关注病灶本身而不是无关的图像细节,这表明它学习到了有医学意义的线索。尽管该研究仅评估了恶性与良性中两类病变的二分类任务,但其性能既反映了图像标签的高质量,也展示了在提供足够大且组织良好的数据时,基于超声的计算诊断潜力。
这对患者可能意味着什么
对非专业读者而言,关键信息是:该数据集本身并不会立即改变医生解读你下一次扫描的方式——但它奠定了重要基础。通过自由共享一个大规模且经严格验证的超声图像库,作者为全球研究者提供了训练与测试更智能肝脏筛查工具的原材料。未来,此类工具可作为“第二只眼睛”,标记值得进一步关注的可疑病灶,并减少对明确良性发现的非必要随访。最终,这或有助于将肝癌诊断推向更早、更易治疗的阶段,同时控制成本与复杂性。
引用: Tak, J., Ko, RE., Kwon, R.D. et al. SMC-LUD:Large-Scale B-Mode Liver Ultrasound Dataset for Hepatocellular Carcinoma and Hemangioma Classification. Sci Data 13, 649 (2026). https://doi.org/10.1038/s41597-026-07023-7
关键词: 肝脏超声, 肝细胞癌, 血管瘤, 深度学习, 医学影像数据集