Clear Sky Science · it
SMC-LUD:Dataset ecografico B-mode su larga scala per la classificazione di carcinoma epatocellulare e emangioma
Perché è importante per la salute quotidiana
Il cancro al fegato è uno dei tumori più letali al mondo, in parte perché è difficile da individuare e classificare abbastanza presto da poter intervenire efficacemente. I medici ricorrono spesso all’ecografia, un esame rapido e poco costoso, per cercare lesioni sospette nel fegato. Ma in queste immagini granulose in bianco e nero, tumori pericolosi e formazioni benigne possono apparire sorprendentemente simili, anche per gli specialisti. Questo articolo presenta una nuova ampia raccolta di immagini progettata per aiutare i computer a imparare a distinguerle, con il potenziale di rendere i controlli epatici più accurati e più accessibili.
Uno sguardo più ravvicinato alle lesioni epatiche
Due reperti comuni nelle scansioni epatiche si collocano agli estremi dello spettro di rischio. Il carcinoma epatocellulare è un tumore primario del fegato che può mettere in pericolo la vita se non viene riconosciuto o viene scoperto in fase avanzata. Gli emangiomi, al contrario, sono di solito aggregati benigni di vasi sanguigni che raramente richiedono trattamento. Nelle immagini ecografiche di base, tuttavia, queste due entità possono essere difficili da distinguere, specialmente quando il tessuto epatico è già danneggiato o quando le lesioni sono di piccole dimensioni. Oggi i medici spesso devono prescrivere esami aggiuntivi come TC o risonanza magnetica per avere certezza, con costi, tempi e l’esposizione a radiazioni o a mezzi di contrasto.
Creare una grande libreria di immagini epatiche
Per affrontare questo problema, i ricercatori del Samsung Medical Center di Seoul hanno messo insieme SMC-LUD, una nuova raccolta pubblica di 5.385 immagini ecografiche epatiche provenienti da 1.021 pazienti reali esaminati tra il 2015 e il 2024. Ogni immagine mostra una lesione epatica che è stata accuratamente classificata in uno dei due gruppi: cancro (carcinoma epatocellulare, 2.716 immagini) o emangioma benigno (2.669 immagini). I casi di cancro sono stati confermati esaminando il tessuto rimosso durante intervento chirurgico o biopsia, mentre gli emangiomi sono stati diagnosticati usando caratteristiche tipiche osservate nelle scansioni interpretate da radiologi esperti. Tutte le immagini sono state anonimizzate, raggruppate per paziente e ricontrollate da specialisti per garantire etichette affidabili. 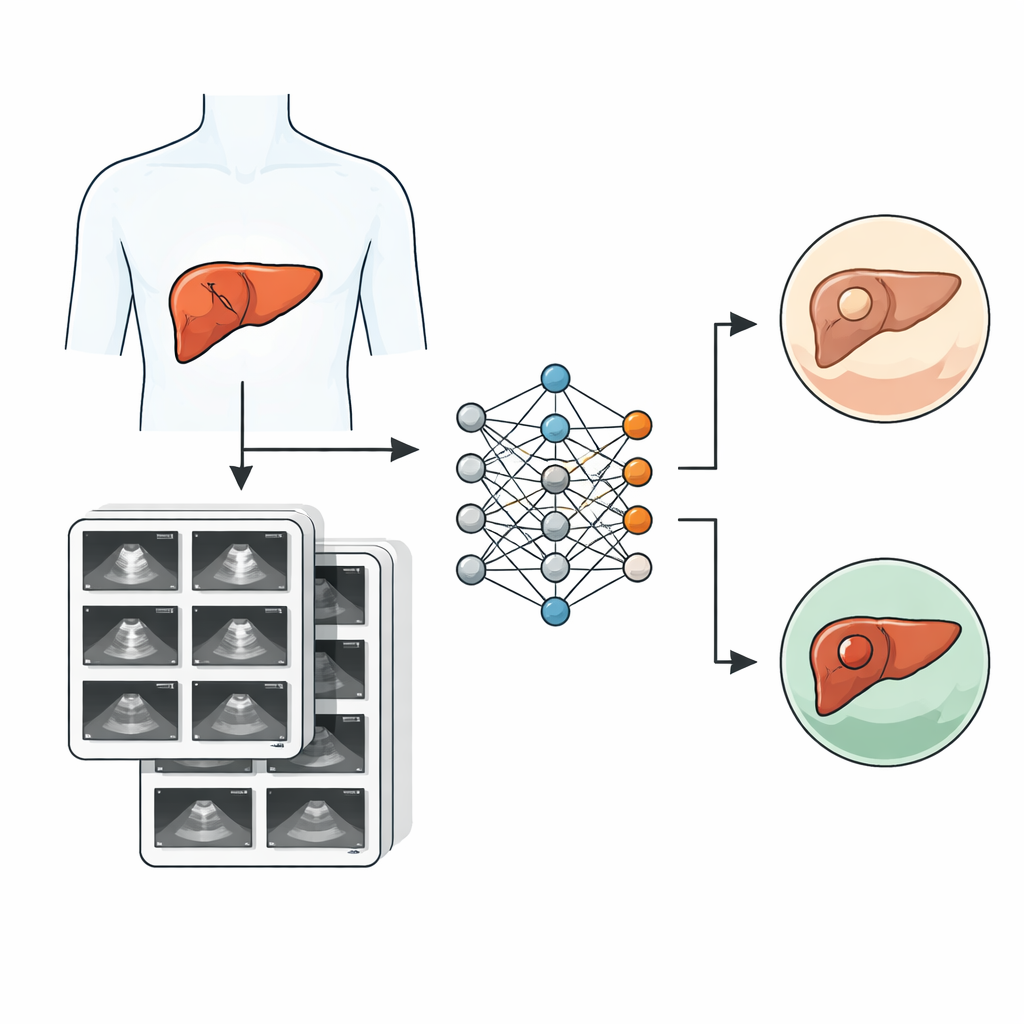
Preparare i dati per algoritmi intelligenti
Il team ha organizzato il dataset in modo da renderlo facile da usare per i ricercatori in intelligenza artificiale. Le immagini sono state ridimensionate e standardizzate in modo che i modelli informatici le vedano in un formato coerente, e i dati sono stati suddivisi in gruppi separati per addestramento, messa a punto e test finale, con la cura di non includere immagini dello stesso paziente in più di un gruppo. Il dataset è disponibile in due versioni: una versione “Clean” senza marcatori di misura e una versione “Caliper” che li include. Per testare in modo equo, i ricercatori hanno addestrato i loro modelli solo sulle immagini Clean per evitare che gli algoritmi barassero imparando ad associare i motivi dei marcatori a certe diagnosi invece di concentrarsi sulle lesioni stesse. Una tabella di accompagnamento con informazioni sul paziente, come la dimensione del tumore e lo stadio nei casi di cancro, permette analisi cliniche più approfondite.
Come il computer impara a vedere
Per mostrare cosa si può ottenere con questa risorsa, gli autori hanno costruito un modello di deep learning basato su un noto framework di riconoscimento delle immagini e lo hanno potenziato con speciali moduli di “attention”. Questi componenti aiutano la rete a focalizzarsi sulle parti più informative dell’immagine e sui pattern più rivelatori di luminosità e texture. Il progetto utilizza due rami paralleli che elaborano gli stessi elementi in modo leggermente diverso prima di ricongiungersi e applicare quindi un filtro spaziale che mette in evidenza le regioni importanti, un po’ come un radiologo che mentalmente zooma su un’area sospetta. Addestrato sul sottoinsieme Clean di SMC-LUD, questo modello è stato confrontato con diversi noti design di reti neurali per imaging medico. 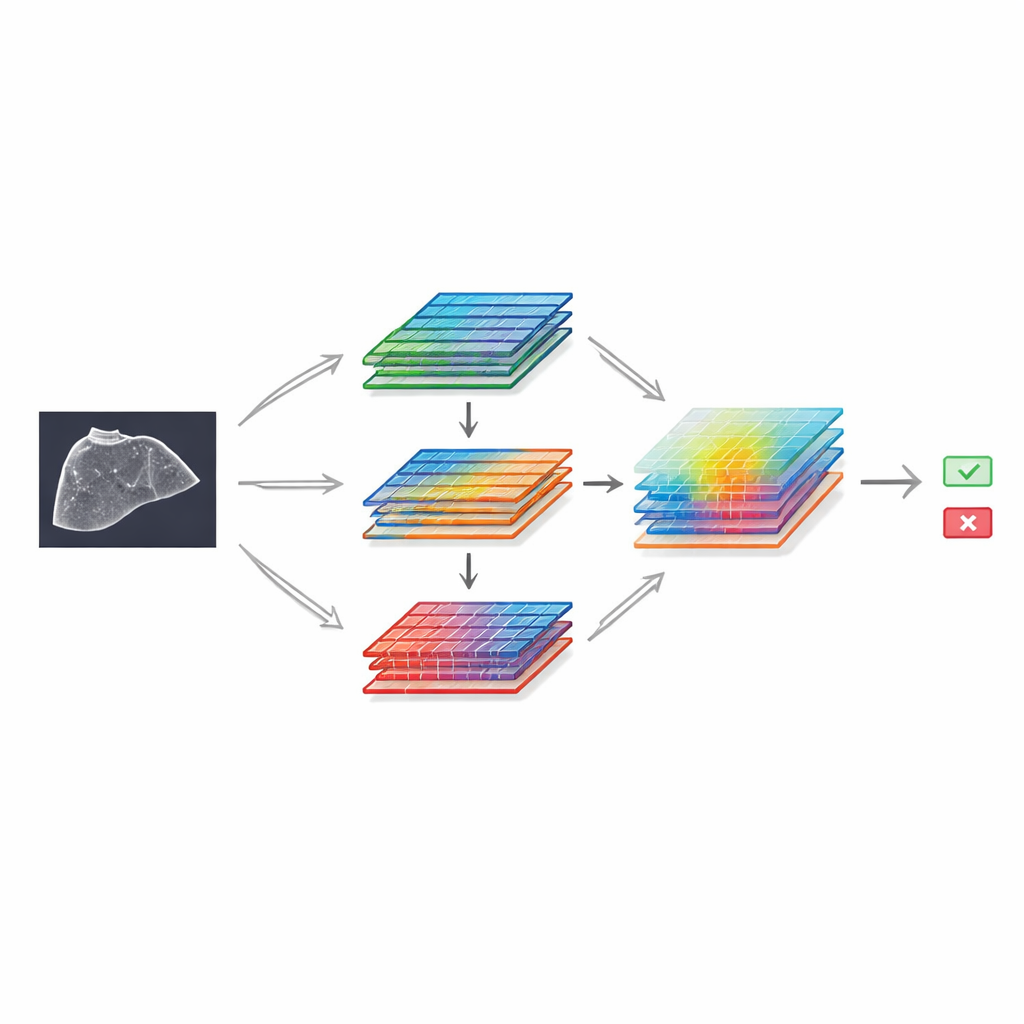
Cosa mostrano i risultati
Sulle immagini di test tenute separate, il modello con attention ha distinto correttamente carcinoma epatocellulare ed emangioma in quasi il 99% dei casi, superando i modelli di confronto. Le mappe di calore derivate dai calcoli interni della rete hanno mostrato che essa tendeva a concentrarsi sulle lesioni stesse piuttosto che su dettagli dell’immagine non correlati, suggerendo che stava apprendendo indizi di rilievo medico. Anche se questo studio valuta solo una distinzione binaria tra un tipo maligno e un tipo benigno, le prestazioni evidenziano sia la qualità delle etichette delle immagini sia il potenziale della diagnosi computerizzata basata su ecografia quando viene alimentata con dati sufficientemente numerosi e ben organizzati.
Cosa potrebbe significare per i pazienti
Per i non specialisti, il messaggio chiave è che questo dataset da solo non cambia il modo in cui il tuo medico interpreterà la prossima ecografia — ma pone fondamenta importanti. Condividendo liberamente una vasta libreria di immagini ecografiche accuratamente verificate, gli autori forniscono ai ricercatori di tutto il mondo la materia prima necessaria per addestrare e testare strumenti più intelligenti per lo screening del fegato. In futuro, tali strumenti potrebbero funzionare come un secondo paio di occhi, segnalando aree preoccupanti che meritano maggiore attenzione e riducendo i follow-up inutili per reperti chiaramente benigni. In ultima istanza, questo potrebbe contribuire a spostare la diagnosi del cancro al fegato verso fasi più precoci e trattabili, mantenendo sotto controllo costi e complessità.
Citazione: Tak, J., Ko, RE., Kwon, R.D. et al. SMC-LUD:Large-Scale B-Mode Liver Ultrasound Dataset for Hepatocellular Carcinoma and Hemangioma Classification. Sci Data 13, 649 (2026). https://doi.org/10.1038/s41597-026-07023-7
Parole chiave: ecografia epatica, carcinoma epatocellulare, emangioma, deep learning, dataset di imaging medico