Clear Sky Science · pl
SMC-LUD: Duży zbiór obrazów ultradźwiękowych w trybie B wątroby do klasyfikacji raka wątrobowokomórkowego i naczyniaka
Dlaczego to ma znaczenie dla codziennego zdrowia
Rak wątroby jest jednym z najgroźniejszych nowotworów na świecie, częściowo dlatego, że trudno go wykryć i sklasyfikować na tyle wcześnie, by zastosować skuteczne leczenie. Lekarze często polegają na ultradźwiękach — szybkiej i stosunkowo taniej metodzie — aby poszukać podejrzanych zmian w wątrobie. Na tych ziarnistych, czarno-białych obrazach niebezpieczne guzy i niegroźne zmiany mogą wyglądać bardzo podobnie, nawet dla ekspertów. Artykuł przedstawia nową dużą kolekcję obrazów zaprojektowaną tak, aby komputery mogły nauczyć się je rozróżniać, co może zwiększyć dokładność i dostępność badań wątroby.
Bliższe spojrzenie na zmiany w wątrobie
Dwa częste znaleziska na badaniach wątroby znajdują się na przeciwległych końcach spektrum ryzyka. Rak wątrobowokomórkowy jest pierwotnym nowotworem wątroby, który może zagrażać życiu, jeśli zostanie przeoczony lub wykryty zbyt późno. Naczyniaki natomiast to zwykle niegroźne skupiska naczyń krwionośnych, które rzadko wymagają leczenia. Na podstawowych obrazach ultradźwiękowych oba mogą być jednak trudne do odróżnienia, szczególnie gdy tkanka wątroby jest już uszkodzona albo zmiany są małe. Dziś lekarze często muszą zlecać dodatkowe badania, takie jak tomografia komputerowa (CT) czy rezonans magnetyczny (MRI), aby mieć pewność, co wiąże się z dodatkowymi kosztami, czasem oraz ekspozycją na promieniowanie lub środki kontrastowe.
Budowanie dużej biblioteki obrazów wątroby
Aby sprostać temu problemowi, badacze z Samsung Medical Center w Seulu zgromadzili SMC-LUD, nowy publiczny zbiór 5 385 obrazów ultradźwiękowych wątroby pochodzących od 1 021 rzeczywistych pacjentów, badanych w latach 2015–2024. Każde zdjęcie pokazuje zmianę w wątrobie, która została starannie zaklasyfikowana do jednej z dwóch grup: nowotwór (rak wątrobowokomórkowy, 2 716 obrazów) lub naczyniak łagodny (2 669 obrazów). Przypadki raka potwierdzono badaniem tkanki pobranej podczas zabiegu chirurgicznego lub biopsji, podczas gdy naczyniaki rozpoznano na podstawie charakterystycznych cech obrazowych ocenianych przez doświadczonych radiologów. Wszystkie obrazy zostały zanonimizowane, pogrupowane według pacjenta i dwukrotnie sprawdzone przez specjalistów, by zapewnić wiarygodne etykiety. 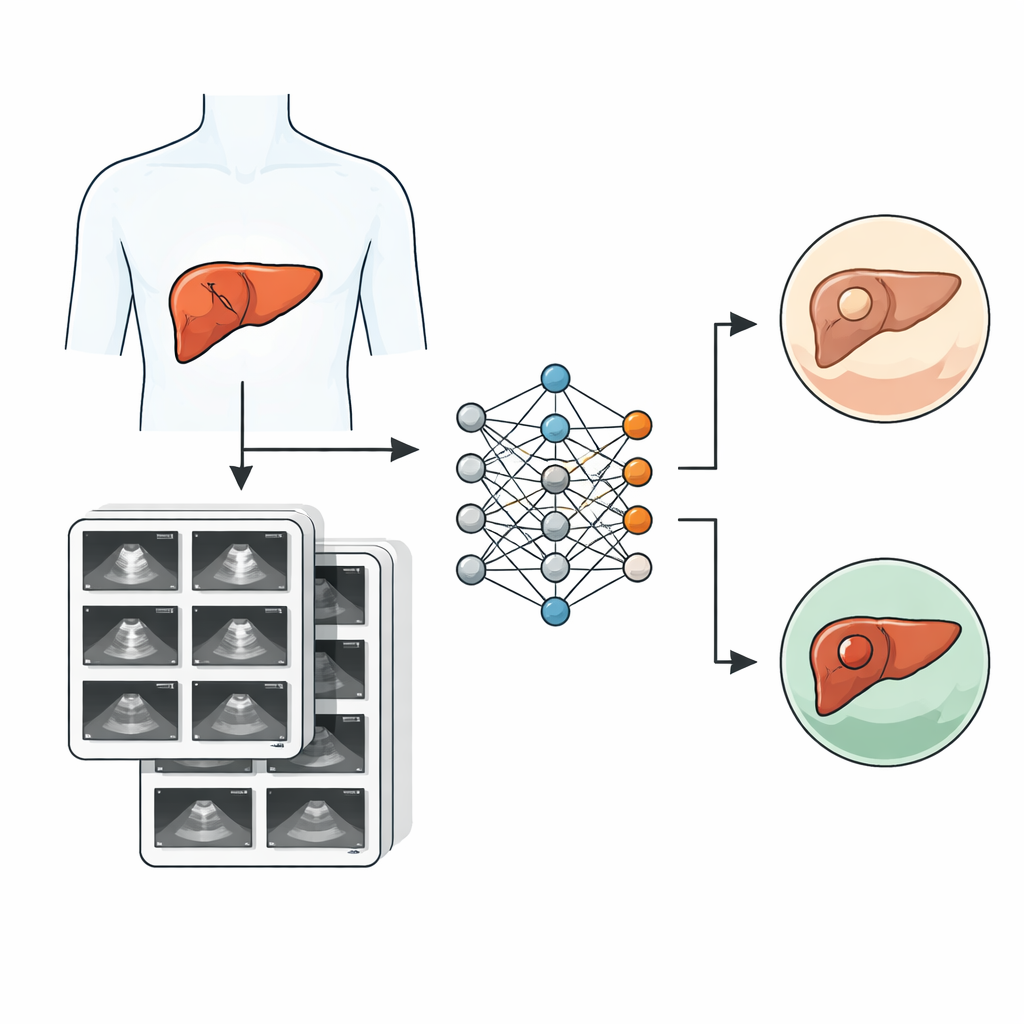
Przygotowanie danych dla inteligentnych algorytmów
Zespół zorganizował zbiór danych tak, by ułatwić jego wykorzystanie badaczom zajmującym się sztuczną inteligencją. Obrazy zostały przeskalowane i ustandaryzowane, aby modele komputerowe oglądały je w jednolitym formacie, a dane podzielono na oddzielne zbiory do trenowania, dostrajania i testów końcowych, z zachowaniem zasad, by obrazy tego samego pacjenta nigdy nie pojawiły się w więcej niż jednej grupie. Zbiór dostępny jest w dwóch wariantach: wersji „Clean” bez znaczników pomiarowych oraz wersji „Caliper”, która je zawiera. Dla uczciwych porównań badacze trenowali swoje modele wyłącznie na obrazach Clean, aby uniknąć ryzyka, że algorytmy nauczą się wiązać wzory znaczników z określonymi diagnozami zamiast skupiać się na samych zmianach. Towarzysząca tabela z informacjami o pacjentach, takimi jak rozmiar guza i jego stadium w przypadkach raka, pozwala na głębsze analizy kliniczne.
Jak komputer uczy się widzieć
Aby pokazać, co można osiągnąć z tym zasobem, autorzy zbudowali model uczenia głębokiego oparty na dobrze znanym systemie rozpoznawania obrazów i rozbudowali go o specjalne moduły „uwagi” (attention). Te komponenty pomagają sieci skupić się na najbardziej informatywnych fragmentach obrazu oraz na najbardziej wymownych wzorcach jasności i tekstury. Konstrukcja wykorzystuje dwie równoległe gałęzie, które przetwarzają te same cechy w nieco inny sposób, zanim ponownie się połączą, a następnie stosuje filtr przestrzenny, który uwypukla istotne obszary — podobnie jak radiolog mentalnie przybliżający podejrzane miejsce. Trenowany na podzbiorze SMC-LUD Clean, model ten porównano z kilkoma popularnymi architekturami sieci neuronowych stosowanych w obrazowaniu medycznym. 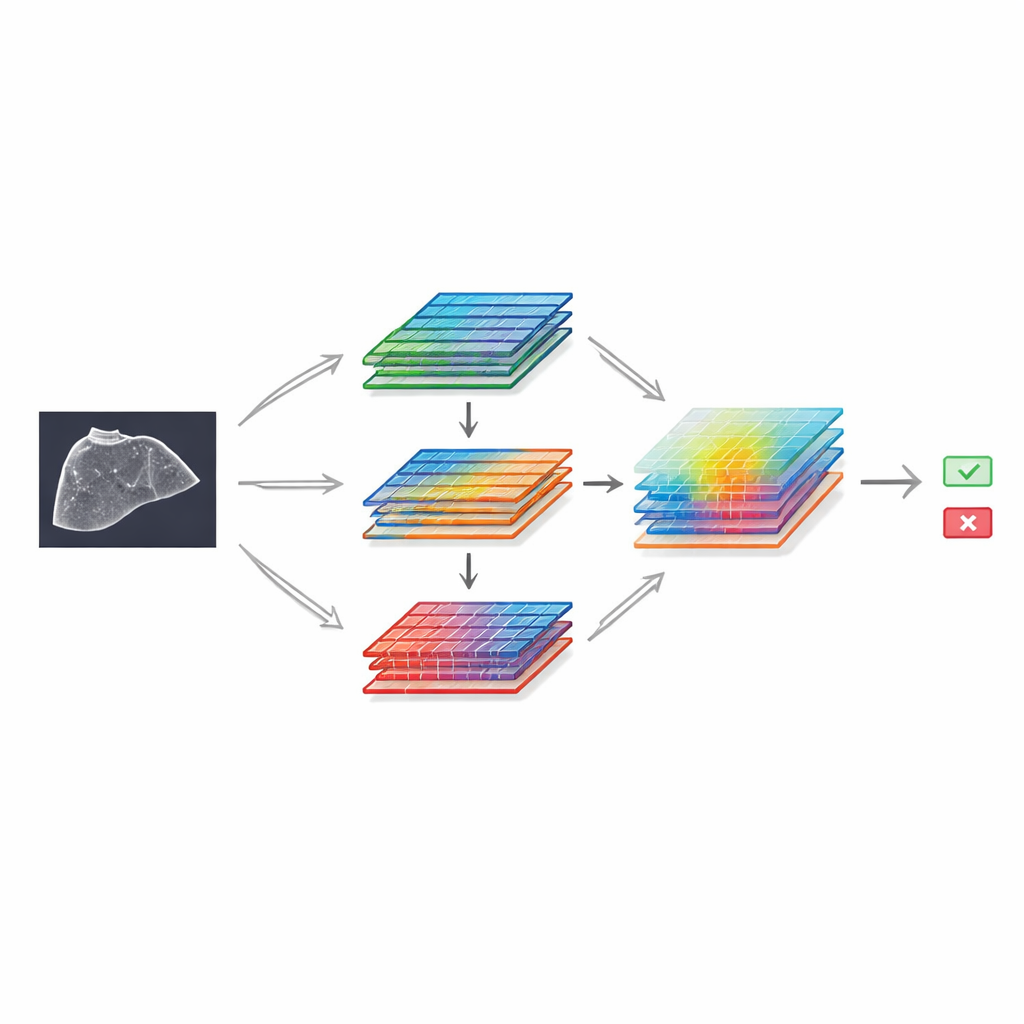
Co pokazują wyniki
Na wydzielonym zbiorze testowym model z modułami uwagi poprawnie rozróżniał raka wątroby od naczyniaka niemal w 99% przypadków, przewyższając modele porównawcze. Mapy cieplne wygenerowane z wewnętrznych obliczeń sieci wykazywały, że model miał tendencję do koncentrowania uwagi na samych zmianach, a nie na niezwiązanych szczegółach obrazu, co sugeruje, że uczył się medycznie istotnych wskazówek. Choć badanie ocenia jedynie dwuwarunkowe rozróżnienie między jednym typem zmiany złośliwej i jednym łagodnym, jego wyniki podkreślają zarówno jakość etykiet obrazów, jak i potencjał diagnostyki ultradźwiękowej wspomaganej komputerowo, gdy dysponuje się wystarczająco dużymi, dobrze uporządkowanymi danymi.
Co to może znaczyć dla pacjentów
Dla osób niezajmujących się medycyną kluczowy komunikat jest taki, że sam ten zbiór danych nie zmieni sposobu, w jaki lekarz oceni twoje następne badanie — ale stanowi ważny fundament. Dzięki bezpłatnemu udostępnieniu dużej, starannie zweryfikowanej biblioteki obrazów ultradźwiękowych autorzy dostarczają badaczom na całym świecie surowego materiału potrzebnego do trenowania i testowania inteligentniejszych narzędzi do przesiewania wątroby. W przyszłości takie narzędzia mogłyby pełnić rolę drugiej pary oczu, sygnalizując niepokojące zmiany wymagające bliższej uwagi i ograniczając niepotrzebne badania uzupełniające przy jednoznacznie łagodnych obrazach. Ostatecznie może to przyczynić się do przesunięcia wykrywania raka wątroby ku wcześniejszym, bardziej uleczalnym stadiów przy jednoczesnym kontrolowaniu kosztów i złożoności procedur.
Cytowanie: Tak, J., Ko, RE., Kwon, R.D. et al. SMC-LUD:Large-Scale B-Mode Liver Ultrasound Dataset for Hepatocellular Carcinoma and Hemangioma Classification. Sci Data 13, 649 (2026). https://doi.org/10.1038/s41597-026-07023-7
Słowa kluczowe: ultrasonografia wątroby, rak wątrobowokomórkowy, naczyniak, uczenie głębokie, zbiór danych obrazowych medycznych